Природа связи углерод-металл
ЛЕКЦИЯ 21
МЕТАЛЛОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
Способы получения из галогенпроизводных и углеводородов, обладающих СН-кислотностью.
Природа связи углерод-металл.
Химические свойства магний- и литийорганических соединений: взаимодействие с протонодонорными соединениями, галогенпроизводными углеводородов, карбонильными соединениями, производными карбоновых кислот, оксиранами и диоксидом углерода.
Использование в синтезе медь- и ртутьорганических соединений.
Металлоорганические соединения— органические соединения, в молекулах которых существует связь атома металла с атомом/атомами углерода.
По характеру связи они разделяются на 2 типа:
1) с σ-связью (например, (СН3)3Al, C2H5MgI, C4H9Li) и
2) с π-связью (например, ферроцен и бис-π-аллил-никель).
Соединения первого типа образуют преимущественно непереходные металлы, соединения второго типа — переходные.
Металлоорганические соединения широко применяют для самых разнообразных синтезов и в различных производствах.
Магний- и литийорганические соединения являются наиболее важными типами металлорганических соединений.
1.1. Номенклатура металлорганических соединений.
Названия МОС образуют от названий углеводородного радикала и металла, например:
н-BuLi (C2H5)2Mg RMgCl
бутиллитий диэтилмагний алкилмагнийхлорид
Рис. 21.1. Номенклатура металлорганических соединений
1.2. Методы получения литий- и магнийорганических соединений. Универсальным методом получения литий- и магнийорганических соединений является взаимодействие металлов с алкил- и арилгалогенидами в безводном апротонном растворителе.
1.2.1. Получение литийорганических соединений.
1. Литийорганические соединения образуются при взаимодействии металлического лития с галогенводородами (RHal) в растворителях, которые взаимодействуют с ионом металла (сольватируют металлорганические соединения), например, в тетрагидрофуране (ТГФ ), в эфире и др.
2. Реакцию проводят в инертной атмосфере (N2 или аргон, при температуре –30оС), чтобы избежать реакции окисления кислородом воздуха:
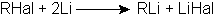
Рис. 21.2. Схема реакции синтеза литийорганических соединений из алкил- и
Арилгалогенидов
3. Обычно литийорганические соединения в чистом виде не получают и не используют, так как они энергично реагируют с O2, CO2, H2O и может произойти самовоспламенение. Поэтому их получают в растворах, и сразу в таком виде используютв дальнейших реакциях.
1.2.2. Получения магнийорганических соединений.
Магнийорганические соединения бывают 2-х типов:
- с одним углеводородным остатком – RMgXal,
- с двумя углеводородными остатками – R2Mg(диалкилмагний).
Магнийорганические соединения получают прямым взаимодействием Mg (в виде стружки) с галогенпроизводными (RX) обычно в растворе безводного диэтилового эфира или тетрагидрофурана:
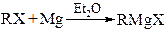
Рис. 21.3. Схема реакции синтеза литийорганических соединений из алкил- и
Арилгалогенидов
Эту реакцию открыл французский химик Гриньяр (1901 г.) и она носит его имя – реакция Гриньяра, а магнийорганические соединения часто называют реактивами Гриньяра.
Доказано, что реакции образования магнийорганических соединений протекают по радикальному механизму:
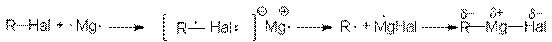
Рис. 21.4. Радикальный механизм синтеза литийорганических соединений из алкил- и
Арилгалогенидов
Вероятно, таков же механизм образования литийорганических соединений.
Природа связи углерод-металл
Связь углерод-металл в органических соединениях лития и магния сильно поляризована, причем электронная плотность ее смещена в сторону более электроотрицательного атома углерода.
