Вращение вокруг простой углерод-углеродной связи. Конформации
И.С. Колпащикова, Е.Р. Кофанов, Е.М. Алов
УГЛЕВОДОРОДЫ.
ГАЛОГЕНПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
Рекомендовано научно-методическим советом университета в качестве учебного пособия для студентов высших учебных заведений, обучающихся по химико-технологическим направлениям подготовки дипломированных специалистов
Ярославль 2007
УДК 547
ББК 24.23
К 60
Колпащикова И.С., Кофанов Е.Р., Алов Е.М.
К 60 Углеводороды. Галогенпроизводные углеводородов: Учебное пособие. – Ярославль: Изд-во ЯГТУ, 2007. – 247 с.
ISBN 978-5-9914-0023-7
В пособии рассмотрены основные вопросы строения и реакционной способности, типичные реакции и основные способы получения ациклических, карбоциклических и ароматических соединений, а также галогенпроизводных углеводородов. Пособие составлено с учетом важнейших достижений органической химии за последние годы.
Предназначено для студентов специальности «Химическая технология органических веществ», а также может быть рекомендовано для студентов дневной и заочной формы обучения всех специальностей химико-технологического факультета.
Ил. 52. Табл. 18. Библиогр. 5.
Рецензенты: кафедра общей и биоорганической химии Ярославского государственного университета; М.В. Дорогов, д-р хим. наук, профессор, заведующий кафедрой органической химии Ярославского государственного педагогического университета им. К.Д. Ушинского.
УДК 547
ББК 24.23
ISBN 5-230-20643-8
© Ярославский государственный технический университет, 2007
АЛКАНЫ
Гомологический ряд, изомеры
Алканами называются углеводороды с открытой цепью, имеющие общую формулу СnН2n+2 и содержащие только простые углерод-углеродные связи.
Алканы образуют гомологический ряд (табл. 1.1). Гомологический ряд- это ряд соединений, в котором каждый член отличается от предыдущего на постоянную структурную единицу СН2, называемую гомологической разностью. Члены этого ряда называются гомологами.
Таблица 1.1
Гомологический ряд алканов. Число структурных изомеров
| Число атомов | Название, формула | Число изомеров | |
| I | Метан | СН4 | I |
| Этан | C2H6 | I | |
| Пропан | C3H8 | I | |
| Бутан | С4Н10 | ||
| Пентан | С5Н12 | ||
| Гексан | С6Н14 | ||
| Гептан | С7Н16 | ||
| Октан | С8Н18 | ||
| Нонан | С9Н20 | ||
| Декан | С10Н22 |
| Изомерами называются соединения, имеющие одинаковый состав, но различное строение и обладающие вследствие этого различными физическими и химическими свойствами. |
Изомеры могут быть разделены на два класса: структурные изомеры и пространственные изомеры (стереоизомеры).
| Структурные изомеры - это соединения, имеющие одинаковый состав, но различную последовательность связывания атомов. | |
| Пространственными изомерами называются соединения, в которых одинаковые состав и способ связывания атомов, но различное расположение атомов в пространстве. | |
Первые три члена гомологического ряда не имеют изомеров. Число структурных изомеров последующих гомологов, начиная с бутана, растет очень быстро с увеличением атомов углерода в молекуле (см. табл. 1.1). Эмпирической формуле С4Н10 соответствуют два структурных изомера, а формуле С5Н10 – три
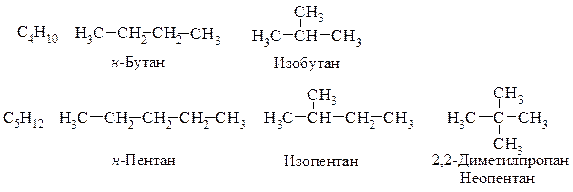
Строение метана
Электронная конфигурация основного состояния атома углерода ls22s2 2p2:
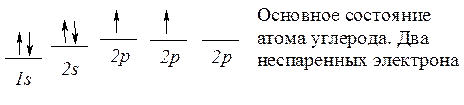
Можно было бы ожидать, что такой атом углерода будет образовывать с двумя атомами водорода соединение СН2. Но в метане углерод связан с четырьмя атомами водорода. Для того чтобы представить образование молекулы СН4, необходимо обратиться к его возбужденному электронному состоянию.
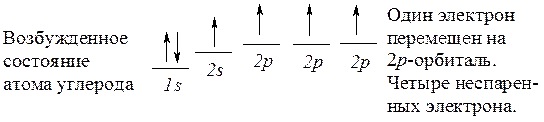
Теперь можно ожидать, что атом углерода образует четыре связи с атомами водорода, но эти связи неравноценны: три связи образованы с использованием р-орбиталей, одна - с использованием s-орбитали. Это противоречит известному факту: все связи в метане эквивалентны.
Далее проводят гибридизацию орбиталей. Математически рассчитаны различные комбинации одной s- и трех р-орбиталей. Гибридные орбитали с наибольшей степенью направленности ("лучшие" орбитали) в результате большего перекрывания дают связи (1) прочнее, чем негибридизованные s- или р-орбитали. Четыре "лучшие" гибридные орбитали (2) эквивалентны. Они направлены к вершинам правильного тетраэдра, угол между двумя орбиталями 109,5о. Такая геометрия обеспечивает (3) минимальное отталкивание между ними.
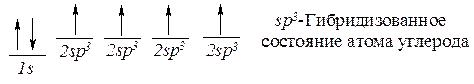
 | 2sp3-орбиталь, большая доля образует s-связи |
Завершим картину построения молекулы метана: каждая из четырех sp3-орбиталей атома углерода перекрывается с 1s-орбиталью атома водорода. Образуются четыре s -связи.
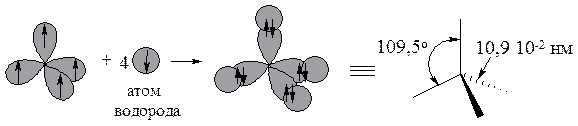 | ||||
| sp3‑гибридное состояние атома углерода | молекула метана имеет четыре s-связи | изображение метана с помощью клиновидной проекции |
Для максимального перекрывания sp3-орбиталей углерода и 1s-орбиталей водорода четыре водородных атома должны лежать на осях sр3-орбиталей. Следовательно, угол между двумя любыми связями С–Н равен 109,5о.
Экспериментальные данные подтверждают расчет: метан имеет тетраэдрическую структуру. Все связи углерод-водород имеют одинаковую длину 10,9·10-2 нм, угол между двумя любыми связями тетраэдрический и равен 109,5о. Для разрыва одной из связей в метане требуется 427·103 Дж/моль.
Строение этана
Построение следующего гомолога ряда алканов - этана H3C–CH3 произведем аналогичным образом. Как и в случае с метаном, С–Н связи возникают благодаря перекрыванию sp3-орбиталей атома углерода с 1s-орбиталями атомов водорода, связь углерод-углерод образуется в результате перекрывания двух sp3-орбиталей атомов углерода.
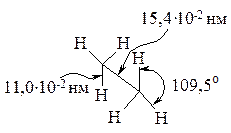
В молекуле этана содержится шесть s-связей углерод-водород и одна s-связь углерод-углерод. s-Связи имеют цилиндрическую симметрию*. Ось симметрии электронного облака s-связи - линия, соединяющая атомы. Электронное облако углерод-углеродной s-связи, обладающее цилиндрической симметрией, можно изобразить следующим образом:

Вращение вокруг простой углерод-углеродной связи. Конформации
В молекуле этана поворот одной метильной группы относительно другой происходит почти свободно.
| Различные расположения групп и атомов в пространстве, возникающие в результате поворота одного атома относительно другого вдоль линии связи, соединяющей эти атомы, называются конформациями. | |||
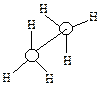 | 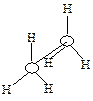 | ||
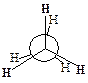 | 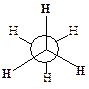 | ||
| Заслоненная конформация этана (I) | Заторможенная конформация этана (II) | ||
Однако вращение одной метильной группы относительно другой не совсем свободно. Потенциальная энергия молекулы минимальна для заторможенной конформации II, при вращении метильной группы она возрастает и достигает максимума для заслонённой конформации I. Избыток энергии заслонённой конформации по сравнению с заторможенной называют энергией торсионного напряжения. Для молекулы этана эта энергия равна 13·103 Дж/моль (рис. 1.1).
Считают, что избыток энергии появляется вследствие отталкивания электронных облаков углерод-водородных связей в тот момент, когда они проходят мимо друг друга. Поскольку при комнатной температуре энергия некоторых столкновений молекул может достигать 86·103 Дж/моль, то барьер в 13·103 Дж/моль легко преодолевается. Вращение в этане рассматривают как свободное.
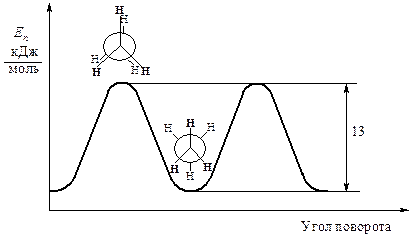
Рис. 1.1. Энергетический профиль вращения групп CH3 в молекуле этана вокруг связи углерод-углерод
Конформации, соответствующие энергетическим минимумам, называют конформационными изомерами или конформерами. В более сложных молекулах число конформеров может быть достаточно большим.
Физические свойства
Физические свойства алканов определяются их строением. Ковалентные связи в алканах неполярные (С-С) или малополярные (С-Н). Эти связи симметричны, полярность их взаимно компенсируется, поэтому молекула алкана неполярна. Силы межмолекулярного притяжения сравнительно слабы. Это является причиной небольших значений плотности, температуры кипения и плавления.
В молекуле углеводорода суммарный дипольный момент равен нулю. Однако распределение электронной плотности в каждый момент времени меняется и возникает небольшой диполь. Этот кратковременно существующий диполь будет влиять на распределение электронной плотности соседней молекулы, таким образом, мгновенный диполь одной молекулы индуцирует противоположно ориентированный диполь в соседней молекуле. В результате между молекулами возникают силы притяжения, которые называются дисперсионными. Дисперсионные силы действуют на очень небольшом расстоянии, между поверхностями молекул. Можно ожидать, что чем больше молекула и чем больше её поверхность, тем больше межмолекулярные силы.
Температуры кипения, плавления и плотность увеличиваются с увеличением молекулярной массы (рис. 1.2). Алканы С1 ...С4 - газы, С5 ...С16 - жидкости, далее - твёрдые кристаллические вещества. За исключением низших алканов, температура кипения повышается на 20 - 30 ºС с ростом углеродной цепи на один атом углерода. Такая закономерность изменения температуры кипения характерна для гомологических рядов других классов соединений.
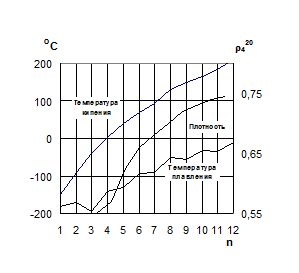
Рис. 1.2. Зависимость температур кипения, плавления и плотностей алканов с неразветвленной цепью от числа атомов углерода (n)
Изомер с разветвлённой цепью имеет более низкую температуру кипения, чем изомер нормального строения.
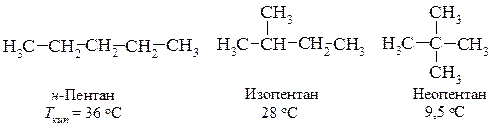
Понижение температуры кипения у изомеров с появлением разветвлений и увеличением их числа объясняется тем, что с увеличением разветвлений форма молекулы стремится к сферической, то есть уменьшается её поверхность, а следовательно, и межмолекулярные силы притяжения. Такая зависимость между формой молекулы и температурой кипения наблюдается и для других классов соединений.
Процесс плавления требует преодоления межмолекулярных сил в твердом теле. Межмолекулярные силы в кристалле зависят не только от размера молекул, но также и от того, как они упакованы в кристаллической решетке. Углеводород с линейной цепью н-пентан плавится при температуре минус 130 оС, а его изомер неопентан, молекулы которого имеют сферическую форму и более плотно упакованы в кристаллической решетке, плавится при более высокой температуре минус 17 оС.
Алканы, неполярные соединения, растворимы в неполярных растворителях (бензол, тетрахлорметан), но нерастворимы в полярных растворителях.
Алканы - диэлектрики с низким значением диэлектрической постоянной (e @ 2) и меньшим значением показателя преломления по сравнению с показателем преломления углеводородов с кратными связями. Показатель преломления показывает способность молекул вещества поляризоваться под действием внешнего электрического поля (переменного электромагнитного поля светового луча, электрического поля ионного реагента, растворителя). Это свойство вещества называется поляризуемостью. Малые значения показателей преломления алканов свидетельствуют о низкой поляризуемости этих соединений.
В инфракрасных спектрах алканов наблюдаются полосы поглощения валентных колебаний nС–Н в области 2800 - 3000 см-1 .
Химические свойства
В молекулах алканов ковалентные связи малополярные и слабополяризуемые. Поэтому они нечувствительны к ионным реагентам, инертны по отношению к кислотам, основаниям, окислителям. Для взаимодействия с ионными реагентами требуется достаточно высокая полярность атакуемых химических связей, обеспечивающая электростатическое притяжение разноименно заряженных активных центров, и/или способность атакуемой связи поляризоваться под влиянием заряда ионного реагента. Алканы в ничтожной степени обладают и тем и другим свойством.
Сравните энергии гетеролитического (а) и гомолитического (б) разрывов связей С–Н в метане:
а). СН4 ® СН3+ + Н- + DНº DНº = 1313·103 Дж/моль
б). СН4 ® СН3·+ Н·+ DНº DНº = 435·103 Дж/моль
Наиболее характерным свойством алканов является свободнорадикальное замещение незаряженного атома водорода при действии незаряженных свободнорадикальных реагентов: атомов хлора и брома при галогенировании, NO2· при нитровании и т.д.
