Определение концентрации раствора кислоты
Цель работы: изучить способы выражения концентрации растворов, научиться рассчитывать концентрацию растворов.
Задание: приготовить приблизительно 0,1 н. раствор соляной кислоты и установить нормальность и титр кислоты. Выполнить требования к результатам работы, оформить отчет, решить задачу.
Теоретическое введение
Один из методов определения концентрации растворов – объемный анализ. Он сводится к измерению объемов реагирующих веществ, концентрация одного из которых известна.
Такое измерение производится постепенным прибавлением одного раствора к другому до окончания реакции. Этот процесс называется титрованием. Окончание реакции определяется с помощью индикатора.
При определении объемов растворов целесообразно использовать следующие способы выражения концентрации растворов:
Молярная концентрация эквивалентов вещества Вили нормальность(сэк (В) или н.) – отношение количества эквивалентов растворенного вещества к объему раствора:
 , моль/л,
, моль/л,
где nэк (В) – количество эквивалентов вещества В, моль; mB – масса вещества В, г; Мэк (В) – молярная масса эквивалентов вещества В, г/моль; Vр – объем раствора, л.
Массовая доля растворенного вещества В(ωВ) – отношение (обычно – процентное) массы растворенного вещества к массе раствора:
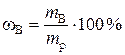 ,
,
где mB – масса вещества В, г; mр – масса раствора, г.
Если выражать массу раствора через его плотность (ρ) и объем (Vр), то
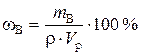 .
.
Титр раствора вещества В(ТВ) показывает массу растворенного вещества, содержащуюся в 1 мл (см3) раствора:
 , г/мл,
, г/мл,
где mB – масса растворенного вещества В, г; Vp – объем раствора, мл.
Титр также можно рассчитать по формуле
 , г/мл,
, г/мл,
где Мэк (В) – молярная масса эквивалентов вещества В, г/моль; сэк(В) – молярная концентрация эквивалентов, моль/л.
Выполнение работы
Опыт 1. Приготовление приблизительно 0,1 н. раствора соляной кислоты
(Проводить в вытяжном шкафу!). Налить в цилиндр концентрированный раствор соляной кислоты и ареометром определить его плотность.
По измеренной плотности по табл. Б. 2 найти массовую долю (%) кислоты в растворе. Рассчитать массу кислоты, необходимую для приготовления 250 мл 0,1 н. раствора HCl по формуле
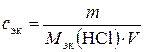 , откуда m = сэк·Мэк (HCl)·V,
, откуда m = сэк·Мэк (HCl)·V,
где сэк – молярная концентрация эквивалентов, моль/л; m – масса кислоты, г; Мэк(HCl) – молярная масса эквивалентов кислоты, г/моль; V – объем кислоты, л.
Полученную величину (m) пересчитать на объем, который требуется для приготовления 250 мл 0,1 н. раствора кислоты по формуле
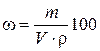 , откуда V =
, откуда V = 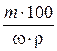 ,
,
где V – объем кислоты, мл; m – масса кислоты,г; ω – массовая доля в % HCl, найденная по табл. Б. 2; ρ – плотность кислоты, г/мл, измеренная ареометром.
Пипеткой отобрать рассчитанный объем раствора кислоты, перенести его в мерную колбу, разбавить водой до метки и хорошо перемешать.
Опыт 2. Установление нормальности и титра кислоты
Отмерить пипеткой 10 мл приготовленного раствора кислоты, перенести его в коническую колбу, добавить 1–2 капли фенолфталеина.
В бюретку налить 0,1 н. раствор NaOH. Оттитровать раствор кислоты. Для этого медленно приливать из бюретки щелочь в колбу с раствором кислоты, непрерывно перемешивая его в процессе титрования. Место, в которое падают капли щелочи, окрашивается в розовый цвет, исчезающий при взбалтывании.. Титрование проводить до тех пор, пока от одной капли щелочи раствор примет неисчезающую окраску. Появление окраски означает, что кислота полностью нейтрализована щелочью. Первое титрование – ориентировочное. Повторить титрование еще три раза. Расхождение между последними тремя титрованиями не должно превышать 0,1 мл.
Требования к результату опыта
Данные опыта занести в табл. 7.1:
Таблица 7.1
