Гидрирование галогеналканов
При каталитическом гидрировании галогеналканов в присутствии палладия образуются алканы.
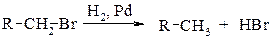
Для восстановления галогеналканов можно использовать также цинк в соляной кислоте и натрий в спирте. Иодалканы могут быть восстановлены нагреванием в запаянной ампуле с иодоводородом.

Декарбоксилирование карбоновых кислот
При нагревании солей карбоновых кислот и щелочных или щелочноземельных металлов с гидроксидами натрия или бария происходит отщепление СО2 и образуется алкан.
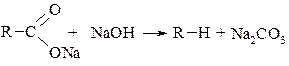
Однозначно эта реакция протекает только для ацетата натрия, в случае других солей образуются побочные продукты.
Синтез Кольбе
При электролизе натриевых и калиевых солей карбоновых кислот образуются углеводороды симметричного строения.
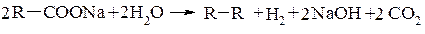
На первой стадии происходит анодное окисление анионов кислот до радикалов RСОО·, которые отщепляют СО2, а затем димеризуются. На катоде образуется водород и гидроксид щелочного металла.
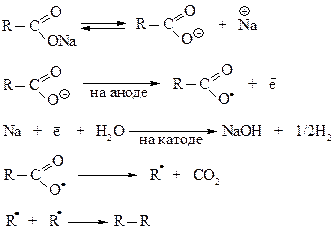
Метод Фишера-Тропша
Каталитическое гидрирование окиси углерода протекает в присутствии катализатора, содержащего кобальт или железо, с образованием смеси алканов с небольшой молекулярной массой.
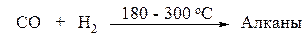
СТЕРЕОИЗОМЕРИЯ. ЭНАНТИОМЕРИЯ
Энантиомеры. Хиральность. Условия хиральности

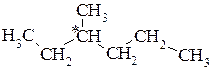
Наряду со структурными изомерами в ряду алканов существуют пространственные изомеры. Это можно представить на примере 3-метилгексана.
Атом углерода, обозначенный С*, соединён с четырьмя разными группами. В этом углеводороде при одном и том же порядке связывания атомов алкильные группы могут быть по-разному расположены в пространстве около атома углерода С*. Существует несколько способов изображения пространственных изомеров на плоскости (рис. 2.1, 2.2).
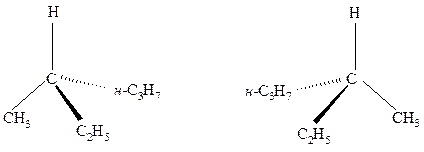
Рис. 2.1. Объемное изображение с помощью «клиньев»

Рис. 2.2. Проекционные формулы Фишера
На рисунке 2.2 в центре находится атом углерода С*, горизонтальной линией обозначена связь между углеродом С* и группами, выступающими перед плоскостью рисунка, а вертикальной - между атомом С* и группами, расположенными за плоскостью рисунка. Проекции Фишера можно поворачивать только в плоскости рисунка и только на 180о, но не на 90о или 270о. Этими формулами изображены два различных соединения. Они отличаются друг от друга так же, как предмет и его зеркальное изображение или как левая и правая рука. Левая и правая руки - два очень похожих друг на друга предмета, но совместить их невозможно (не надеть левую перчатку на правую руку), значит - это два разных объекта.
| Два соединения: предмет и его зеркальное изображение (I и II), несовместимые друг с другом, называются энантиомерами (от греческого “энантио” - противоположный). |
| Свойство соединения существовать в виде энантиомеров называется хиральностью (от греческого “хирос” - рука), а само соединение - хиральным. |
Молекула обладает хиральностью, если она не имеет плоскости симметрии. Существует ряд элементов структуры, которые могут сделать молекулу не идентичной своему зеркальному изображению. Наиболее важным из них является хиральный атом углерода.
| Хиральный атом или хиральный центр - это атом углерода, связанный с четырьмя различными группами и обозначае-мый С*. |
Молекула 2-метилгексана не имеет плоскости симметрии и поэтому может существовать в виде энантиомеров (см. рис. 2.1).
Молекула, в которой при атоме углерода находятся две или более одинаковых групп, имеет плоскость симметрии и, следовательно, не обладает хиральностью, поскольку молекула и ее зеркальное изображение идентичны. Такие молекулы называются ахиральными.
Например, изопентан не может существовать в виде энантиомеров и не обладает хиральностью (рис. 2.3).

Рис. 2.3. Молекула изопентана ахиральна
Другой элемент структуры, который делает молекулу способной существовать в виде энантиомеров, - хиральные аллены. Молекула незамещенного аллена (пропадиена) ахиральна.
В молекуле аллена две плоскости, в которых лежат две концевые метиленовые группы CH2, взаимно перпендикулярны.

Вследствие этого замещенные аллены типа XYC=C=CXY не имеют плоскости симметрии и могут существовать в виде энантиомеров.

Еще одним примером могут быть производные бифенила, в которых заместители в орто-положениях достаточно велики для того, чтобы свободное вращение оказалось невозможным. Они могут существовать в виде энантиомеров, несмотря на отсутствие хиральных атомов. Такой вид изомерии называется атропоизомерией.

Не всегда соединения, не имеющие плоскости симметрии, обладают хиральностью и могут быть разделены на энантиомеры. Например, в метилэтиламине CH3(C2H5)NH азот имеет четыре разных заместителя: H, CH3, C2H5 и неподеленную пару электронов, которые лежат в вершинах тетраэдра.
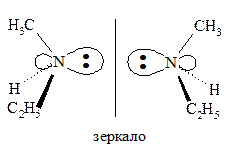
Казалось бы, такое соединение должно существовать в виде энантиомеров и проявлять оптическую активность. Однако невозможность расщепить этот амин на энантиомеры вызвана конфигурационной нестабильностью метилэтиламина, один энантиомер быстро превращается в другой.

Инверсия пирамиды метилэтиламина I → II и II → I осуществляется через плоский ахиральный атом азота. Значит, метилэтиламин состоит из эквимолекулярной смеси энантиомеров, поэтому не разделяется на индивидуальные энантиомеры и не проявляет оптической активности.
Если же в этом амине за счет неподеленной пары электронов образуется связь, которая не позволяет молекуле «выворачиваться», то частица становится конфигурационно устойчивой.
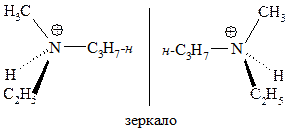
Катион метиэтилпропиламмония существует в виде энантиомеров.
Следовательно, соединения, которые не имеют плоскости симметрии, могут существовать в виде энантиомеров и проявлять оптическую активность только в том случае, когда они конфигурационно устойчивы.
Энантиомеры проявляют одинаковые физические свойства, кроме одного. Например, молекула 2-бромбутана существует в виде двух энантиомеров. Они имеют одинаковые температуры кипения, плавления, плотность, растворимость, показатели преломления. Отличить один энантиомер от другого можно по знаку вращения плоскополяризованного света. Энантиомеры вращают плоскость поляризованного света на один и тот же угол, но в разные стороны: один – по часовой стрелке, другой – на такой же угол, но против часовой стрелки.
Энантиомеры обладают одинаковыми химическими свойствами, скорость их взаимодействия с реагентами, не обладающими хиральностью, одинакова. В случае реакции с оптически активным реагентом скорости реакций энантиомеров различны. Иногда они отличаются настолько, что реакция данного реагента с одним из энантиомеров не протекает совсем.
