Комплексные соединения и органические реагенты
1. ЗНАЧЕНИЯ СТУПЕНЧАТЫХ КОНСТАНТ Кn С ВОЗРАСТАНИЕМ N УМЕНЬШАЮТСЯ. ЭТА ЗАКОНОМЕРНОСТЬ НЕ ВЫПОЛНЯЕТСЯ В СЛУЧАЕ
1) когда при комплексообразовании меняется координационное число иона металла
2) когда проявляется специфическое пространственное влияние лиганда
3) когда происходит изменение электронной структуры иона металла в процессе комплексообразования
4) во всех описанных случаях приведенная закономерность не выполняется
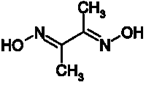
2. ДИМЕТИЛГЛИОКСИМ ЯВЛЯЕТСЯ СЕЛЕКТИВНЫМ РЕАГЕНТОМ В КИСЛОЙ СРЕДЕ ДЛЯ ИОНОВ
1) для ионов никеля
2) для ионов железа
3) для ионов палладия
4) для ионов меди
5) для ионов кобальта
3. ДЛЯ ОБНАРУЖЕНИЯ ИОНОВ ЖЕЛЕЗА (III) ИСПОЛЬЗУЮТСЯ КОМПЛЕКСЫ
1) тиоцианатные
2) фторидные
3) цианидные
4) фосфатные
5) хлоридные
4. ОРГАНИЧЕСКИЙ РЕАГЕНТ ЭТО
1) органическое соединение сложной структуры
2) органическое соединение, применяющееся для маскировки
3) органические соединения, применяющиеся для экстракции комплексов металлов
4) органические соединения, содержащие функционально- аналитическую группу
5) нет правильного ответа
5. МАКСИМАЛЬНОЕ КООРДИНАЦИОННОЕ ЧИСЛО ЦЕНТРАЛЬНОГО АТОМА ОПРЕДЕЛЯЕТСЯ
1) природой металла
2) природой лиганда
3) строением органического реагента
4) строением комплексного соединения
5) условиями опыта
6. СНИЗИТЬ ПРЕДЕЛ ОБНАРУЖЕНИЯ ИОНОВ МЕТАЛЛОВ ПРИ ОСАЖДЕНИИ ИХ ОРГАНИЧЕСКИМИ РЕАГЕНТАМИ МОЖНО
1) введением в молекулу реагента гидрофильных заместителей
2) изменением симметрии молекулы органического реагента
3) понизив кислотность осаждения
4) введением в молекулу органического реагента гидрофобных заместителей
7. ФУНКЦИОНАЛЬНО-АНАЛИТИЧЕСКОЙ ГРУППИРОВКОЙ (ФА4) ОРГАНИЧЕСКОГО РЕАГЕНТА НАЗЫВАЕТСЯ
1) группировка атомов, включающая подвижные атомы водорода
2) группировка атомов органического реагента, включающая атомы с неподеленной парой электронов
3) группировка атомов органического реагента, обусловливающая определенный механизм взаимодействия реагента с ионами металлов
8. СМЕШАНО ЛИГАНДНЫЕ КОМПЛЕКСЫ ЭТО
1) комплексы, включающие два центральных атома
2) координационно-ненасыщенные комплексы
3) комплексы, включающие два и более вида лигандов
4) координационно-насыщенные комплексы
5) комплексы с полидентатными лигандами
9. ШИРОКОЕ ИСПОЛЬЗОВАНИЕ КОМПЛЕКСОНОВ В АНАЛИТИЧЕСКОЙ ХИМИИ ОБУСЛОВЛЕНО СЛЕДУЮЩЕЙ ОСОБЕННОСТЬЮ ВЗАИМОДЕЙСТВИЯ КОМПЛЕКСОНОВ С ИОНАМИ МЕТАЛЛОВ
| 1) | полидентатностью комплексонов | ||
| 2) | высокой устойчивостью комплексонатов | металлов | и |
простой стехиометрией (М : У = 1 : 1)
3) различной скоростью образования комплексонатов металлов
4) различной и характерной окраской комплексонатов
5) доступностью реагентов
10. “ХЕЛАТЫ” ЭТО: КОМПЛЕКСЫ С ДОНОРНО- АКЦЕПТОРНОЙ СВЯЗЬЮ МЕТАЛЛ-ЛИГАНД
1) комплексы, у которых центральный атом включен в циклическую структуру
2) комплексы, при образовании которых выделяются ионы
Н3О+
3) соединения с органическими реагентами
4) нет правильного ответа
11. КОМПЛЕКСООБРАЗОВАТЕЛЬ ЭТО
1) ионы или молекулы, принимающие участие в образовании комплексного соединения
2) ионы или молекулы, проявляющие электронодонорные свойства
3) ионы или молекулы, проявляющие электроноакцепторные свойства
4) ионы, группирующие определенным образом другие ионы или молекулы
12. ПОЛИДЕНТАТНЫМ ЯВЛЯЕТСЯ ЛИГАНД
1) NH3
2) F-
3) ЭДТА
4) SCN-
5) C2O42-
13. НАИБОЛЕЕ ВАЖНЫМ ФАКТОРОМ ОБУСЛАВЛИВАЮЩИМ ИЗБИРАТЕЛЬНОСТЬ ДЕЙСТВИЯ ОРГАНИЧЕСКОГО РЕАГЕНТА ЯВЛЯЕТСЯ
1) органический реагент должен быть сильной кислотой
2) комплекс металла с реагентом должен экстрагироваться
3) важно присутствие в растворе других комплексообразующих веществ
4) природа металла
5) природа функционально-аналитической группировки
14. ДИМЕТИЛГЛИОКСИМ ЯВЛЯЕТСЯ СЕЛЕКТИВНЫМ
| РЕАГЕНТОМ | В АММИАЧНОЙ | СРЕДЕ | ДЛЯ | СЛЕДУЮЩЕГО |
| МЕТАЛЛА | ||||
| 1) | железо | |||
| 2) | палладий | |||
| 3) | никель | |||
| 4) | кобальт | |||
| 5) | медь |
15. ПРИ ДОБАВЛЕНИИ К РАСТВОРУ, СОДЕРЖАЩЕМУ ИОНЫ Fe3+, РОДАНИДА АММОНИЯ ОБРАЗУЕТСЯ СЛЕДУЮЩИЙ ТИП КОМПЛЕКСА
1) разнометальный комплекс
2) смешанолигандный комплекс
3) внутрикомплексное соединение
4) координационно-ненасыщенный комплекс
5) координационно-насыщенный комплекс
16. КООРДИНАЦИОННОЕ ЧИСЛО ИОНА МЕТАЛЛА ЗАВИСИТ
1) от природы металла
2) от строения комплекса
3) от природы лиганда
4) от наличия в комплексе водородных связей
5) нет правильного ответа
17. ДЕНТАТНОСТЬЮ ЛИГАНДА ЯВЛЯЕТСЯ
1) число молекул воды, вытесняемое из аквакомплексов металлов при комплексообразовании
2) число координационных мест, занимаемых лигандом во внутренней координационной сфере
3) число атомов, образующих функционально-аналитическую группировку
4) число атомов, присоединяемых во внешней координационной сфере
5) нет правильного ответа
18. ИОННЫМ АССОЦИАТОМ ЯВЛЯЕТСЯ КОМПЛЕКС
1) фосфатный комплекс железа (III)
2) оксалатный комплекс хрома (III)
3) комплекс ЭДТА с магнием
4) сульфатный комплекс кальция
19. НАИБОЛЕЕ УСТОЙЧИВЫМИ ЯВЛЯЮТСЯ СЛЕДУЮЩИЕ ЦИКЛИЧЕСКИЕ СТРУКТУРЫ
1) четырехчленные цикл
2) трехчленные циклы
3) семичленные циклы
4) пятичленные циклы
20. ВНУТРИКОМПЛЕКСНЫМ СОЕДИНЕНИЕМ ЯВЛЯЕТСЯ КОМПЛЕКС
1) (C9H6ON)2Mg 2H2O
2) Ag4[Fe(CN)6]
3) K2[HgI4]
4) (NH4)3[PMo12O40]
5) (C9H6ONH)BiI4
21. ОРГАНИЧЕСКИЕ АНАЛИТИЧЕСКИЕ РЕАГЕНТЫ (ОАР) В АНАЛИТИЧЕСКОЙ ХИМИИ ПРИМЕНЯЮТ В КАЧЕСТВЕ
1) индикаторов
2) титрантов
3) буферных растворов
4) реагентов-осадителей
5) маскирующих агентов
6) реагентов в качественном анализе
7) реагентов для создания ионной силы растворов
22. ФУНКЦИОНАЛЬНО-АНАЛИТИЧЕСКАЯ ГРУППИРОВКА В МОЛЕКУЛЕ ОАР ОТВЕЧАЕТ ЗА
1) образование химической связи с неорганическим ионом
2) проявление аналитического эффекта
3) растворимость аналитической формы
4) образование осадка аналитической формы
5) появление аналитического сигнала
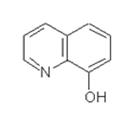
23. ФУНКЦИОНАЛЬНО-АНАЛИТИЧЕСКАЯ ГРУППИРОВКА В МОЛЕКУЛЕ 8-ГИДРОКСИХИНОЛИНА

24.  ПРИ ВЫБОРЕ ТИТРАНТА ДЛЯ ОПРЕДЕЛЕНИЯ Cu2+ C
ПРИ ВЫБОРЕ ТИТРАНТА ДЛЯ ОПРЕДЕЛЕНИЯ Cu2+ C
ИСПОЛЬЗОВАНИЕМ РЕАКЦИИ КОМПЛЕКСООБРАЗОВАНИЯ СЛЕДУЕТ ОТДАТЬ ПРЕДПОЧТЕНИЕ РЕАГЕНТУ (3)
1) NH3
2) (CH3)3N
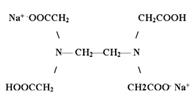
3) (-OOCCH2)2NCH2CH2N(CH2COO-)2
4) SCN-
5) CH3COO-
25. ОСНОВНОЕ ПРЕИМУЩЕСТВО ОРГАНИЧЕСКОГО АНАЛИТИЧЕСКОГО РЕАГЕНТА ПО СРАВНЕНИЮ С НЕОРГАНИЧЕСКИМ ПРИ ИСПОЛЬЗОВАНИИ В КАЧЕСТВЕ ОСАДИТЕЛЯ В ГРАВИМЕТРИЧЕСКОМ АНАЛИЗЕ
1) меньшая растворимость формы осаждения
2) большая молекулярная масса гравиметрической формы
3) меньшая молекулярная масса гравиметрической формы
4) большая летучесть
5) меньшая летучесть
26.
|
| Химические формулы | Названия ОР |
| 1) | а) этилендиаминтетра-ацетат натрия |
|
| 2) | б) диметилглиоксим |
| 3) | в) купферон |
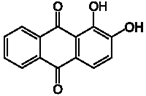
| г) ализарин |
27.
|
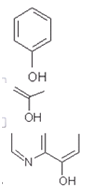
1) ДМГ
2) ализарин
3) ЭДТА
4) купферон
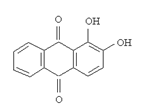
28. 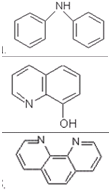 CООТВЕТСТВИЕ МЕЖДУ НАЗВАНИЯМИ ОР И ИХ ХИМИЧЕСКИМИ ФОРМУЛАМИ
CООТВЕТСТВИЕ МЕЖДУ НАЗВАНИЯМИ ОР И ИХ ХИМИЧЕСКИМИ ФОРМУЛАМИ
| Химические формулы | Названия ОAР |
| 1. | а) 8-гидроксихинолин |
| 2. | б) 1,10-фенантролин |
| 3. | в) дифениламин |
| г) ализарин |
| 29. ЧИСЛО ПРИХОДЯЩЕЕСЯ НА | МОЛЕЙ ОДИН | 8-ГИДРОКСИХИНОЛИНА, МОЛЬ АЛЮМИНИЯ ПРИ | |
| ОБРАЗОВАНИИ ХЕЛАТА | |||
| 1) | |||
| 2) | |||
| 3) | |||
| 4) | |||
30. РАСТВОР ФЕРРОИНА ИМЕЕТ КРАСНУЮ ОКРАСКУ, ЕСЛИ ЦЕНТРАЛЬНЫЙ ИОН КОМПЛЕКСООБРАЗОВАТЕЛЬ – FeN+. ВВЕДИТЕ ЗАРЯД КАТИОНА ЖЕЛЕЗА (N)
1) 1+
2) 2+
3) 3+
4) 4+
31. ОТМЕТЬТЕ ПРИЗНАК, НЕ ПОДХОДЯЩИЙ К ПОНЯТИЮ
«КОМПЛЕКСНОЕ СОЕДИНЕНИЕ
1) способность отдельных частей к самостоятельному существованию
2) частичная диссоциация в растворе по гетеролитическому механизму
3) наличие положительно заряженной центральной частицы
4) наличие неподеленной пары электронов
32. ЧИСЛО ДОНОРНЫХ АТОМОВ, ОБРАЗУЮЩИХ СВЯЗЬ С ЦЕНТРАЛЬНЫМ АТОМОМ В КОМПЛЕКСНОМ СОЕДИНЕНИИ НАЗЫВАЕТСЯ
1) дентатность
2) координационное число
3) хелатность
4) изомеризация
Fe2+
33. УСЛОВНАЯ КОНСТАНТА УСТОЙЧИВОСТИ КОМПЛЕКСА С АНИОНОВ ЭТИЛЕНДИАМИНТЕТРАУКСУСНОЙ КИСЛОТЫ
ПРИ pH=2
1) 2,8·1011
2) 2,34·106
3) 1,6
4) 45
34. АКВАКОМПЛЕКСЫ ОБЫЧНО ОКРАШЕНЫ В СЛУЧАЕ
1) полного заполнения d- и f- орбиталей
2) частичного заполнения d- и f- орбиталей
3) наличия хромофорных группировок
4) в присутствии индикаторов
35. НАИБОЛЬШЕЙ УСТОЙЧИВОСТЬЮ ОБЛАДАЕТ КОМПЛЕКС, СОДЕРЖАЩИЙ
1) 5-6 атомов
2) 7 атомов
3) 3 атома
4) 2 атома
36. НЕ СУЩЕСТВУЮТ КОМПЛЕКСЫ
1) внутрисферные
2) внешнесферные
3) полиядерные
4) ауксохромные
37. b 0 = K 0 K 0 ...K
= aMLN
- ЭТО

|
|
|
M L
1) реальная константа устойчивости
2) концентрационная константа устойчивости
3) ступенчатая константа устойчивости
4) общая термодинамическая константа устойчивости
38. НАИБОЛЕЕ РАСПРОСТРАНЁННЫМИ ПОБОЧНЫМИ РЕАКЦИЯМИ С УЧАСТИЕМ ЛИГАНДОВ ЯВЛЯЮТСЯ РЕАКЦИИ
1) окисления-восстановления
2) образования гидрокомплексов
3) протонирования
4) донорно-акцепторные
39. КОМПЛЕКСЫ, ОТЛИЧАЮЩИЕСЯ ВЫСОКОЙ СКОРОСТЬЮ ОБМЕНА ЛИГАНДАМИ, НАЗЫВАЮТСЯ
1) инертные
2) активные
3) лабильные
4) донорные
40. ПОНЯТИЕ «ЖЁСТКОСТИ» И «МЯГКОСТИ» КИСЛОТ ЛЬЮИСА ВВЁЛ
1) Шварценбах
2) Аррениус
3) Брёнстед
4) Пирсон
41. В РЯДУ: ЗАРЯЖЕННЫЕ>НЕЗАРЯЖЕННЫЕ ГИДРОФИЛЬНЫЕ>НЕЗАРЯЖЕННЫЕ ГИДРОФОБНЫЕ КОМПЛЕКСЫ- УМЕНЬШАЕТСЯ
1) растворимость в высокополярных растворителях
2) летучесть комплексных соединений
3) температура плавления
4) интенсивность электронного перехода
42. В ОПТИЧЕСКИХ МЕТОДАХ АНАЛИЗА ДЛЯ ОПРЕДЕЛЕНИЯ МАЛЫХ КОЛИЧЕСТВ МЕТАЛЛОВ ИСПОЛЬЗУЮТ КОМПЛЕКСЫ С ЭЛЕКТРОННЫМ ПЕРЕХОДОМ ТИПА
1) d-d, f-f
2) n-π*
3) π- π*
4) с переносом заряда
43. СОБСТВЕННОЙ ЛЮМИНИСЦЕНЦИЕЙ ОБЛАДАЮТ КОМПЛЕКСЫ
1) f и некоторые d-элементов
2) s, p – элементов
3) только d-элементов
4) d, s – элементов
44. К ФУНДАМЕНТАЛЬНЫМ ФАКТОРАМ, ВЛИЯЮЩИМ НА УСТОЙЧИВОСТЬ КОМПЛЕКСОВ, НЕ ОТНОСИТСЯ
1) природа центрального и донорного атома
2) хелатный эффект
3) стерический эффект
4) внешние условия (t, природа растворителя, ионная сила, состав раствора)
45. ОСНОВАТЕЛЕМ КООРДИНАЦИОННОЙ ТЕОРИИ КОМПЛЕКСНХ СОЕДИНЕНИЙ ЯВЛЯЕТСЯ
1) Ю.Ю. Лурье
2) В. Оствальд
3) А. Вернер
4) К.Р. Фрезениус
46. СОЕДИНЕНИЯ, ОБРАЗОВАННЫЕ НЕЙТРАЛЬНЫМИ МОЛЕКУЛАМИ, ОБЫЧНО НЕ СОДЕРЖАЩИМИ МЕТАЛЛЫ, НАЗЫВАЮТСЯ
1) комплексными соединениями
2) молекулярными комплексами
3) координационными соединениями
4) активными соединениями
47. КАК НАЗЫВАЕТСЯ КОМПЛЕКСООБРАЗУЮЩАЯ СВЯЗЬ, КОТОРУЮ ЛИГАНД ОБРАЗУЕТ С МЕТАЛЛОМ
1) металлическая
2) координационная
3) ионизированная
4) атомная
48. ПЕРВИЧНАЯ ДИССОЦИАЦИЯ КОМПЛЕКСНОГО СОЕДИНЕНИЯ
1) отщепление лигандов
2) распад внутренней сферы на составляющие ее части
3) отщепление ионов металла
4) отщепление ионов внешней сферы
49. ФУНКЦИЯ ОБРАЗОВАНИЯ КОМПЛЕКСНОГО СОЕДИНЕНИЯ ЭТО
1) константа устойчивости комплекса
2) заряд комплексного иона
3) степень окисления металла комплексообразователя
4) среднее координационное число
50. НАЛИЧИЕ У ОРГАНИЧЕСКИХ РЕАГЕНТОВ ГРУПП, СОДЕРЖАЩИХ Π-ЭЛЕКТРОНЫ, ОБУСЛАВЛИВАЕТ
1) лабильность связывания в комплекс
2) разрушение при нагревании
3) возможную электропроводность
4) существование характерной окраски
51. ГРУППЫ >С=С<, >С=О, >С=N-, >C=C-C=C<, -N=N-, -O-N=O, СОДЕРЖАЩИЕСЯ В ОРГАНИЧЕСКИХ РЕАГЕНТОВ, НАЗЫВАЮТСЯ
1) флуорисцентные
2) хромофоры
3) радикальные
4) гетероатомные
52. ПРИЧИНОЙ СДВИГА ПОЛОС ПОГЛОЩЕНИЯ РЕАГЕНТОВ И КОМПЛЕКСОВ В ТУ ИЛИ ИНУЮ ОБЛАСТЬ СПЕКТРА ЯВЛЯЕТСЯ
1) присутствие ауксохромов
2) воздействие полярного растворителя
3) влияние pH среды
4) возможность перехода электронов на вакантные орбитали
53. ВОЗМОЖНАЯ ГИДРОФОБНОСТЬ МНОГИХ ОРГАНИЧЕСКИХ РЕАГЕНТОВ ОБУСЛОВЛЕНА
1) наличием электронодонорных заместителей
2) малым числом доступным для гидратации функциональных групп
3) присутствием подвижного протона
4) стерическими эффектами крупных агрегатов
54. СЕЛЕКТИВНОСТЬ ОРГАНИЧЕСКИХ РЕАГЕНТОВ ОПРЕДЕЛЯЕТСЯ
1) легкостью полимеризации основной цепи, температурой раствора и устойчивостью образующегося комплекса
2) совпадением спектров поглощения раствора реагента и комплекса
3) природой и числом донорных атомов функционально –
аналитических
4) группировок, размером цикла и стерическими факторами
5) размером и устойчивостью образующегося цикла, легкостью его гидратации
55. СЕРОСОДЕРЖАЩИЕ РЕАГЕНТЫ С МЕТАЛЛАМИ, ИОНЫ КОТОРЫХ ИМЕЮТ ЗАПОЛНЕННЫЕ ИЛИ ЧАСТИЧНО ЗАПОЛНЕННЫЕ d-ОРБИТАЛИ, ОБРАЗУЮТ УСТОЙЧИВЫЕ КОМПЛЕКСЫ С ЧИСЛОМ ЦИКЛОВ РАВНЫМ 1
1) 2
2) 4
3) 5
4) 6
56. РЕАКЦИОННАЯ СПОСОБНОСТЬ ОРГАНИЧЕСКИХ РЕАГЕНТОВ ОПРЕДЕЛЯЕТСЯ ПРЕЖДЕ ВСЕГО
1) наличием функционально-аналитических групп
2) наличием заряда
3) существованием мгновенно-индуцированных диполей
4) присутствием таутомерных форм
57. ГРУППЫ ТИПА –SO3-, -PO3H-, -AsO3H-, -COO-В СТРУКТУРУ ОРГАНИЧЕСКИХ РЕАГЕНТОВ ВВОДЯТ ДЛЯ
1) повышения растворимости в неполярных растворителях
2) для смещения максимума поглощения в ИК-область
3) для повышения термической устойчивости реагента
4) для повышения растворимости в воде
58. С КАКИМИ ОРГАНИЧЕСКИМИ РЕАГЕНТАМИ ПРИ ОБРАЗОВАНИИ КОМПЛЕКСА НАИБОЛЬШЕЕ МЕШАЮЩЕЕ ВЛИЯНИЕ ПРОЯВЛЯЕТСЯ ЗА СЧЁТ СТЕРИЧЕСКОГО ЭФФЕКТА
1) N-донорными
2) хелатообразующими
3) интенсивно окрашенными
4) гетероциклическими
59. В КАЧЕСТВЕ ТИТРАНТА ПРИ КОМПЛЕКСОНОМЕТРИЧЕСКОМ ТИТРОВАНИИ НАИБОЛЕЕ ЧАСТО ИСПОЛЬЗУЮТ
1) нитрилотриуксусную кислоту (НТУ), комплексон I
2) этилендиаминтетрауксусную кислоту (ЭДТУ), комплексон
II
3) транс-1,2-диаминциклогексантетрауксусную кислоту
(ДЦТА), комплексон IV
4) двунатриевую соль этилендиаминтетрауксусной кислоты (ЭДТА), комплексон III
60. ОАР ФЕНОЛФТАЛЕИН ИСПОЛЬЗУЕТСЯ В КАЧЕСТВЕ ИНДИКАТОРА ПРИ
1) окислительно-восстановительном титровании
2) осадительном титровании
3) комплексонометрическом титровании
4) кислотно-основном титровании
61. ОАР, ФОРМУЛА КОТОРОГО
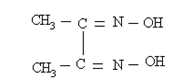
ИСПОЛЬЗУЕТСЯ ДЛЯ ИДЕНТИФИКАЦИИ ИОНОВ
1) Ca2+
2) Al3+
3) Ni2+
4) Fe3+
5) Mg2+
62. 8-ГИДРОКСИХИНОЛИН ИСПОЛЬЗУЕТСЯ В КАЧЕСТВЕ
1) титранта в кислотно-основном титровании
2) осадителя в гравиметрии
3) титранта в комплексонометрии
4) титранта в окислительно-восстановительном титровании
5) металлоиндикатора
63. ОАР, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНДИКАТОРОВ В МЕТОДАХ КИСЛОТНО-ОСНОВНОГО ТИТРОВАНИЯ, ПРЕДСТАВЯЛЯЮТ СОБОЙ
1) органические соединения, способные к реакциям окисления-восстановления
2) органические кислоты или основания, имеющие различающиеся окраски кислой и основной форм
3) органические соединения, образующие окрашенные комплексы при участии ионов водорода
4) органические соединения, образующие окрашенные комплексы с ионами металлов
5) органические соединения, образующие окрашенные комплексы с ионами неметаллов
64. ФОРМУЛА ХЕЛАТА АЛЮМИНИЯ С АЛИЗАРИНОМ 1) (С14O4H7)2Al
2) (С14O4H7)3Al
3) С14O4H7Al 4) (С14O4H7)Al3
65. СООТВЕТСТВИЕ МЕЖДУ ОРГАНИЧЕСКИМ АНАЛИТИЧЕСКИМ РЕАГЕНТОМ И ОПРЕДЕЛЯЕМЫМ С ЕГО ПОМОЩЬЮ ИОНОМ ФОРМУЛА РЕАГЕНТА ОПРЕДЕЛЯЕМЫЕ ИОНЫ
| Формула реагента | Определяемые ионы |
| 1.Fe2+ | |
| 2.Ca2+ | |
| 3.Ni2+ | |
| 4.Al3+ |
66. ОАР ФЕРРОИН ИСПОЛЬЗУЕТСЯ В МЕТОДЕ ОКИСЛИТЕЛЬНО
ВОССТАНОВИТЕЛЬНОГО ТИТРОВАНИЯ В КАЧЕСТВЕ _
1) титранта
2) установочного вещества
3) вторичного стандартного раствора
4) индикатора
67. СООТВЕТСТВИЕ МЕЖДУ НАЗВАНИЯМИ ОАР И МЕТОДАМИ, В КОТОРЫХ ОНИ ПРИМЕНЯЮТСЯ
| Метод химического анализа | Название ОАР |
| 1. Кислотно-основное титрование | 1) 8-гидроксихинолин |
| 2. Комплексонометрия | 2) Фенолфталеин |
| 3. Гравиметрия | 3) Этилендиаминтетрауксусная кислота |
| 4) Метиловый оранжевый | |
| 5) Эриохромовый черный Т | |
| 6) Диметилглиоксим | |
| 7) Ализарин |
68. ФОРМУЛА ХЕЛАТА ЖЕЛЕЗА (III) С АНИОНОМ ЭТИЛЕНДИАМИНТЕТРАУКСУСНОЙ КИСЛОТЫ Y
1) FeY2-
2) FeY-
3) FeY3
4) Fe3Y