Расчет ионной силы растворов электролитов, коэффициента активности и активной концентрации ионов
Теория электролитической диссоциации справедлива лишь для водных растворов слабых электролитов. Сильные электролиты (минеральные кислоты, растворимые основания и соли) не имеют постоянных констант диссоциации при различных концентрациях. Следовательно, в растворах сильных электролитов нет динамического равновесия между ионами и недиссоциированными молекулами, т.е. процесс диссоциации сильных электролитов необратим и растворы их не подчиняются закону действия масс.
Дебай П. и Хюккель Э. в 1923 г. разработали теорию сильных электролитов, в которой они объяснили причину неподчинения процесса диссоциации сильных электролитов закону действующих масс.
Согласно этой теории сильные электролиты диссоциируют на 100°/о, доказано экспериментально. В результате образуется сравнительно большая концентрация ионов, между которыми возникают электростатические взаимодействия. Межионные силы влияют на все свойства электролитов, особенно в концентрированных растворах. Они понижают подвижность ионов и их активность, и ионы в реакциях ведут себя так, будто их концентрация меньше действительной (аналитической) концентрации. С разбавлением растворов влияние ионной атмосферы понижается. В очень разбавленных растворах влиянием межионных сил можно пренебречь, так как эти растворы близки к идеальным.
Для оценки реакционной способности сильных электролитов введены понятия: активная концентрация, коэффициент активности, ионная сила.
Активная концентрация или «активность» (α) – эффективная концентрация ионов в водных растворах с учетом электростатического взаимодействия между ними, равная произведению общей концентрации на коэффициент активности.
α = f ·С,
где α – активная концентрация,
f – коэффициент активности
С – общая концентрация.
«α» и «С» выражаются в моль/дм3 или моль/л.
Коэффициент активности ионов показывает степень отклонения свойств реальных растворов от идеальных. Эта величина зависит от заряда иона, общей концентрации ионов данного электролита и концентрации всех посторонних ионов присутствующих в растворе.
В растворах, близких к идеальным, коэффициент активности по величине приближается к единице, т.е. f → 1 и тогда α → С. Для реальных растворов электролитов, как правило, коэффициент активности f меньше единицы.
Величина коэффициента активности и активность зависят от ионной силы раствора.
Ионная сила раствора (I) – величина, характеризующая электрическое поле и меру электростатического взаимодействия ионов в растворе и определяется зарядом ионов и их концентрацией. Ионная сила вычисляется по формуле предложенной Г. Льюисом и М. Ренделом в 1921г. Данная величина равна полусумме произведения молярных концентраций всех присутствующих ионов на квадраты их зарядов:
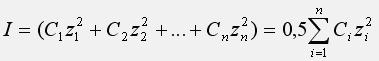
Cj – молярная концентрация какого-либо иона в растворе
Zj – заряд иона
Ионная сила – безразмерная величина. Экспериментально показано, что с увеличением ионной силы раствора коэффициенты активности уменьшаются. Если ионная сила меньше 0,0005, то коэффициенты активности близки к единице и в расчетах свойств растворов не используются.
Коэффициент активности иона в разбавленном растворе можно приближенно вычислить по формуле:

Пример:Вычислить ионную силу 0,005 М раствора нитрата бария.
Решение: Нитрат бария Ва(N03 )2 диссоциирует по уравнению:
Ba(N03)2 Ва2+ + 2N03-
Определяют концентрацию каждого иона: С (Ва2+) = 0,005 моль/дм3, С(NO3)=2 · 0,005 =0,010 моль/дм3
Рассчитывают ионную силу раствора:
I=1/2 (0,005 * 22 +0,01 * 12) = 0,015
