Работа 1. Определение общей жёсткости воды.
Пипеткой Мора вместимостью 25 мл вносят исследуемую пробу воды в колбу для титрования, добавляют 2 мл аммиачной буферной смеси, 3-4 микрошпателя индикатора эриохрома Т в смеси с хлоридом натрия (1:100) и титруют комплексоном (III) (трилоном Б) до изменения винно-красной окраски раствора в фиолетово-синюю. Титрование повторяют три раза и за окончательный результат принимают среднее из трех показателей, по которому рассчитывают общую жёсткость воды в мг-экв/л по формуле:
 , (1)
, (1)
где Ж - жёсткость воды, мг-экв/л
VТ - объём израсходованного раствора трилона Б, мл
СТ - молярная концентрация трилона Б
VВ - объём воды, взятой для анализа.
Работа 2. Определение содержания кальция в воде.
Пипеткой Мора вместимостью 25 мл вносят исследуемую пробу воды в колбу для титрования, добавляют 2.5 мл 2н раствора NaOH, 1 шпатель индикатора мурексида, смешанного с хлоридом натрия и титруют стандартным раствором ЭДТА ( комплексон III) (медленно) до перехода красной окраски в фиолетовую, не исчезающую в течение 3 мин. Титрование повторяют три раза и за окончательный результат принимают среднее из трех показателей, по которому рассчитывают содержание ионов кальция в мг-экв/л по следующей формуле:
 , (2)
, (2)
где CT – молярная концентрация трилона Б;
VT - объём трилона Б
Содержание ионов кальция (г) вычисляют по формуле:
 , (3)
, (3)
ЭCa2+ - эквивалент кальция;
NТ – нормальность трилона Б;
Vк – объем мерной колбы для разведения (если таковое имеется);
VА - объем аликвоты для титрования
Содержание ионов магния (г) вычисляют по формуле:
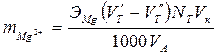 , (4)
, (4)
VB - объём исследуемой воды
Содержание ионов магния мг-экв/л рассчитывают по разности:
[Mg2+] = Ж - [Ca2+]
Занятие 19.
Контрольная работа 3.
Контрольные вопросы.
1 Теория сильных электролитов. Ионная сила растворов электролитов. Активность электролитов и ионов. Коэффициент активности.
2 Теории кислот и оснований (Аррениуса, Льюиса, Бренстеда-Лоури). Константы кислотности и основности.
3 Протолитическое равновесие. Протолитическая теория кислот и оснований.
4 Ионное произведение воды. рН водных растворов. Константа кислотности и основности.
5 Кислотно-основное равновесие в организме.
6 Протолитическое равновесие в водных растворах солей.
7 Расчет рН в растворах гидролизующихся солей. Степень и константа гидролиза.
8 Протолитическое равновесие в буферных растворах. Классификация буферных растворов. Механизм буферного действия.
9 Буферная емкость и её определение.
10 Значение рН в буферных растворах (уравнение Гендерсона-Гассельбаха).
11 Роль буферных систем в организме человека. Использование буферных систем в анализе.
12 Количественный анализ. Классификация методов. Роль и значение количественного анализа.
13 Сущность титриметрического метода анализа. Классификация методов. Требования к реакциям в титриметрических методах анализа.
14 Приготовление и стандартизация растворов. Титранты, рабочие растворы.
15 Способы титрования: прямое, обратное, заместительное. Сущность, примеры.
16 Кислотно-основное титрование. Сущность данного метода. Реакции, используемые в данном методе, требования к ним.
17 Точка эквивалентности в титровании, ее фиксация с помощью индикаторов.
18 Теории кислотно-основных индикаторов, зона и точка перехода окраски индикаторов.
19 Кривые кислотно-основного титрования, их расчет и построение по изменению значений рН.
20 Ациди-алкалиметрия в биологии и медицине.
22. Окислительно-восстановительное титрование. Сущность метода.
23. Классификация редокс-методов.
24. Требования, предъявляемые к реакциям.
25. Виды окислительно-восстановительного титрования (прямое, обратное, заместительное) и расчеты результатов титрования.
26. Перманганатометрическое титрование.Сущность метода. Условия проведения титрования. Титрант, его приготовление, стандартизация. Установление конечной точки титрования.
27. Реакции перманганата в различных средах (рН).
28. Применение перманганатометрии в биологии и медицине
29. Иодометрическое титрование. Сущность метода. Титрант, его приготовление, стандартизация, его приготовление, стандартизация, хранение. Условия проведения титрования, определение конечной точки титрования.
30. Применение иодометрии в биологии и медицине.
31. Сущность осадительного титрования.
32. Требования, предъявляемые к реакциям, лежащим в основе осадительного титрования.
33. Метод Мора. Сущность метода. Основные тиранты метода. Методы приготовления и стандартизации титрантов.
34. Метод Фольгарда. Сущность, индикаторы. Основные титранты метода. Методы приготовления и стандартизации титрантов.
35. Метод Фаянса. Индикаторы осадительного титрования Понятие о комплексиметрическом методе титрования. Сущность, требования к реакциям.
36. Понятие о комплексонатах металов
37. Равновесия в водных растворах ЭДТА. Состав и устойчивость комплексонатов металлов.
38. Индикаторы комплексонометрии (металлохромные индикаторы), принцип их действия;
39. Приготовление титрантов в комплексонометрии. Применение данного метода в биологии и медицине
40. Решение расчётных задач.
