Методика определения растворимости.
Комплект учебно-методических материалов к
Учебно-методическому комплексу
(фармацевтическая химия)
Методические указания к практическому занятию
Для студентов 3 курс, 5 семестр
060108 «фармация»
Тема: Фармакопейный анализ натрия нитрита, висмута нитрата основной.
.
| Тема: | Фармакопейный анализ натрия нитрита, висмута нитрата основной. |
| Время: | 4 часа |
| Учебная цель: |
|
| План занятия: |
|
| Требования к исходному уровню знаний |
|
| Задание для самоподготовки: | Ответ по отдельным препаратам строить по схеме: - Название лекарственного препарата - Химическая формула - Описание - Растворимость - Подлинность - Доброкачественность - Количественное определение - Применение лекарственного препарата |
| Самоподготовка | 1.Какими химическими реакциями устанавливается подлинность натрия нитрита? 2.Каким методом проводится количественное определение натрия нитрита по ГФ X? Какие другие методы можно использовать для этой цели? 3.Какими химическими реакциями установить подленности висмута нитрата основного? |
| Практическая работа. | |
| Объекты исследования: | Натрия нитрит Висмута нитрат основной |
Задание № 1. Описать физические и физико-химические свойства изучаемых лекарственных препаратов.
Свойства лекарственных препаратов контролируют по приведенным в соответствующей статье ГФ X (ФС, ВФС) параметрам: описанию, физическим свойствам, физико-химическим константам.
Методика проведения.Полученные данные оформить в виде таблицы № 1 и сделать заключение о соответствии физических и физико-химических свойств испытуемого препарата соответствующей статьи ГФ X.
Таблица №1
| Препарат (латинское и русское название) | Формула и химическое название | Описание | Цвет | Запах | Вкус | t, оС |
Задание № 2. Установить растворимость изучаемых лекарственных препаратов.
В фармакопее под растворимостью подразумевают свойство вещества растворятся в разных растворителях, принятых Государственной фармакопеей. Показатели растворимости в разных растворителях приведены в частных статьях. Если растворимость является показателем чистоты препарата, то в частной статье есть об этом специальное указание.
Для обозначения растворимости веществ в фармакопее приняты условные термины (в пересчете на 1 г), значения которых приведены в таблице №2.
Таблица №2
| Условный термин | Количество растворителя (мл) необходимое для растворения 1,0 г препарата |
| Очень легко растворим | Не более 1 |
| Легко растворим | От 1 до 10 |
| Растворим | От 10 до 30 |
| Трудно растворим | От 30 до 100 |
| Мало растворим | От 100 до 1000 |
| Очень мало растворим | От 1000 до 10000 |
| Практически не растворим | Более 10000 |
Методика определения растворимости.
Навеску препарата вносят в отмеренное количество растворителя и непрерывно встряхивают в течение 10 мин при 20±2°С. Предварительно
препарат может быть растерт.
Для медленно растворимых препаратов, требующих для своего растворения более 10 мин, допускается также нагревание на водяной бане до 30°С. Наблюдение производят после охлаждения раствора до 20±2°С и энергичного встряхивания в течение 1—2 мин.
Условия растворения медленно растворимых препаратов указываются в частных статьях.
Препарат считают растворившимся, если в растворе при наблюдении в проходящем свете не обнаруживаются частицы вещества. Для препаратов, образующих при растворении мутные растворы, соответствующее указание должно быть приведено в частной статье.
Задание №3. Установление подлинности лекарственных препаратов.
Подлинность органических лекарственных препаратов устанавливают химическими реакциями (осаждения, окисления, конденсации, нитрования, диазотирования и азосочетания, этерификации, галогенирования, комплексообразования и др.), подтверждающими наличие соответствующих функциональных групп.
После проведения испытаний на подлинность лекарственного препарата в протоколе кратко описывают методику выполнения качественных реакций с обязательным приведением уравнений химических реакций. Результаты качественных реакций оформляют в виде табл. 3, сопоставляют их с данными ГФ X и делают заключение о соответствии препарата требованиям ГФ.
Таблица №3.
Ион натрия.
1. Ион натрия.Отмеривают 1 мл 10%-ного раствора натрия сульфата, подкисляют разведенной уксусной кислотой, если необходимо, фильтруют, затем прибавляют 0,5 мл раствора цинк-уранил-ацетата; образуется желтый кристаллический осадок:
NaСl + Zn [(UO2)3 (СН3СОО)8] + СН3СООН + 9Н2О ==
Na [Zn (UO2)3 (СН3СОО)9]*9H2O + НСl
2. Ион натрия.Соль натрия, внесенная в бесцветное пламя, окрашивает его в желтый цвет.
Нитрит-ион.
1. Нитрит-ион.К ~ 0,002 г натрия нитрита прибавляют несколько капель раствора дифениламина; появляется синее окрашивание.
2. Нитрит-ион.К 1 мл 10%-ного раствора натрия нитрита прибавляют 1 мл разведенной серной кислоты. Выделяются желто-бурые пары (отличие от нитратов):
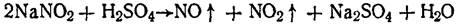
3. Нитрит-ион.Несколько кристаллов антипирина растворяют в фарфоровой чашке в 2 каплях разведенной соляной кислоты, прибавляют 1 каплю 10%-ного раствора натрия нитрита. Появляется зеленое окрашивание (отличие от нитратов):
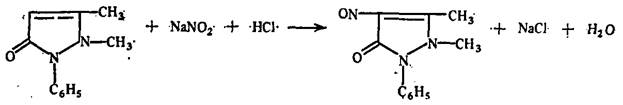
Ион висмута.
1. Препараты висмута (около 0,05 г иона висмута) взбалтывают с 5 мл разведенной серной кислоты и фильтруют. К фильтрату прибавляют 2 капли раствора йодида калия; выпадает черный осадок, растворимый в избытке реактива.
2. Препараты висмута (около 0,05 г иона висмута) взбалтывают с 3 мл разведенной соляной кислоты и прибавляют 1 мл раствора сульфида натрия; появляется коричневато-черное окрашивание
Задание № 4. Выполнить испытания на доброкачественность лекарственных препаратов.
При выполнении испытаний на доброкачественность необходимо соблюдать все указания общей статьи ГФ X (с. 748) или ГФ XI (с. 165) и соответствующей частной статьи на испытуемый лекарственный препарат.
Определение допустимых примесей, указывающих на степень очистки лекарственного препарата, основано на его сравнении с эталонными растворами. Недопустимые примеси, влияющие на фармакологическое действие лекарственного препарата, обнаруживают с помощью качественных реакций на эти примеси.
Методики установления специфических примесей приведены в соответствующих заданиях лабораторной работы. Полученные результаты испытаний оформляют в виде табл. 4 и делают заключение о соответствии доброкачественности испытуемого препарата требованиям ГФ X.
Таблица №4.
| Испытание | Препарат | |
| установлено | требования ГФ X (ГФ XI) | |
Натрия нитрит.
4.1.А. Хлориды. Нагревают 0,2 г препарата с 3 мл воды и 2 мл азотной кислоты до прекращения выделения бурых паров. Раствор, полученный после охлаждения и разбавления водой до 10 мл, должен выдерживать испытание на хлориды (не более 0,01% в препарате).
4.1.Б. Сульфаты. Смешивают 2 г препарата с 2 г хлорида аммония и 10 мл воды и выпаривают на водяной бане досуха, прибавляют 5 мл воды и снова выпаривают. Остаток растворяют в 20 мл воды. Отмеренные 10 мл этого раствора должны выдерживать испытание на сульфаты (не более 0,01% в препарате).
4.1.В. Тяжелые металлы. Тот же раствор (см. 4.3.Б) объемом 10 мл должен выдерживать испытание на тяжелые металлы (не более 0,0005% в препарате).
4.1.Г. Мышьяк. Масса 0,12 г препарата должна выдерживать испытание на мышьяк (не более 0,0004% в препарате)
Висмута нитрат основной.
4.2.А. Кислотность. 5 г препарата смешивают с 75 мл воды, оставляют на 24 часа и затем фильтруют через стеклянный фильтр № 3 или № 4, на который положена небольшим слоем бумажная масса (до 1 см). На титрование 50 мл прозрачного фильтрата должно расходоваться не более 1,5 мл 0,1 н. раствора едкого натра (индикатор — фенолфталеин).
4.2.Б. Хлориды. 0,4 г препарата растворяют в 5 мл азотной кислоты и доводят водой до 10 мл. 1 мл этого раствора, разведенный водой до 10 мл, должен выдерживать испытание на хлориды (не более 0,05% в препарате).
4.2.В. Соли щелочных и щелочноземельных металлов. 0,5 г препарата растворяют в 20 мл разведенной соляной кислоты, разбавляют водой до появления слабой мути и нагревают раствор до кипения. Медленно пропускают сероводород до полного осаждения висмута и фильтруют. Фильтрат выпаривают досуха и остаток осторожно прокаливают до постоянного веса. Остаток не должен превышать 0,5%.
4.2.Г. Карбонаты. 1 г препарата должен растворяться в 3 мл азотной кислоты без выделения пузырьков газа.
4.2.Д. Соли аммония. 1 г препарата кипятят с 5 мл раствора едкого натра; не должен ощущаться запах аммиака.
4.2.Е. Медь. 3 г препарата растворяют при нагревании в 4 мл концентрированной азотной кислоты. Полученный раствор вливают в стакан, содержащий 100 мл воды, выпавший осадок отфильтровывают и промывают разведенной азотной кислотой (2 раза по 5 мл). Фильтрат вместе с промывной жидкостью упаривают до объема 30 мл и вторично фильтруют. К 5 мл этого фильтрата прибавляют небольшой избыток раствора аммиака; жидкость над осадком должна оставаться бесцветной.
4.2.Ж.Свинец. К 5 мл того же фильтрата прибавляют 5 мл разведенной серной кислоты; не должна появляться муть.
4.2.З.Серебро. К 5 мл того же фильтрата прибавляют 10 капель разведен-«ой соляной кислоты; допускается опалесценция, не превышающая опа-лесценцию 5 мл эталонного раствора.
Примечание. Приготовление эталонного раствора. 1 мл 0,1 н.
раствора нитрата серебра разводят водой в мерной колбе до 100 мл. 10 мл полученного раствора разводят водой в мерной колбе до 100 мл. 1 мл полученного раствора доводят водой до 5 мл.
4.2.И. Сульфаты. К 5 мл того же фильтрата прибавляют 0,5 мл раствора нитрата бария; раствор должен быть прозрачным.
Задание №5. Выполнить количественное определение лекарственных препаратов.
В протоколе кратко описывают методику количественного определения одним из химических (нейтрализации, окисления — восстановления, осаждения, комплексонометрии, нитритометрии) или физико-химических (спектрофотометрии, фотоколориметрии, рефрактометрии, потенциометрии, хроматографии) методов.
Обязательно приводят уравнения протекающих при этом химических реакций. При использовании титриметрических методов предварительно рассчитывают эквивалент, титр определяемого вещества и его массу, необходимую для количественного определения.
Содержание лекарственного препарата (% или г) вычисляют по формулам, указанным в задании или в соответствующей статье ГФ X (ФС, ВФС).
