Схема электролитической диссоциации.
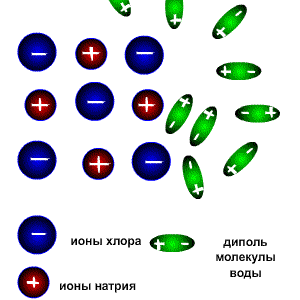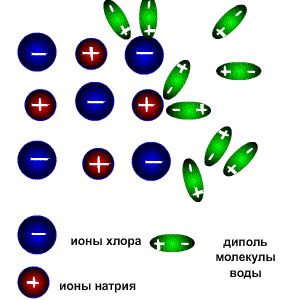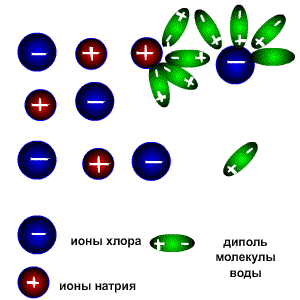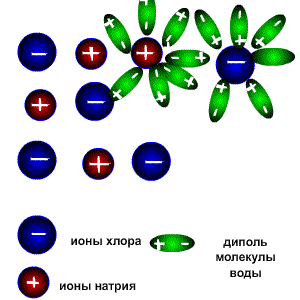
Молекулы воды являются дипольными, т.е. один конец молекулы заряжен отрицательно, другой-положительно. Молекула отрицательным полюсом подходит к иону натрия, положительным-к иону хлора; окружают ионы со всех сторон и вырывают из кристалла, причём, только с его поверхности
Уравнение диссоциации можно записать следующим образом:
NaCl 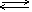 Na+ + Cl- Na+ + Cl- |
Электролитическую диссоциацию вызывает не только вода, но и неводные полярные растворители, такие как Жидкий аммиак и жидкий диоксид серы. Однако именно для воды характерно свойство ослаблять электростатическое притяжение между ионами в решётке выражено особенно ярко.
Свободные ионы, оказавшиеся в водном растворе окружаются полярными молекулами воды: вокруг ионов образуется гидратная оболочка, т.е. протекает процесс гидратации.
Сила электролитов.
Силу электролитов можно охарактеризовать с помощью степени диссоциации.
Степень диссоциации электролита-это частное от деления числа продиссоциированных молекул к общему числу молекул электролита, введённого в раствор.
| α=Nдисс/N |
Степень диссоциации потенциальных электролитов изменяется в пределах 0< α ≤1( значение α=0 относится к неэлектролитам).
Степень диссоциации возрастает при увеличении разбавления раствора, а также при повышении температуры ( повышение температуры приводит к увеличению кинетической энергии растворённых частиц, что способствует распаду молекул на ионы.)
Сила электролитов в водном растворе определяется их степенью диссоциации при постоянной концентрации и температуре. К сильным электролитам относятся относятся вещества степень диссоциации которых близка к 1. К ним относятся хорошо растворимые щёлочи, соли, кислоты.
14.вопрос
Основания. Название «основания» первоначально было отнесено к веществам, которые в реакциях с кислотами образуют соли. К основаниям принадлежат гидроксиды многих металлов.
Водные растворы таких оснований, как NаОН, КОН и Ва(ОН)2, обладают сильнощелочными свойствами, поэтому эти вещества и некоторые другие называютщелочами.
С точки зрения теории электролитической диссоциации основания — это вещества, диссоциирующие в водном растворе с образованием анионов одного вида — гидроксид-ионов ОН-.
В общем виде уравнение электролитической диссоциации основания имеет вид:
NаОН « Na+ + OH-; Ва(ОН)2 « Ba2+ + 2OH-; NH3·H2O « NH4+ + OH-.
Гидроксиды металлов типа NаОН и Ва(ОН)2, представляющие собой ионные кристаллы, являются сильными электролитами, а гидрат аммиака (ковалентное соединение) — это слабое основание.
Некоторые из щелочей аналогично диссоциируют и при плавлении, например КОН.
Большинство же основных гидроксидов разлагаются при нагревании на оксиды и воду еще до плавления.
Основания — гидроксиды металлов — могут быть получены при взаимодействии неблагородных металлов с водой или основных оксидов с водой: 2Nа + 2Н2О = 2 NаОН + Н2, СаО + Н2О = Са(ОН)2.
Оксиды металлов, которые подобным путем образуют основания, раньше называли основными ангидридами.
Типичные свойства оснований по Аррениусу связаны с тем, что они поставляют в водный раствор гидроксид-ионы ОН-. На этом основано обнаружение щелочей с помощью индикаторов. Так, самый распространенный в лаборатории индикатор — лакмус окрашивается растворами щелочей в синий цвет.
Кислоты. Кислоты исторически получили такое название из-за кислого вкуса водных растворов таких веществ, как хлороводород или уксусная кислота.
С точки зрения теории электролитической диссоциации
кислоты — это вещества, диссоциирующие в водном растворе с образованием катионов одного вида — катионов водорода Н+,
В общем виде уравнение электролитической диссоциации кислоты имеет вид:
Н2SО4 = 2Н+ + SО2-
СН3СООН = Н+ + СН3СОО-.
Таким образом, характеристической составной частью всех кислот является водород, способный диссоциировать в водный раствор.
кислота — это водородсодержащее соединение, водород которого может быть замещен на металл с образованием соли: Мg + Н2SO4 = МgSO4 + Н2
Следует различать кислородсодержащие кислоты и бескислородные кислоты.
Все кислоты являются потенциальными электролитами в водном растворе. Под воздействием полярных молекул воды они отщепляют катионы водорода, которые мгновенно гидратируются водой и образуют катионы оксония Н3О+, так как простые катионы водорода Н+, являющиеся по существу индивидуальными протонами р+, не способны к существованию в водном растворе. Среди кислот есть как сильные электролиты (Н2SО4, НМО3, НС1), так и слабые (Н2СO3, Н2S).
Кислородсодержащие кислоты могут быть получены взаимодействием кислотных оксидов с водой: СО2 + Н2О = Н3СО3; SО3 + Н2О = Н2SО4.
Ранее такие оксиды неметаллов называли кислотными ангидридами. Многим неметаллам, ввиду многообразия их степеней окисления, отвечает несколько кислородсодержащих кислот. Для хлора известны: НСlO4 — хлорная кислота, НСlO2 — хлористая кислота, НС1О3 — хлорноватая кислота, НСlO — хлорноватистая кислота.
Металлы, которые проявляют несколько степеней окисления, также могут образовывать кислотные оксиды и кислоты.
Многоосновные кислоты, содержащие в молекулах по два или несколько атомов водорода, способных замещаться на атомы металла, обычно являются слабыми электролитами и диссоциируют ступенчато, причем каждая следующая стадия протекает в значительно меньшей степени, чем предыдущая: Н3PO4 « н+ + н2РО4-
н2ро4-« н+ + нРО42-
нРО42-« н+ + РО43-
Типичные свойства кислот по Аррениусу связаны с тем, что они поставляют в водный раствор катионы водорода Н+(Н3О+). На этом основано обнаружение кислот с помощью индикаторов. Так, самый распространенный в лаборатории индикатор — лакмус окрашивается растворами кислот в красный цвет.
Соли. С точки зрения теории электролитической диссоциации соли — это вещества, которые в водном растворе диссоциируют с образованием катионов основания и анионов кислотного остатка: BaС12 = Ba2+ + 2С1.
