Равновесие двухфазной системы
Рассмотрим переход системы между фазами 1 и 2, например, переход вода–пар в закрытом изолированном сосуде. Найдем химические потенциалы фаз в состоянии равновесия.
Для фазы 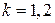 из (2.57)
из (2.57)
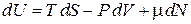
находим
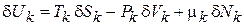 . (2.57а)
. (2.57а)
Для изолированной системы
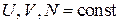 ,
,
тогда вариации
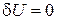 ,
, 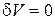 ,
, 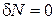 .
.
Для отдельных фаз получаем
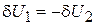 ,
, 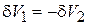 ,
, 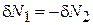 .
.
Величины 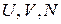 являются аргументами энтропии
являются аргументами энтропии 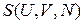 . При переходе системы между фазами аргументы не меняются, тогда в равновесном состоянии энтропия системы минимальна и ее вариация
. При переходе системы между фазами аргументы не меняются, тогда в равновесном состоянии энтропия системы минимальна и ее вариация
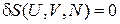 .
.
Из (2.57а) выражаем вариации энтропии подсистем
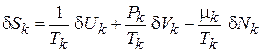 .
.
Энтропия является аддитивной величиной, тогда для равновесной системы
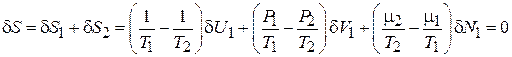 .
.
Величины 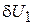 ,
, 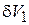 и
и 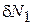 взаимно независимые, это дает условия равновесия
взаимно независимые, это дает условия равновесия
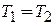 ,
,
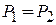 ,
,
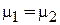 .
.
При наличии внешнего поля
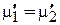 . (2.60)
. (2.60)
Электрохимический потенциал одинаков в разных фазах и в разных местах одной фазы равновесной системы.
Если химические потенциалы в разных фазах отличаются при одинаковых температурах и давлениях
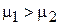 ,
, 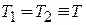 ,
, 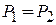 ,
,
то равновесия нет, и идет диффузия. Согласно второму началу термодинамики энтропия увеличивается
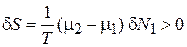 .
.
Следовательно, dN1 < 0 – частицы переходят из фазы 1 в фазу 2. Частицы перемещаются в ту сторону, где химический потенциал меньше, повышая его величину и выравнивая химические потенциалы.
Вычисление химического потенциала
Химический потенциал выразим через свободную энергию 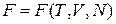 и далее через статистический интеграл Z.
и далее через статистический интеграл Z.
1. Выражаем химический потенциал через свободную энергию, используя формулы (2.31) и (2.57) для свободной и внутренней энергии
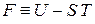 ,
,
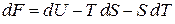 ,
,
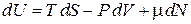 ,
,
получаем
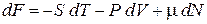 . (2.61)
. (2.61)
Из (2.61) находим
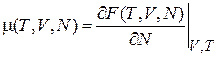 . (2.61а)
. (2.61а)
Химический потенциал равен изменению свободной энергии при добавлении частицы, если система имеет постоянный объем и фиксированную температуру.
2. Выражаем химический потенциал через статистический интеграл, используя (2.19)
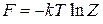 .
.
Из (2.61а) получаем
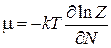 . (2.61б)
. (2.61б)
Статистический интеграл идеального газа из 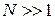 частиц выражаем через статистический интеграл одной частицы
частиц выражаем через статистический интеграл одной частицы
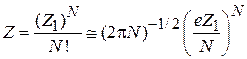 ,
,
где использована формула Стирлинга
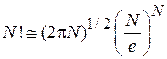 .
.
Вычисляем
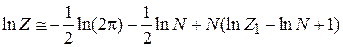 ,
, 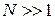 ,
,
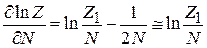 .
.
Из (2.61б) находим химический потенциал многочастичного идеального газа
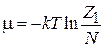 . (2.62)
. (2.62)
3. Для газа с поступательным движением частиц используем (2.22)
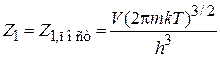 .
.
Из (2.62) получаем
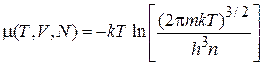 , (2.62а)
, (2.62а)
где 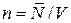 – концентрация частиц. Химический потенциал увеличивается с ростом концентрации газа, с уменьшением температуры и массы частицы. При высокой температуре и низкой концентрации химический потенциал отрицательный, это соответствует условию применимости классической физики. При низкой температуре и высокой концентрации химический потенциал положительный и такая система описывается квантовой физикой.
– концентрация частиц. Химический потенциал увеличивается с ростом концентрации газа, с уменьшением температуры и массы частицы. При высокой температуре и низкой концентрации химический потенциал отрицательный, это соответствует условию применимости классической физики. При низкой температуре и высокой концентрации химический потенциал положительный и такая система описывается квантовой физикой.
Активность
Активность системы
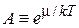
характеризует относительный вклад упорядочивающих и хаотических процессов системы в виде баланса между химическим потенциалом и тепловой энергией. При 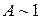 система упорядочена, при
система упорядочена, при 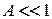 система хаотична.
система хаотична.
Используем (2.62)
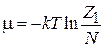 ,
,
находим
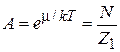 . (2.62б)
. (2.62б)
Для газа с поступательным движением частиц
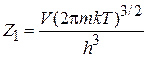 ,
,
получаем
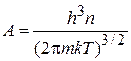 . (2.62в)
. (2.62в)
При повышении температуры и уменьшении концентрации частиц активность упорядочивающих процессов понижается.
Для гелия при нормальных условиях
 ,
, 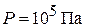
из (2.62а) и (2.62б) получаем
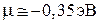 ,
, 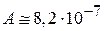 .
.
Классический газ соответствует высоким температурам, низким концентрациям, большим расстояниям между частицами, когда преобладают силы притяжения, поэтому химический потенциал отрицательный и активность мала
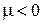 ,
, 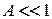 .
.
