Определение диаграммы состояния
Сплавы называют однородными (гомогенными), если структура их однофазная, и разнородными (гетерогенными), если структура их состоит из нескольких фаз. Для сплавов, образованных одними и теми же компонентами, фазовое состояние описывается диаграммой состояния.
Диаграмма состояния - графическое изображение состояния любого сплава изучаемой системы в зависимости от его концентрации и температуры. Диаграмма состояния показывает равновесные, устойчивые состояния, то есть такие, которые обладают минимальной свободной энергией. Изучение любого сплава прежде всего начинается, с построения и анализа диаграммы состояния, так как именно она дает возможность изучать фазы и структурные составляющие сплава.
Пользуясь диаграммой состояния, можно установить возможность проведения термической обработки и ее режимы, температуры литья, горячей пластической деформации и т. д.
Правило фаз
Правило фаз устанавливает температурные условия процесса кристаллизации при заданном давлении, а также определяет, сколько фаз должно быть в чистом компоненте или в сплаве определенного состава, если они находятся в равновесном состоянии при данной температуре (или давлении). Число факторов, которые можно менять, не изменяя фазового состава сплава, называется степенью свободы.
Правило фаз выражает зависимость между числом степеней свободы С (вариантностью) системы, числом компонентов К и числом фаз Ф системы, находящихся в равновесии (рис. 3)
Обычно все превращения в металлах и сплавах происходят при постоянном давлении (атмосферном). Тогда правило фаз записывается так:
С = К - Ф + 1.
Уравнение правила фаз позволяет корректировать правильность построения диаграмм состояния.
Построение диаграмм состояния осуществляют экспериментальными методами. Наиболее часто пользуются методом термического анализа. Сущность этого метода заключается в следующем. Отбирают несколько сплавов данной системы с различным отношением масс входящих в них компонентов. Сплавы помещают в огнеупорные тигли и нагревают в печи. После расплавления сплавов тигли с ними медленно охлаждают и фиксируют скорость охлаждения. По полученным данным строят термические кривые в координатах «время - температура» (рис. 3).
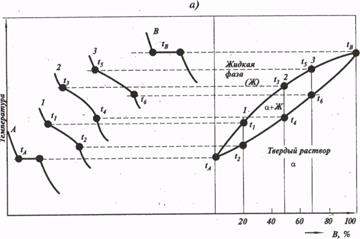
Рис. 3 Методы построения диаграмм состояния
В результате измерений получают серию кривых охлаждения, на которых при температурах фазовых превращений наблюдаются точки перегиба и температурные остановки.
Температуры, соответствующие фазовым превращениям, называются критическими точками.
Точки, отвечающие началу кристаллизации, называют точками ликвидуса, а конца кристаллизации - точками солидуса. По полученным кривым охлаждения (критическим точкам) для различных сплавов изучаемой системы строят диаграмму состояния в координатах; ось абсцисс - концентрация компонентов, ось ординат - температура.
Вид диаграммы состояния определяется характером взаимодействий, которые возникают между компонентами в жидком и твердом состояниях. Во всех случаях предполагают, что в жидком состоянии существует неограниченная растворимость, то есть однородная фаза существует при любом соотношении компонентов.
Диаграммы с ограниченной растворимостью или с полным отсутствием растворимости в жидком состоянии практического значения не имеют, так как сплавы этих систем мало применяются в технике.
ПРИЛОЖЕНИЕ 3
