Периодический закон и периодическая система элементов (псэ) д.и. менделеева
Периодически повторяющиеся свойства простых веществ объясняются периодической повторяемостью электронных конфигураций атомов соответствующих элементов, например:
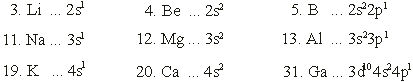
| Периодический закон был сформулирован в 1869 г. Д. И. Менделеевым: Свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов. | |
| Современная формулировка периодического закона гласит: Свойства элементов и их соединений находятся в периодической зависимости от величины заряда ядер их атома. |
Периодическая система химических элементов – это графическое выражение периодического закона. Короткопериодный вариант. По горизонтали имеется 7 периодов, из них I, II и III называются малыми, а IV, V, VI, VII – большими, каждый большой период состоит из двух рядов: четного и нечетного. Периоды, кроме первого, начинаются щелочным металлом и заканчиваются инертным газом. Элементы II и III периодов называются типическими. Свойства элементов закономерно изменяются от типического металла до инертного элемента. Однако, в больших периодах изменение свойств происходит медленно, так как в четных рядах больших периодов находятся одни металлы. У элементов нечетных рядов больших периодов свойства изменяются как у типических: металлические – неметаллические – инертные элементы. По вертикали в периодической системе расположены 8 групп. Каждая группа делится на две подгруппы – главную (элементы малых и больших периодов) и побочную (элементы только больших периодов); в восьмой группе имеются одна главная (инертные элементы) и три побочных, в остальных группах – по одной главной и побочной подгруппе. В главных подгруппах металлические свойства сверху вниз возрастают, а неметаллические – убывают.
Усиление того или иного свойства связано с изменением радиуса атома, так как эта величина определяет энергию взаимодействия электронов с ядром. При химическом взаимодействии более удаленные электроны участвуют в образовании связи с другими атомами. Число валентных электронов равно номеру группы для короткопериодного варианта таблицы (для s и p-элементов – это электроны наружного уровня, для d- элементов – электроны предпоследнего подуровня и наружного уровня). Эти электроны называются валентными.
Частицы, образующиеся в результате потери или присоединения электронов, называются ионами. Положительно заряженные ионы называются катионами, отрицательно- анионами. Как потеря, так и присоединение электронов сопровождаются энергетическим эффектом.
Энергия ионизации (J) – энергия, которую необходимо затратить для отрыва электрона от атома, превращая его в положительный ион (выражается в электрон-вольтах). Это мера способности элемента проявлять металлические свойства.
Сродство к электрону(E)– энергия, выделяющаяся при присоединении электрона к атому, превращая его в отрицательный ион (выражается в электрон-вольтах). Это мера способности элемента проявлять неметаллические свойства.
Электроотрицательность (Э.О.) – способность атома данного элемента к оттягиванию на себя электронной плотности по сравнению с другими элементами соединения. Может быть выражена как арифметическая полусумма величин энергии ионизации и сродства к электрону, выражается в относительных единицах. Чем больше электроотрицательность, тем сильнее неметаллические свойства.
В группах для s и p-элементов сверху вниз увеличивается число энергетических уровней; увеличивается радиус атома и уменьшается энергия ионизации, т. е. усиливаются металлические свойства. У неметаллов в группе сверху вниз увеличивается радиус атома, уменьшается сродство к электрону, т. е. уменьшаются неметаллические свойства.
В периоде с увеличением заряда атомного ядра электроны сильнее к нему притягиваются, происходит сжатие электронных уровней, радиус атома уменьшается, это приводит к увеличению энергии ионизации, сродства к электрону, возрастает электроотрицательность, т. е. металлические свойства ослабевают, а неметаллические усиливаются.
У d- элементов с увеличением заряда ядра радиусы атомов изменяются незначительно: это объясняется тем, что у них постепенно увеличивается число электронов на подуровнях, близко расположенных к ядру атома. Поэтому у переходных элементов не наблюдается резкого изменения свойств, и все они металлы.
Свойства оксидов и гидроксидов зависят от степени окисления соответствующих элементов. Если данный элемент проявляет переменную степень окисления и образует несколько оксидов и гидроксидов, то с увеличением степени окисления свойства последних меняются от основных через амфотерные к кислотным.
Изменение химического характера оксидов и гидроксидов марганца

В группах для s - и р -элементов сверху вниз основные свойства гидроксидов усиливаются, а кислотные – уменьшаются. Так, основание Ва(ОН)2 более сильное, чем Sr(OH)2, а кислота H2SO3, более сильная, чем H2SeO3.
| С возрастанием радиуса иона элемента (при неизменном его заряде) усиливаются основные свойства и ослабляются кислотные свойства образуемого этим элементом гидроксида. |

3. ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
По составу все вещества делятся на простые и сложные.
Простые вещества состоят из одного вида атомов. Каждый отдельный вид атомов называется химическим элементом. Например, простое вещество уголь образовано атомами элемента углерода С, простое вещество хлор – двухатомными молекулами хлора Сl2. К простым веществам относятся металлы и неметаллы. К металлам относятся все s- (кроме Н, Не), d-, f- элементы и некоторые р-элементы: Al, Ga, Ge, Sn, Pb, Sb, Bi, Po.
Неметаллы (в основном это р-элементы) в периодической системе расположены только в главных подгруппах и в конце малых и больших периодов.
Сложные вещества (или химические соединения) состоят из атомов разных элементов: серная кислота H2SO4 образована атомами элементов водорода, серы и кислорода, и т.д.
Классификация неорганических веществ

Согласно этой классификации, важнейшими классами неорганических соединений являются оксиды, гидроксиды и соли.
| Оксидами называются соединения элементов с кислородом, в которых кислород проявляет степень окисления –2. |
Степень окисления элементов определяется как число электронов, смещенных от атома данного элемента к другим атомам (положительная степень окисления) или от других атомов к атому данного элемента (отрицательная степень окисления). Алгебраическая сумма степеней окисления всех атомов, входящих в молекулу, равна нулю.
Номенклатура оксидов. В названиях оксидов в начале пишут слово «оксид», затем название элемента: Na2O – оксид натрия, СаО – оксид кальция, Аl2О3 – оксид алюминия. Если элемент находится в различных состояниях окисления, то в конце названия оксида в скобках римскими цифрами указывается его степень окисления, например, NO – оксид азота (II), N2O3 – оксид азота (III).
По химическим свойствам оксиды подразделяются на солеобразующие и несолеобразующие, или безразличные. Безразличные оксиды (СО, NO, N2O3) не образуют ни кислот, ни оснований, ни солей. Солеобразующие оксиды делятся на основные, кислотные и амфотерные.
Основными оксидами называются оксиды типичных металлов в низших степенях окисления (+1, +2), гидратные соединения которых относятся к классу оснований (основных гидроксидов):
 ;
; 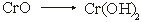 .
.
Отличительное свойство всех основных оксидов – способность реагировать только с соединениями кислотного характера (кислоты, кислотные оксиды) с образованием солей
Кислотными оксидами называются оксиды неметаллов и большинства переходных металлов в высших степенях окисления (+5, +6, +7), гидратные соединения которых относятся к кислотам (кислотным гидроксидам):
 ;
; 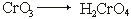 .
.
Отличительное свойство всех кислотных оксидов – способность реагировать только с соединениями основного характера (основания, основные оксиды) с образованием солей
Амфотерные (двойственные) оксиды – оксиды, которые в зависимости от условий реакции проявляют свойства как основных, так и кислотных оксидов. Им отвечают гидратные соединения, проявляющие кислотные и основные свойства.
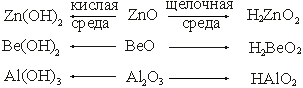
К амфотерным оксидам относятся также: SnO, SnO2, PbO, PbO2, Сr2O3. Амфотерные оксиды образуют соли с основными оксидами и основаниями, с кислотами и кислотными оксидами . Амфотерные оксиды с водой не реагируют.
Гидроксиды. Большинство оксидов при непосредственном взаимодействии с водой или косвенным путем образуют соединения, которые называются гидроксидами, состав которых выражается общей формулой ЭОН. В зависимости от химической природы элемента гидроксиды делятся на основания, кислоты, амфолиты (амфотерные гидроксиды).
Принадлежность гидроксида к определенному классу обусловливается его диссоциацией, которая может протекать по двум направлениям:
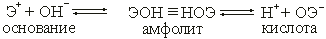
Если прочность химической связи Н—О больше, чем Э—О, то диссоциация происходит по основному типу. Если прочность химической связи О—Э выше, чем Н—О, то диссоциация происходит по кислотному типу. В случае равноценной прочности связи Э—О и Н—О возможна одновременная диссоциация по обеим связям (амфолит).
Направление диссоциации, определяющее основной или кислотный характер гидроксида, зависит от положения элемента в периодической системе.
| Основания – это соединения, при диссоциации которых в качестве анионов образуются только гидроксид-ионы ОН–. |
Например: KOH = K+ + OH– ;
Ba(OH)2 = Ba2+ + 2OH–;
NH4OH  NH4+ + OH–.
NH4+ + OH–.
Число гидроксильных групп определяет кислотность основания, т.е. способность данного основания нейтрализовать кислоты: NaOH, КОН – однокислотные основания, Са(ОН)2 – двухкислотное основание и т.д. Реакции протекают по уравнениям:
NaOH + HCl = NaCl + Н2О;
Са(ОН)2 + 2НСl = СаСl2 + 2Н2О.
По способности диссоциировать основания делятся на сильные (КОН, Ва(ОН)2) и слабые (NH4OH, Ni(OH)2) Сильные основания диссоциируют в одну стадию практически необратимо:
КОН = К+ + ОН–;
Ва(ОН)2 = Ва2+ + 2ОН–.
Слабые основания диссоциируют обратимо:
 .
.
Гидроксиды щелочных (Li, Na, К, Rb, Cs, Fr), щелочноземельных (Ca, Sr, Ba, Ra) металлов и таллия (I) растворимы в воде и называются щелочами. Водные растворы щелочей мылки на ощупь, разъедают кожу, ткани и т.д. Поэтому их называют едкими щелочами. Растворы оснований имеют рН > 7, изменяют окраску индикаторов: лакмус окрашивается в синий цвет, метилоранж – в желтый, фенолфталеин – в малиновый.
Номенклатура оснований. Согласно международной номенклатуре, название оснований составляется из слова «гидроксид» и названия металла: NaOH – гидроксид натрия (едкий натр),KOH− гидроксид калия (едкое кали), Са(ОН)2 – гидроксид кальция (гашеная известь). Если элемент образует несколько оснований, то в названии указывается его степень окисления римской цифрой в скобках: Fe(OH)2 – гидроксид железа (II), Fe(OH)3 – гидроксид железа (III).
| Кислоты – это соединения, при диссоциации которых в качестве катионов образуются только катионы водорода Н+. |
Числом ионов водорода, образующихся при диссоциации кислоты, определяется заряд кислотного остатка: НСl, HNO3 образуют только однозарядные кислотные остатки (Сl–, NO–3); H3PO4 образует три кислотных остатка; однозарядный дигидрофосфат-ион Н2РO4– , двухзарядный гидрофосфат-ион НРО42– и трехзарядный фосфат-ион РО43−; H2SO4 образует два кислотных остатка; HSO4– – гидросульфат-ион, –SO42- сульфат-ион и т.д.
Число ионов водорода, способных замещаться атомами металла и другим основным остатком, определяет основность кислоты. Таким образом, HNO2 – азотистая кислота – одноосновная, H2SO4 – серная кислота – двухосновная, Н3РО4 – фосфорная кислота – трехосновная.
Сильные кислоты диссоциируют в водных растворах практически нацело.
HNO3 = Н+ + NO3- ;
H2SО4 = 2Н+ + SО42-
К сильным кислотам относятся: HNO3, H2SО4, HCl, HBr, HI, HClO4 и др. К слабым кислотам относится большинство органических кислот, а также HNO2, H2S, H2CO3, HCN и др.
Слабые кислоты диссоциируют обратимо:
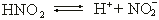 ;
;
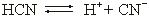 .
.
Слабые многоосновные кислоты диссоциируют обратимо ступенчато:
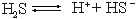 – I ступень;
– I ступень;
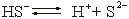 – II ступень.
– II ступень.
Сила кислоты определяется тем, насколько легко она отщепляет ион водорода (протон), и количественно определяется константой равновесия реакции:
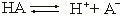 ;
;
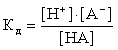 .
.
Кд константой диссоциации данной кислоты.
По наличию кислорода в своем составе кислоты делятся на кислородосодержащие (Н3ВО3, Н3РО4, H2SO4, HNO3) и бескислородные (НСl, HI, H2S, HCN).
Номенклатура кислот. Название кислот производят от названия элемента, образующего кислоту. В случае бескислородных кислот к названию элемента добавляют «о» и слово «водород»: HF – фтороводородная кислота, H2S – сероводородная кислота, HI – иодоводородная кислота и т.д.
Название кислородосодержащих кислот зависит от степени окисления кислотообразующего элемента. Максимальной степени окисления элемента соответствует суффикс «-н(ая)» или «-ов(ая)», например 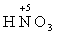 – азотная кислота,
– азотная кислота,  – мышьяковая кислота. Низшей степени окисления элемента соответствует суффикс «-ист(ая)» или «-овист(ая)»:
– мышьяковая кислота. Низшей степени окисления элемента соответствует суффикс «-ист(ая)» или «-овист(ая)»:  – азотистая кислота,
– азотистая кислота, 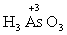 – мышьяковистая кислота.
– мышьяковистая кислота.
Если элемент, находясь в одной и той же степени окисления, образует несколько кислот, содержащих по одному атому данного элемента в молекуле, то название кислоты, содержащей наименьшее число атомов кислорода, снабжается приставкой «мета-», а название кислоты с наибольшим числом атомов кислорода – приставкой «орто-»: НРО3 – метафосфорная кислота, Н3РО4 – ортофосфорная кислота.
| Амфолиты (амфотерные гидроксиды). Гидроксиды, проявляющие кислотно-основную двойственность, называются амфотерными. |
Они способны вступать во взаимодействие и образовывать соли не только с кислотами и кислотными оксидами, но и с основаниями и основными оксидами. К таким гидроксидам относятся гидроксиды цинка, бериллия, свинца, олова, алюминия, хрома, галлия и др. Амфотерные гидроксиды способны диссоциировать как по типу кислот (с образованием ионов водорода), так и по типу оснований (с образованием гидроксид-ионов):
 ;
;

Ввиду двойственного характера амфотерные гидроксиды имеют и два названия: Zn(OH)2 – гидроксид цинка, H2ZnO2 – цинковая кислота, Аl(ОН)3 – гидроксид алюминия, H3AlO3 – ортоалюминиевая кислота, НАlО2 – метаалюминиевая кислота. Амфотерность проявляется в образовании двух рядов солей.
При взаимодействии с кислотами и кислотными оксидами амфотерные оксиды проявляют основные свойства, образуя соль катионного типа
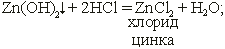
При взаимодействии с основаниями и основными оксидами амфотерные гидроксиды проявляют кислотные свойства, образуя соль анионного типа

В настоящее время взаимодействие амфотерных гидроксидов со щелочами рассматривается не как процесс замещения атомов водорода металлом, а как присоединение к молекуле амфолита ионов ОН– с образованием гидроксокомплексов.

| Соли.Соли можно рассматривать как продукт полного или частичного замещения атомов водорода в молекуле кислоты атомами металла или как продукты полного или частичного замещения гидроксильных групп в молекуле основания кислотными остатками. Все растворимые соли являются сильными электролитами. С позиций теории электролитической диссоциации, при растворении в воде они диссоциируют, отщепляя положительные ионы (основные остатки) и отрицательные ионы (кислотные остатки). Поэтому можно дать такое определение: Химическое соединение, состоящее из основного и кислотного остатков, называется солью. |
Классификация солей
Средние соли. Средние соли являются продуктами полного замещения водорода кислоты металлом или гидроксильных групп основания кислотным остатком:
H2SO4 + Zn = ZnSO4 + H2;
Ca(OH)2 + 2HCl = CaCl2 + 2H2O.
Средние соли диссоциируют как сильные электролиты на катион металла (либо заменяющий его катион аммония) и анион кислотного остатка:
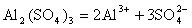 .
.
По международной номенклатуре название соли отражает название металла и латинское название кислотного остатка. Латинское название кислотного остатка происходит от латинского названия элемента, образующего кислоту.
Название соли бескислородной кислоты имеет суффикс «-ид» (NaCl – хлорид натрия, K2S – сульфид калия). Название соли кислородной кислоты зависит от степени окисления кислотообразующего элемента: суффикс «-ат» используют в случае максимальной степени окисления, «-ит» – в случае низкой степени окисления (Li2SO4 – сульфат лития, Li2SO3 – сульфит лития). Для солей, образованных металлами с переменной степенью окисления, последняя указывается в скобках, как в оксидах и в гидроксидах: FeSO4 – сульфат железа (II), Fe2(SO4)3 – сульфат железа (III).
Гидросоли (кислые). При неполном замещении иона водорода на металл в многоосновных кислотах (обычно слабых) образуются кислые соли.
Кислые соли получают при взаимодействии кислот с основаниями, когда количество взятого основания недостаточно для образования средней соли, например:
NaOH +H3PO4 = NaH2PO4 + H2O;
2NaOH + H3PO4 = Na2HPO4 + 2H2O.
Название кислых солей образуется так же, как и средних, но при этом добавляют приставку «гидро-», указывающую на наличие незамещенных атомов водорода, число которых обозначают греческими числительными (ди-, три-, тетра- и т.д.). Например: Na2HPO4 – гидрофосфат натрия, NaH2PO4 – дигидрофосфат натрия.
Большинство кислых солей хорошо растворимо в воде.
Гидроксосоли (основные соли). При частичном замещении гидроксид-ионов в многокислотных основаниях образуются основные соли (гидроксосоли).
Основные соли образуются в тех случаях, когда взятого количества кислоты недостаточно для образования средней соли, например:
Fe(OH)3 + HCl = Fe(OH)2Cl + H2O;
Fe(OH)3 + 2HCl = FeOHCl2 + 2H2O.
Название основных солей тоже образуется подобно названиям средних солей, но при этом добавляют приставку «гидроксо-», указывающую на наличие незамещенных гидроксогрупп, например: Fe(OH)2Cl – дигидроксохлорид железа, FeOHCl2 – гидроксохлорид железа.
Двойные соли состоят из катионов двух разных металлов и кислотного остатка, например, AlK(SO4)2, (NH4)2Fe(SO4)2, СаNН4РО4 и т.д. Такие соли диссоциируют сразу на те ионы, которые входят в их состав:  .
.
Комплексные соли. В комплексном соединении различают внутреннюю (или координационную ) и внешнюю сферу. Более прочно связанные частицы внутренней сферы образуют комплексный ион (в формулах он заключен в квадратные скобки), который и отщепляется при первичной диссоциации, протекающей по типу сильных электролитов.
Например: K4[Fe(CN)6] = 4K+ + [Fe(CN)6]4–.
Внутренняя сфера состоит из центральной частицы - комплексообразователя (чаще всего d-элемента) и непосредственно связанных (координированных) лигандов (ионы противоположного знака или молекулы). Так, в приведенном выше примере комплексообразователем является ион железа, а лигандами- ионы CN- (кислтный остаток слабой синильной кислоты). Число мест во внутренней сфере комплекса, которые могут быть заняты лигандами, называется координационным числом (к.ч.). Координационное число - справочная величина.
ХИМИЧЕСКАЯ СВЯЗЬ
Химическая связь возникает лишь в том случае, если полная энергия взаимодействующих атомов уменьшается, следовательно, при образовании химической связи всегда выделяется энергия.
Различают четыре основных вида химической связи:
1) ковалентную;
2) ионную;
3) металлическую;
4) водородную.
| Ковалентная связь. Химическая связь между атомами, осуществляемая обобществленными электронами, называется ковалентной связью. |
Ковалентная связь существует между атомами как в молекулах, так и в кристаллах. Она возникает как между одинаковыми атомами (например, в молекулах водорода, хлора, в кристалле алмаза), так и между разными атомами (например, в молекулах Н2О и NH3, в кристаллах SiC). Почти все связи в молекулах органических соединений являются ковалентными (С—С, С—Н, С—Г и др.).
Характерными особенностями ковалентной связи являются ее:
1) насыщаемость,
2) направленность,
3) полярность.
Насыщаемость ковалентных связей. Насыщаемость ковалентных связей обусловлена тем, что при химическом взаимодействии участвуют только валентные электроны, т. е. ограниченное число электронов.
| Способность атома к образованию химических связей называют валентностью элемента. |
Согласно методу валентных связей (ВС), валентность элементов определяется числом содержащихся в атоме неспаренных электронов.
Для s- и р-элементов это электроны внешнего уровня, для d-элементов – внешнего и предвнешнего уровней.
Направленность ковалентной связи. Наиболее прочные химические связи возникают в направлении максимального перекрывании атомных орбиталей. Поскольку атомные орбитали имеют определенную форму, то их максимальное перекрывание возможно при определенной пространственной ориентации. Поэтому ковалентная связь характеризуется направленностью.
σ-, π-, δ-cвязи. В зависимости от направления перекрывания атомных орбиталей различают σ-, π-, δ-cвязи.
σ-Связь возникает при перекрывании атомных орбиталей вдоль оси, соединяющей ядра взаимодействующих атомов. σ-Связь может возникнуть при перекрывании двух s-орбиталей, s- и р-орбиталей, двух р-орбиталей, двух d-орбиталей, р- и d-орбиталей. σ-Связь возникает, если атомные р- и d-орбитали ориентированы вдоль оси связи.
π-Связь осуществляется при перекрывании атомных орбиталей по обе стороны оси, соединяющей ядра атомов. При взаимодействии двух р-орбиталей, расположенных перпендикулярно оси, соединяющей ядра атомов, возникают две области перекрывания, расположенные по обе стороны оси, соединяющей ядра атомов. Связь также может образовываться при перекрывании двух d-орбиталей.
π- и δ-Связи налагаются на σ-связи, вследствие чего образуются двойные и тройные связи. Например, между атомами углерода в молекуле этилена образуется одна π- и одна σ-связь. Соответственно, связь между атомами углерода является двойной: 
Двойные связи также возникают при образовании молекул СO2, некоторых кислот и т. п.: 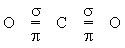
| Количество связей, образующихся между атомами, называется кратностью (порядком) связи. |
Энергия π-связи меньше, чем энергия σ-связей; π-связь менее прочная, чем σ-связь, и разрушается при химических взаимодействиях в первую очередь.
Полярность связи.В гомоядерных двухатомных молекулах одна или несколько пар электронов в равной мере принадлежат обоим атомам (Н:Н). При образовании молекул Н2, Сl2, F2, O2 и т. п. каждое ядро атома с одинаковой силой притягивает пару связывающих электронов. Такая связь называется неполярной связью.
Если взаимодействующие атомы характеризуются различной электроотрицательностью, то обобществленная пара электронов смещается к ядру более электроотрицательного атома. Например, электроотрицательность фтора (4,0) больше электроотрицательности водорода (2,1), поэтому обобществленная электронная пара в молекуле HF смещена в сторону фтора.
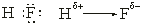
| Если пара электронов, образующих химическую связь, смещена к одному из ядер атомов, то связь называется полярной ковалентной связью. |
Вследствие смещения пары электронов от одного ядра к другому средняя плотность отрицательного заряда у одного из атомов будет выше, чем у другого. Поэтому один из атомов приобретает избыточный отрицательный заряд δ–, другой – избыточный положительный заряд δ+. Эти заряды называют эффективными зарядами атомов в молекуле. В результате образуется диполь (система из двух равных по величине, но противоположных по знаку зарядов  ). Количественной мерой полярности химической связи является электрический момент диполя связи Рсв.
). Количественной мерой полярности химической связи является электрический момент диполя связи Рсв.
Электрическим моментом диполя связи называется произведение эффективного заряда d на расстояние между центрами тяжести положительных и отрицательных зарядов l : 
