Мырышты гексацианоферрат(ІІ) калийдің ерітіндісімен титрлеу.
Мырыш иондары (Zn2+) бейтарап, не қышқылды ортада K4[Fe(CN)6] мен нашар еритін қостұз түзеді:
2K4[Fe(CN)6] + 3 ZnSO4→ K2Zn3[Fe(CN)6]2↓ +3К2SO4
Эквиваленті нүктені екі жолмен анықтауға болады:
1) сыртқы индикатор пайдалану. Сыртқы индикаторлар ретінде аммоний молибдаты, темір(ІІІ) хлориді, уранил ацетаты не нитраты қолданылады. Эквиваленті нүктені анықтау үшін ақ пластинкаға индикатордың, мысалы 1% уранил нитратының, бір тамшысын тамызады. Титрлеу аяғына жақындағанда титрлеп жатқан ерітіндінің бір тамшысын алып индикатордың үстіне тамызады. 30 секундтан кейін қоспаның түсі қараяды. Егер тамшы қызыл қоңыр түске боялса, бұл титрлеу эквивалентті нүктеге жеткенін көрсетеді. Сыртқы индикаторды пайдалану химиктен үлкен тәжірибені талап етеді.
2) Ішкі индикатор пайдалану. Ішкі индикатор ретінде дифениламин мен гексацианоферат(ІІІ) калийдің қоспасын алуға болады. Дифениламин – тотығу – тотықсыздану индикаторы. Ерітіндінің потенциалы +0,76В-тан (қалыпты сутегі электордымен салыстырғанда ) көп болса, түссіз дифениламин көк түсті дифенилбензидинге дейін тотығады. Потенциал +0,76В – тан кіші болса, керісінше, индикатордың көк түсі тотықсыздану нәтижесінде жойылады.
K4[Fe(CN)6] ерітіндісін мырыш тұзының ертіндісімен титрлеуді қарастырайық. [Fe(CN)6]3- және [Fe(CN)6]4- иондары бар ертіндінің тотығу – тотықсыздану потенциалы былай анықталады: 
E = E0 +0.058lg 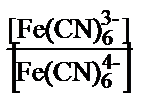 (12.2)
(12.2)
Fe(CN)6]3- пен Fe(CN)6]4- иондарының қоспасы бар қышқыл ерітіндінің потенциалы дифениламинді тотықтыру потенциалынан әлдеқайда кем. Егер осы ертіндіге мырыш тұзын қоса, онда [Fe(CN)6]-4 иондары К2Zn3[Fe(CN)6]2 түрінде тұнбаға түсе бастайды. Тұнба түзілу нәтижесінде [Fe(CN)6]-4 иондарының концентрациясы азайып, (12.2) теңдік бойынша ерітіндінің тотығу - тотықсыздану потенциалы артады. [Fe(CN)6]-4 иондары түгел тұнбаға түсіп болғаннан кейін әрмен қарай құйылған мырыш иондарының аз мөлшерінен тотыққан индикатордың көк түсі пайда болады.
Бұл титрлеуді кері жолмен де жүргізуге болады. Мырыш тұзының қышқыл ерітіндісіне аз мөлшерде дифениламин мен К3[Fe(CN)6] қоспасын құйғанда ерітінді көк түске боялады. Ерітіндінің көк түсі К4[Fe(CN)6] – мен титрлегенде мырыш түгел K2Zn3[Fe(CN)6]2 тұнбасына айналғанша сақталады. К4[Fe(CN)6] – нің алғашқы артық тамшысы индикатордың көк түрін түссіз түріне дейін тотықсыздандырады, яғни эквивалентті нүктеге жеткенде көк ертінді түссізденеді.
Титрлеу жолы. 25,0мл мырыш сульфатының ертіндісіне 25,0мл – ден 75 мл – ге дейін су, 2г (NH4)2SO4, 10 мл- ден 30 мл-ге дейін 6М(1/2H2SO4), 2-3 тамшы дифениламин қосады. Ерітінді көк түске боялғанша күтеді. Содан кейін концентрациясы белгілі К4[Fe(CN)6] ерітіндісімен көк түсті ерітіндіні түссізденгенше титрлейді, эквивалентті нүктеге жақындағанда титрлеуді баяулатады.
К4[Fe(CN)6] ерітіндісінің титрін мырыш (II) ерітіндісі арқылы анықтайды. Ол үшін дәл өлшенген таза мырыш өлшем колбасында сұйытылғын күкірт қышқылымен ерітіледі. Ерітіндінің дәл концентрациясын өлшеп алынған мырыштың нақты мөлшері бойынша анықтайды.
Осы анықтауда мырыштың fэкв =1/2, [Fe(CN)6]-4 үшін fэкв =1/3 – ге тең, себебі мырыштың бір ионы екі калий ионын алмастырады, ал [Fe(CN)6]-4 бір ионына мырышпен алмасу реакциясында үш калий ионы сәйкес келеді.
