Комплексометрический (объемный) метод
Сущность метода заключается в осаждении сульфат-ионов определенным количеством титрованного раствора хлорида бария, избыток которого затем оттитровывается в присутствии ионов магния и индикатора хромогена черного раствором трилона Б.
Метод дает точные результаты, если концентрация ионов SO42- в объеме фильтрата, взятого для анализа, не превышает 0,6 мг-экв (качественная проба дает заметный осадок BaSO4). При большом осадке следует разбавлять исследуемый фильтрат, при малом- сгущать выпариванием.
Необходимые реактивы:
барий хлористый 0,05 н. раствор;
6,11 г ВаCl2×2Н2О растворить в дистиллированной воде и довести объем до 1 литра; нормальность раствора установить по титрованному раствору трилона Б;
магний хлористый 0,05 н. раствор;
5,08 г МgCl2×6 Н2О растворить в дистиллированной воде до 1 литра; нормальность раствора установить по титрованному раствору трилона Б;
трилон Б (комплексон III), 0,05 н. раствор;
9,3 г трилона Б растворить в дистиллированной воде и довести объем до 1 литра; нормальность раствора устанвливают по перекристаллизованному МgSO4×7 Н2О;
аммиачная буферная смесь: NH4Cl –20 г, NaОН – 7 г, КОН-10 г, NH4ОН –400 мл;
растворить хлористый аммоний в дистиллированной воде, добавить необходимое количество NaОН и КОН, затем влить концентрированный аммиак (25 %-ный) и смесь довести до 1 литра дистиллированной водой;
сухая индикаторная смесь хромоген черного с КСl 1:99;
соляная кислота, плотностью 1,19 г/см3;
аммиак 10%-ной концентрации;
гидроксиламин солянокислый или сернокислый.
Порядок проведения анализа:
пробу фильтрата поместить в коническую колбу на 25 мл; разбавить водой до 100 мл;
подкислить соляной кислотой (плотность 1,19 г/см3) до изменения окраски бумажки конго в сине-фиолетовую (рН=3); кипятить в течение нескольких минут для удаления углекислого газа, сразу же прибавить 5-10 мл 0,05 н. раствора хлористого бария и оставить в покое для охлаждения до комнатной температуры;
нейтрализовать фильтрат аммиаком (до покраснения бумажки конго, рН=5,2);
прилить равное с ВаСl2 количество 0,05 н. раствора хлорида магния и, не отфильтровывая осадка, внести 5-10 кг гидроксиламина, 10-25 мг индикатора хромоген черного;
добавить 5-10 мл аммиачно-буферной смеси и титровать 0,05 н. раствором трилона Б до изменения окраски от винно-красной до сине-голубой, в конце титрования следует ввести индикатор дополнительно;
после этого (или предварительно) оттитровать смесь растворов ВаСl2+ MgCl2, взятых в тех же объемах, которые внесены в испытуемый раствор; разбавить смесь дистиллированной водой до 100 мл, внести 5 мл буферной смеси, прибавить хромоген черный и титровать трилоном Б; этим титрованием устанавливают количество ионов бария, внесенного в раствор для осаждения сульфат-ионов.
Сумма щелочно-земельных элементов, как правило, известна, так как анализ на определение Са2+ и Мg2+ проводится заранее.
Обработка полученных данных.
Концентрация сульфат-иона рассчитывается по формулам:
хSO42-=[V1-(V2-V3)]×Н× 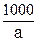 , (34)
, (34)
УSO42-= хSO42 ×Э (35)
где хSO42(УSO42-) – концентрация сульфат-иона, мг-экв/л (мг/л);
V1 – объем трилона Б, израсходованного на титрование отдельной
пробы смеси ВаСl2+ MgCl2, мл;
V2 – объем трилона Б, израсходованного на титрование пробы фильтрата, мл;
V3 - объем трилона Б, израсходованного на титрование суммы Са2+ и Мg2+, мл;
Н – нормальность раствора трилона Б;
Э – эквивалент аниона SO42-, равный 48;
а – объем фильтрата, взятого на определение сульфатов, мл
