Схема кристаллической решетки металлов.
 |  |  |  |
  . . |  . . . . |  . . |
  . . . . |  . . |  . . |
  . . |  . . . . |  . . . . |
В углах кристаллической решетки находятся ионы металлов (M e n+1), между ними относительно свободно перемещаются валентные электроны, осуществляя связь между всеми атомами и ионами металла.
Химическая связь между атомами и ионами металлов, основанная на обобществлении валентных электронов получила название металлической.
Металлическая связь довольна прочная, особенно у тяжелых металлов, чем и объясняется определенный комплекс физических и химических свойств металлов. Прочность металлической связи обеспечивает устойчивость кристаллической решетки и пластичность металлов, то есть способность подвергаться разнообразной обработке без разрушения; свободное передвижение валентных электронов позволяет металлам хорошо проводить электрический ток и тепло. Строением кристаллической решетки металла объясняется также способность отражать световые волны, то есть металлический блеск.
Металлическая связь проявляется в твердом и жидком состоянии металла, тогда как в газообразном состоянии молекулы металла представляют собой отдельные атомы, почти не действующие друг на друга.
Однако и у неметаллов при определенных условиях, например, у фосфора при сверхвысоком давлении, атомная связь переходит в металлическую; у металла висмута в твердом состоянии наряду с металлической имеется атомная связь.
д) Водородная связь.
Ионная, ковалентная, металлическая, химические связи являются только внутримолекулярными, но особый вид межмолекулярного и внутримолекулярного взаимодействия представляет водородная связь. Примером внутримолекулярной водородной связи может быть водородная связь в двухосновной кислоте:
 |
 О
О
 С
С
 О-δ H +δ
О-δ H +δ

 О-δ H
О-δ H

 С
С
О
Примером межмолекулярной связи может быть водородная связь между молекулами воды:

 H +δ О –δ …H +δ О –δ
H +δ О –δ …H +δ О –δ


H +δ H+δ
Водородная связь образуется между атомом водорода, связанным с сильным электроотрицательным элементом и другим сильным электроотрицательным элементом.
Водородная связь может рассматриваться как некоторая дополнительная связь, которую проявляет атом водорода, уже связанный в молекуле ковалентной связью с другим атомом.
Атом водорода образует водородную связь лишь с атомами определенных элементов, к которым относятся атомы F, CL, O, S, N (фтора, хлора, кислорода, серы, азота). Эти атомы сильно стягивают на себя общую электронную пару, что вызывает появление у них эффективного отрицательного заряда и приводит к превращению атома водорода в протон, почти лишенный электрона.
В отличии от других положительных ионов положительный ион водорода не имеет электронов, поэтому не отталкивается электронными облаками названных выше отрицательно заряженных атомов, а только притягиваются. Так как размеры протона во много раз меньше размеров других ионов, то это позволяет ему ближе подходить к другим частицам. Водородная связь и является причинной ассоциации молекул некоторых водородных соединений. Например, во фтороводороде существуют не только молекулы HF, но и ассоциирование агрегаты (HF)2 и (HF) 3
 F- F -
F- F -
. .
. H+ . H +
. . .
. . .

 H+ . H +
H+ . H +
.
F - F –
В обычной воде за счет водородной связи существуют ассоциированные молекулы состава (H2O)n, где n=2,3,4,5…; простые молекулы воды существуют в парообразном состоянии:
O . . . H H O
 |  |  |  |  |  |
. . H H O . . . . .H H
Именно наличием водородных связей объясняется повышением температуры кипения (1000 С) по сравнению с водородными соединениями элементов подгруппы кислорода (H2S, H2Se, H2Te) а также ее жидкое и твердое агрегатные состояния при незначительной молекулярной массе.
Существование ассоциатов у воды и является причиной различных аномалий воды.
Особенно распространены водородные связи в молекулах белков, нуклеиновых кислот и других биологически важных соединений. Водородную связь могут иметь разнородные молекулы, например, воды и спирта:
 С2H5 O . . . . H H .
С2H5 O . . . . H H .
 .
.
H . . . O .
Водородные связи обозначают пунктирной линией или точками и этим указывают, что она намного слабее ковалентной связи (примерно в 15-20 раз).
Итак, водородная связь – это химическая связь, образованная атомом водорода, связанного с атомом другого элемента, который обладает большим значением электроотрицательности.
Валентность элементов.
Валентность элементов - это число химических связей, которые атом этого элемента образует с другими атомами в данной молекуле. Валентность элемента определяется числом неспаренных электронов в его атоме.
Атомы многих элементов могут увеличивать свою валентность в результате перехода из основного состояния в возбужденное состояние, то есть состояние с более высокой энергией, чем основное.
Процесс перехода атома из основного в возбужденное состояние называется возбуждением атома, происходит разъединение спаренных электронов и переход одного из них с данного подуровня на свободную орбиталь другого подуровня в пределах одного энергетического уровня.
Например, атом углерода в основном состоянии является двухвалентным, так как из четырех электронов внешнего электронного слоя (2s2 2p2) только два являются неспаренными:
 | |||
 |

 6С свободная орбиталь
6С свободная орбиталь
2p



 2s
2s
При поглощении энергии E один из электронов 2s подуровня переходит на свободную орбиталь 2p – подуровня, в результате чего образунтся четыре неспаренных электрона:














 + E
+ E
 |
2p 2p 2s12p3
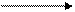 2s 2s
2s 2s
В возбужденном состоянии углерод является четырехвалентным.
Энергия возбуждения атомов компенсируется энергией образования новых химических связей.
Возбуждение атомов возможно не для всех элементов.
Например, атомы кислорода и серы имеют одинаковую конфигурацию внешнего электронного слоя s2 p 4 , так как кислород и сера находится в главной подгруппе VI группы. В невозбужденном состоянии имеют по два неспаренных электрона на внешнем электронном слое:
 | |||
 |
8О 16 S 3 d





 2p 3p
2p 3p
2s 3s
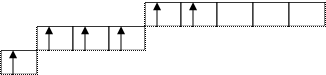
В основном состоянии кислород и сера имеют одинаковую валентность, равную двум. Но атом серы может перейти в возбужденное состояние за счет перехода электронов с 3s и 3p – подуровней на свободные орбитали 3d –подуровня:
S










 + Е
+ Е
















 3d S * 3d
3d S * 3d




 3p 3p
3p 3p
3s основное состояние + E
 В II 3s
В II 3s
3s23p4 S *
Возбужденное состояние В IV
 3d
3d
3p
Возбужденное
3s 3s13p33d2 состояние B VI
Это является причиной переменной валентности серы. Атом кислорода не может перейти в возбужденное состояние, потому что на втором энергетическом уровне отсутствует d – подуровень, т.е. нет свободных орбиталей, что и является причиной постоянной валентности кислорода во всех соединениях.
Для большинства элементов максимальное число неспаренных электронов в основном или в возбужденном состоянии равно номеру группы, в которой находится элемент.
Высшая валентность элементов, как правило, равно номеру группы (исключения рассмотрелны ранее).
Следовательно, валентность элемента определяется числом орбиталей, которые атом данного элемента может использовать для образования химических связей.
Это могут быть: орбитали с неспаренными электронами; орбитали с неподелнными электронными парами; свободные орбитали.
Степень окисления
Степень окисления – это одно из основных понятий химии. Оно характеризует состояние атома в соединении. Степень окисления – это условный заряд атома в соединении, вычисленный, исходя из предположения, что оно состоит только из ионов. Степень окисления может быть положительной (+), отрицательный (-) и нулевой. Обозначается арабскими цифрами, которые ставят над символом элемента +1 -2 0
(Na2O; CL2).
Положительная степень окисления показывает, сколько электронов нейтральный атом отдал при образовании химической связи:
0 _ +6
 S – 6е S
S – 6е S
Максимальная положительная степень окисления обычно равна номеру группы.
Отрицательная степень окисления показывает, сколько электронов нейтральный атом присоединил при образовании химической связи.
0 _ -2
 S + 2е S
S + 2е S
При определении степени окисления элемента в соединении необходимо помнить: степень окисления водорода во всех соединениях за исключением гидридов металлов (Na+1H-1, Li+1H-1, Ca+2H-1 и др.) равна «+1», H+1; степень окисления кислорода во всех соединениях равна «-2», О-2 за исключением пероксидов водорода и металлов (О+2F-12 H+12O-12 Na+12O-12 Ca+2O-12 и др.); металлы в соединениях всегда имеют положительную степень окисления – щелочные (Li, Na, K и др. ) «+1» , щелочноземельные (Ca, Ba и др. II группы, кроме ртути) - «+2» , алюминий - «+3» ; фтор – «-1» ; степень окисления атомов в простых веществах всегда равна нулю (O02 H02 и тд.) – это элементы, имеющие постоянную степень окисления.
Элементы с переменной степенью окисления: медь (+1) и (+2), железо (+2) и (+3), ртуть (+1) и (+2) .
Все элементы имеют высшую степень окисления, которая как правило, равна номеру группы П.С. ; низшую (минимальную) степень окисления у металлов равная нулю, у неметаллов равна – (8 – номер группы, в которой находится элемент); значения степеней окисления между высшей и низшей степенями окисления называются промежуточными (азот: низшая (-3) , промежуточные (-2; -1; 0; +1; +2; +3; +4) и высшая (+5) .
Любая молекула является электронейтральной, поэтому алгебраическая сумма степеней окисления всех атомов в молекуле всегда равна нулю.
Степень окисления не всегда численно совпадает с валентностно. Например, в N2 (N = N) степень окисления азота равна нулю, а валентность – трем; в H2O2 (H – O – O – H) степень окисления кислорода (-1) , а валентность равна двум.
