Получение в свободной виде
Элемент хром (Cr) не встречается в природе в свободном виде. Единственной полезной рудой является шпинелевая руда, хромит или хромистый железняк, представляющий собой хромит железа , который широко распространен на земной поверхности. Кроме хромовой кислоты, эта руда содержит также другие вещества в различных пропорциях. Коммерческой ценностью обладают только те руды или концентраты, которые содержат более 40% оксида хрома .
Хромит добывается в шахтах подземного и открытого типа. Руда дробится и при необходимости обогащается.
Физические и химические свойства.
Физические свойства.
Хром — серовато-белый блестящий металл по внешнему виду похож на сталь. Из металлов он самый твердый, его плотность 7,19 г/см3, т. пл. 1855 °С. Природный хром состоит из смеси пяти изотопов с массовыми числами 50, 52, 53, 54 и 56. Радиоактивные изотопы получены искусственно.
Хром обладает всеми характерными свойствами металлов — хорошо проводит тепло, почти не оказывает сопротивления электрическому току, имеет присущий большинству металлов блеск. Любопытна одна особенность хрома: при температуре около 37°С он ведет себя явно «вызывающе» — многие его физические свойства резко, скачкообразно меняются. В этой температурной точке внутреннее трение хрома достигает максимума, а модуль упругости падает до минимальных значений. Так же внезапно изменяются электропроводность, коэффициент линейного расширения, термоэлектродвижущая сила. Пока ученые не могут объяснить эту аномалию.
Даже незначительные примеси делают хром очень хрупким, поэтому в качестве конструкционного материала его практически не применяют, зато как легирующий элемент он издавна пользуется у металлургов почетом. Небольшие добавки его придают стали твердость и износостойкость. Такие свойства присущи шарикоподшипниковой стали, в состав которой, наряду с хромом (до 1,5%), входит углерод (около 1%). Образующиеся в ней карбиды хрома отличаются исключительной твердостью — они-то и позволяют металлу уверенно сопротивляться одному из опаснейших врагов — износу.
В качестве представителя металлов, относящихся к побочным подгруппам периодической системы, рассмотрим хром: он возглавляет побочную подгруппу VI группы. Хром — металл, по внешнему виду похожий на сталь. От ранее рассмотренных металлов он, как и все металлы с достраивающимся предпоследним электронным слоем атома, отличается тугоплавкостью и твердостью. По твердости хром превосходит все металлы, он царапает стекло.
Химические свойства.
 |
Расположение электронов на 3d- и 4s-орбиталях атома хрома можно представить схемой:
Отсюда видно, что хром может проявлять в соединениях различные степени окисления — от +1 до +6; из них наиболее устойчивы соединения хрома со степенями окисления +2, +3, +6. Таким образом, в образовании химических связей участвует не только электрон внешнего уровня, но и пять электронов d-подуровня второго снаружи уровня.
Как и у алюминия, на поверхности хрома образуется оксидная пленка Сr2О3. Поэтому хром в разбавленных серной и соляной кислотах начинает растворяться не сразу, а после растворения оксидной пленки:
Cr + 2H+=Cr5+ + H2
В азотной и концентрированной серной кислотах хром не растворяется, так как его оксидная пленка упрочняется, т. е. хром переходит в пассивное состояние. По этой же причине не взаимодействуют с хромом разбавленные серная и соляная кислоты, содержащие растворенный кислород. Пассивацию хрома можно устранить очисткой поверхности металла.
При высокой температуре хром горит в кислороде, образуя оксид Cr2О3. Раскаленный хром реагирует с парами воды:
2Cr + ЗН2О = Cr2О3 + ЗН2
Металлический хром при нагревании реагирует также с галогенами, галогеноводородами, серой, азотом, фосфором, углем, кремнием и бором. Например:
Cr + 2HF = CrF2 + H2 ; 2Cr + N2 = 2CrN
2Cr + 3S = Cr2S3; Cr + Si = CrSi
На воздухе хром совершенно не изменяется. Поэтому хромом с помощью электролиза его соединений покрывают — хромируют — стальные изделия для предохранения их от ржавления и механического износа. Эти же качества хром придает своим сплавам с железом — хромистым сталям. К ним относится нержавеющая сталь, содержащая около 12% хрома.
В быт нержавеющая сталь вошла в виде вилок, ножей и других предметов домашнего обихода. Блестящие, серебристого цвета полосы нержавеющей стали украшают арки станции «Маяковская» Московского метрополитена.
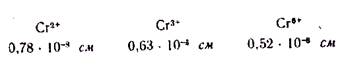 При химических реакциях атом хрома может отдавать, кроме единственного электрона наружного слоя, до 5 электронов предпоследнего слоя, т. е. проявлять высшую степень окисления (+6). Но, как и все элементы с достраивающимся предпоследним слоем атома, хром проявляет несколько значений степеней окисления, т. е. кроме высшего и низшие значения, а именно + 2 и + 3. У металлов с переменной валентностью, как и у элементов одного и того же периода, например III, с возрастанием степени окисления уменьшается радиус иона. Так, у хрома:
При химических реакциях атом хрома может отдавать, кроме единственного электрона наружного слоя, до 5 электронов предпоследнего слоя, т. е. проявлять высшую степень окисления (+6). Но, как и все элементы с достраивающимся предпоследним слоем атома, хром проявляет несколько значений степеней окисления, т. е. кроме высшего и низшие значения, а именно + 2 и + 3. У металлов с переменной валентностью, как и у элементов одного и того же периода, например III, с возрастанием степени окисления уменьшается радиус иона. Так, у хрома:
Радиус иона
При этом соблюдается та же самая закономерность в изменении химических свойств соединений металла с возрастанием его степени окисления, как у элементов одного и того же периода, а именно:
1. С возрастанием степени окисления основные свойства гидроксидов ослабляются, а кислотные усиливаются.
2. При одинаковых значениях степени окисления и близких значениях ионного радиуса химические свойства гидроксидов элементов оказываются сходными.
Это мы и наблюдаем на гидроксидах хрома, учитывая близость численных значений радиусов ионов Сг2 и Mg2 ; Сг3 и А13; С г6 и S6*:
 Гидроксиды хрома
Гидроксиды хрома
Гидроксиды элементов III периода
Хром образует три ряда соединений:

Познакомимся с важнейшими из этих соединений. При растворении хрома в кислотах получаются соли, в которых хром двухвалентен, например:

Соединения двухвалентного хрома сходны по составу и свойствам с соединениями магния; гидроксид хрома (II) является основанием.
проявляют все соединения, в которых содержится хром в степени окисления +6: оксид.
Свойства соединений.
Оксиды
Оксид хрома (II) CrO (основной) - сильный восстановитель, чрезвычайно неустойчив в присутствии влаги и кислорода. Практического значения не имеет.
Оксид хрома (III) Cr2O3 (амфотерный) устойчив на воздухе и в растворах.
Cr2O3 + H2SO4 = Cr2(SO4)3 + H2O
Cr2O3 + 2NaOH = Na2CrO4 + H2O
Образуется при нагревании некоторых соединений хрома (VI), например:
4CrO3 2Cr2O3 + 3О2
(NH4)2Cr2O7 Cr2O3 + N2 + 4H2O
4Cr + 3O2 2Cr2O3
Оксид хрома (III) используется для восстановления металлического хрома невысокой чистоты с помощью алюминия (алюминотермия) или кремния (силикотермия):
Cr2O3 +2Al = Al2O3 +2Cr
2Cr2O3 + 3Si = 3SiO3 + 4Cr
Оксид хрома (VI) CrO3 (кислотный) - темно малиновые игольчатые кристаллы.
Получают действием избытка концентрированной H2SO4 на насыщенный водный раствор бихромата калия:
K2Cr2O7 + 2H2SO4 = 2CrO3 + 2KHSO4 + H2O
Оксид хрома (VI) - сильный окислитель, одно из самых токсичных соединений хрома.
При растворении CrO3 в воде образуется хромовая кислота H2CrO4
CrO3 + H2O = H2CrO4
Кислотный оксид хрома, реагируя со щелочами, образует желтые хроматы
CrO42
CrO3 + 2KOH = K2CrO4 + H2O
Гидроксиды
Гидроксид хрома (III) обладает амфотерными свойствами, растворяясь как в
кислотах (ведет себя как основание),так и в щелочах (ведет себя как кислота):
2Cr(OH)3 + 3H2SO4 = Cr2(SO4)3 + 6H2O
Cr(OH)3 + KOH = K[Cr(OH)4]
Cr(OH)3 + NaOH = NaCrO2 + 2H2O
При прокаливании гидроксида хрома (III) образуется оксид хрома (III) Cr2O3.
Нерастворим в воде.
2Cr(OH)3 = Cr2O3 + 3H2O
Кислоты
Кислоты хрома, отвечающие его степени окисления +6 и различающиеся соотношением числа молекул CrO3 и H2O, существуют только в виде растворов. При растворении кислотного оксида CrO3, образуется монохромовая кислота (просто хромовая) H2CrO4.
CrO3 + H2O = H2CrO4
Подкисление раствора или увеличение в нем CrO3 приводит к кислотам общей формулы nCrO3 H2O
при n=2, 3, 4 это, соответственно, ди, три, тетрохромовые кислоты.
Самая сильная из них - дихромовая, то есть H2Cr2O7. Хромовые кислоты и их соли- сильные окислители и ядовиты.
Соли
Различают два вида солей: хромиты и хроматы.
Хромитами с общей формулой RCrO2 называются соли хромистой кислоты HCrO2.
Cr(OH)3 + NaOH = NaCrO2 + 2H2O
Хромиты обладают различной окраской - от темно коричневой до совершенно черной и обычно встречаются в виде сплошных массивов. Хромит мягче многих других минералов, температура плавления хромита зависит от его состава 1545-1730 0 С.
Хромит имеет металлический блеск и почти нерастворим в кислотах.
Хроматы - соли хромовых кислот.
Соли монохромовой кислоты H2CrO4 называют монохроматами (хроматы) R2CrO4, соли дихромовой кислоты H2Cr2O7 дихроматы (бихроматы) - R2Cr2O7. Монохроматы обычно окрашены в желтый цвет. Они устойчивы только в щелочной среде, а при подкислении превращаются в оранжево-красные бихроматы:
2Na2CrO4 + H2SO4 = Na2Cr2O7 + Na2SO4 + H2O
