Природный гипс, природный ангидрит
Природный гипс и природный ангидрит встречаются в природе как породообразующие в больших и легкодоступных месторождениях; они возникли в результате выкристаллизовывания при испарении морских водоёмов. Особо богатые залежи образовались в пермском, триасовом и третичном периоде. Во всём мире они представляли важнейший источник сырья для производства гипса для технического использования. С сегодняшней точки зрения при возникновении этих залежных месторождений вначале образовался гипс, а из него позднее из-за увеличивающегося давления и повышенной температуры в некоторых залежных месторождениях появился ангидрит, который при поглощении воды частично снова регидратизировался в гипс [183].
В зависимости от месторождений доломитовый и ангидритный камни могут быть не чистыми, имея в своём составе такие примеси как известняк, доломит или глины. В небольших количествах они не влияют на пригодность сырья. Структура и цвет гипсового или же ангидритного камня могут быть различными (каменный гипс, зернистый гипс, волокнистый гипс, кристаллический гипс, алебастр, крупнозернистый ангидрит, плотный ангидрит; белый, серый, красноватый, чёрный). Некоторые гипсовые залежи содержат природную нефть, находящуюся в более глубоких слоях.
Химический гипс
При производстве сырой фосфорной кислоты, плавиковой кислоты и других кислот, а также диоксида титана, в больших количествах в виде сырых порошковых побочных продуктов образуются так называемые химический гипс или химический ангидрит (также их называют синтетическим гипсом или синтетическим ангидритом). При изготовлении сырой фосфорной кислоты, в соответствии с уравнением 30, из 1 т сырьевого фосфата (например, фторапатита) и 1 т серной кислоты получается 1,7 т фосфогипса и 0,4-0,5 т фосфорной кислоты. Ежегодно получается, таким образом, около 100 млн. т фосфогипса, из которого лишь небольшое количество находит применение (< 2%) [184]. Причина такого незначительного использования фосфогипса заключается в технологических трудностях при дальнейшей переработке, которые делают применение фосфогипса нерентабельным [185]. Содержащиеся в фосфогипсе примеси являются водорастворимыми и водонерастворимыми, такими неорганическими и органическими веществами как фосфаты, силикаты гексофтора и остатками кислот, большей частью в виде солей натрия или кальция. Нередко они ухудшают свойства при переработке и применении строительного гипса. Фосфогипс должен, поэтому, до своего применения очищаться с помощью промывки, флотации и гидравлической классификации, что является очень затратным. Для изготовления штукатурного гипса необходима перекристаллизация с добавкой известкового гидрата для того, чтобы устранить вызываемую кислыми фосфатами восприимчивость извести, а также неподходящую структуру частиц.
Ca10(PO4)6F2 + 5H2SO4 + 10H2O →
Фтороапатит
→ 5CaSO4·2H2O+3H3PO4 + H2F2
фосфорная кислота плавиковая кислотаУравнение 30
При промышленном изготовлении белого пигмента из минерала ильменит в соответствии с уравнениями 31 и 32получается большое количество разбавленной серной кислоты, которая раньше сбрасывалась с кораблей в Северном море. Сегодня эта кислота нейтрализуется с помощью известняка, при этом образуется так называемый титаногипс в виде крупных кристаллов. Он мало используется в строительстве из-за примесей тяжёлых металлов.
FeTiO3 + конц. H2SO4 → TiOSO4 + FeSO4 + разб. H2SO4Уравнение 31
Ильменит сульфат титана разбавленная кислота
разб. H2SO4 + CaCO3 → CaSO4·2H2O + CO2↑ Уравнение 32
Для гипсовой и цементной промышленности по-прежнему имеет значение и побочный ангидрит из производства фтороводорода, так называемый фтороангидрит или ангидрит плавиковой кислоты. Он получается в сухом, с мелкими частицами виде при изготовлении плавиковой кислоты из флюорита (плавикового шпата) и серной кислоты в соответствии с уравнением 33. Из 1 т флюорита и 1,25 т серной кислоты образуется 0,5 т плавиковой кислоты и 1,7 т ангидрита. По этому способу в мире ежегодно получается около 2-3 млн.т фторогипса [184], которые используются лишь частично (например, для бесшовного пола).
CaF2 + конц. H2SO4 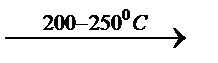 CaSO4 + H2F2Уравнение 33
CaSO4 + H2F2Уравнение 33
флюорит ангидрит плавиковая кислота
УДДГ-гипс
Гипс из дымовых газов получается при промывке отработанных газов установкой для десульфитизации дымовых газов (УУСДГ) и поэтому называется также УУСДГ-гипсом (англ. “desulfogypsum” или FGD-Gypsum = Flue Gas Desulfurization Gypsum). Он образуется из влажного, состоящего из мелких частиц порошка при десульфитизации газов (дымовых газов) после сжигания ископаемого топлива (каменный уголь, бурый уголь, нефть) на крупных установках для сжигания, например, электростанций. Десульфитизация осуществляется путём промывки дымовых газов с помощью суспензий известняка или извести. При этом содержащийся в дымовых газах диоксид серы, привязанный вначале к сульфиту кальция, преобразуется в легкорастворимый гидрогенный сульфит кальция и затем с помощью кислорода воздуха легко окисляется в гипс.
Ca(OH)2 + SO2 → CaSO3 + H2OУравнение 34
CaSO3 + ½ O2 + 2 H2O → CaSO4·2H2OУравнение 35
Благодаря очистке дымовых газов содержание SO2 с 800-1200 мг/м3 снижается примерно до 100 мг/м3 в отработанном газе. По этому способу с введением распоряжения о крупных топочных установках (КТУР) только в Германии выброс SO2 была сокращён с 1,55 млн. т (1982 г.) до 0,22 млн. т (1988 г.). Путём вакуумной фильтрации гипс обезвоживается с остатком влаги около 10% и, одновременно с этим, освобождается от ненужных примесей, главным образом хлоридов. Пригодная для изготовления штукатурного гипса структура частиц может быть достигнута с помощью прессования. Из 1 т серы в топливе получается 5,4 т гипса. Такой способ получения гипса из дымовых газов в гипсовой и цементной промышленности технически возможен и имеет большое экономическое значение [184, 186].
Сульфат кальция другого происхождения, образующийся, например, при изготовлении органических и неорганических кислот (винная, лимонная, щавелевая, борная кислота), или же при переработке сульфатсодержащих сточных вод, из-за большого содержания нежелательных загрязнений и высокого содержания влаги не получил до сих пор технического значения. Размолотые осколки гипсовых форм из керамической промышленности находят частичное применение в качестве регулятора схватывания при производстве цемента.
