Принцип работы гальванических элементов
Простейший медно-цинковый гальванический элемент Вольта(рис. 4.1) состоит из двух пластин (электродов): цинковой 2 (катода) и медной 1 (анода), опущенных в электролит 3 (водный раствор серной кислоты H2S04).
При растворении серной кислоты в воде часть молекул кислоты распадается на положительные ионы водорода H2+ и отрицательные ионы кислотного остатка S04-.
Одновременно происходит растворение цинкового электрода в серной кислоте. П 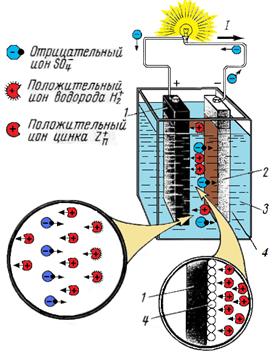 оложительные ионы цинка Zn+ переходят в раствор и соединяются с отрицательными ионами S04- кислотного остатка, образуя нейтральные молекулы сернокислого цинка ZnS04.
оложительные ионы цинка Zn+ переходят в раствор и соединяются с отрицательными ионами S04- кислотного остатка, образуя нейтральные молекулы сернокислого цинка ZnS04.
При этом на цинковом электроде будут скапливаться оставшиеся свободные электроны, вследствие чего этот электрод приобретает отрицательный заряд. В электролите же образуется положительный заряд ввиду нейтрализации части отрицательных ионов S04-.
Таким образом, в пограничном слое между цинковым электродом и электролитом возникает некоторая разность потенциалов и создается электрическое поле, которое препятствует дальнейшему переходу положительных ионов цинка в электролит; при этом растворение цинкового электрода прекращается.
Медный электрод практически не растворяется в электролите и приобретает тот же положительный потенциал, что и электролит.
Разность потенциалов медного φСu и цинкового φZn электродов при разомкнутой внешней цепи представляет собой э.д.с. Ерассматриваемого гальванического элемента.
|
При подключении к электродам гальванического элемента какого-либо приемника электрической энергии по внешней цепи начнет протекать ток I от медного электрода (положительный полюс элемента) к цинковому (отрицательный полюс).
В электролите в это время начнется движение положительных ионов цинка Zn+ и водорода от цинковой пластины к медной и отрицательных ионов кислотного остатка S04- от медной пластины к цинковой. В результате нарушится равновесие электрических зарядов между электродами и электролитом, вследствие чего в электролит с катода снова начнут поступать положительные ионы цинка Zn+, поддерживая на этом электроде отрицательный заряд: на медном же электроде будут осаждаться новые положительные ионы. Таким образом, между анодом и катодом все время будет существовать разность потенциалов, необходимая для прохождения тока по электрической цепи.
Элемент Вольта не может долго работать. Ионы водорода на медном электроде создают как бы другой элемент с э.д.с., направленной против основной и ухудшающей электрические свойства элемента. Для нейтрализации добавляют деполяризаторы.
Контрольные вопросы
1. Как называются устройства, преобразующие химическую энергию в электрическую?
2. Что такое электролит?
3. Что такое электролиз?
4. На какие составляющие распадается молекула серной кислоты?
5. Из чего состоит гальванический элемент Вольта?
6. Как происходит поляризация элемента?
7. Какое воздействие оказывают ионы водорода на работу аккумуляторной батареи?
8. Что такое сухой гальванический элемент?
9. Как проходит электрический ток в жидких проводниках?
