Метод определения аминного азота методом формольного
Титрования
Метод основан на связывании аминогрупп с формалином и косвенном определении их количества по результатам титрования карбоксильных групп.
Оборудование, реактивы: весы аналитические класса 2 с пределами измерений от 0 до 200 г; потенциометр постоянного тока измерительный с пределами измерений значений рН от 0 до 14; стаканы стеклянные лабораторные вместимостью 500 и 100 см3; пипетки вместимостью 2, 10, 20 см3; цилиндр мерный вместимостью 10 см3; колба мерная вместимостью 100, 250 см3; бюретка вместимостью 25 см3; мешалка магнитная; марля медицинская; бумага фильтровальная; ступка фарфоровая с пестиком вместимостью 250 см3; кислота трихлоруксусная 200 г/ дм3 (20 %-ная); вода дистиллированная; хлорид бария; натрия гидроксид, раствор 0,1 моль/ дм3 (0,1 н), 0,02 моль/ дм3 (0,02 н) и 2 моль/дм3 (2 н); кислота соляная 0,5 н раствор; кислота розоловая; формалин, раствор 400 г/ дм3 (40 %-ный) нейтрализованный – формалин нейтрализуется в день анализа раствором 0,1 моль/ дм3 (0,1 н) гидроксида натрия до рН = 7; кислота серная, раствор 0,05 моль/ дм3 (0,1 н); спирт этиловый ректификованный; индикатор смешанный (Таширо) - схема приготовления см. п.2.1.3; бумага лакмусовая, фенолфталеин 1 %-ный спиртовой раствор.
Проведение анализа:
для жидкой навески исследуемого продукта:
Сначала проводят контрольное титрование.
В стеклянный стакан наливают 20 см3 дистиллированной воды, помещают магнит. В стакан помещают электроды, приливают 10 см3 нейтрализованного формалина, включают мешалку и титруют жидкость раствором 0,02 моль/ дм3 гидроксида натрия до рН = 9.
При проведении рабочего анализа в стакан вместимостью 50 см3 помещают 0,2-0,3 г исследуемого продукта, взвешенного с абсолютной погрешностью не более 0,001 г, и доводят объем дистиллированной водой до 20 см3. В стакан опускают магнит, электроды.
Раствор нейтрализуют 0,1 моль/ дм3 гидроксида натрия до рН = 6,8-7,0.
При работе с очень кислыми продуктами (рН = 1,0) начинать нейтрализацию удобно раствором 1 моль/ дм3 (1 н) гидроксида натрия, постепенно переходя к концентрации 0,1 моль/ дм3 и 0,02 моль/ дм3.
По окончании нейтрализации в раствор добавляют 10 см3 формалина (рН от 4,5 до 5,5) и титруют раствором 0,02 моль/ дм3 (0,02 н) гидроксида натрия до рН = 9.
Массовую долю аминного азота 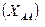 в процентах вычисляют по формуле:
в процентах вычисляют по формуле:
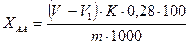 , (3.7)
, (3.7)
где  - объем раствора гидроксида натрия 0,02 моль/ дм3, израсходованный на титрование исследуемого образца, см3;
- объем раствора гидроксида натрия 0,02 моль/ дм3, израсходованный на титрование исследуемого образца, см3; 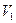 - объем раствора гидроксида натрия 0,02 моль/ дм3, израсходованный на титрование контрольного образца, см3;
- объем раствора гидроксида натрия 0,02 моль/ дм3, израсходованный на титрование контрольного образца, см3; 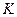 - коэффициент пересчета на точный раствор 0,02 моль/ дм3 гидроксида натрия;
- коэффициент пересчета на точный раствор 0,02 моль/ дм3 гидроксида натрия; 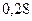 - количество аминного азота, соответствующее 1 см3 раствора 0,02 моль/ дм3 гидроксида натрия, мг;
- количество аминного азота, соответствующее 1 см3 раствора 0,02 моль/ дм3 гидроксида натрия, мг; 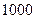 - коэффициент пересчета в мг в г;
- коэффициент пересчета в мг в г; 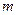 - навеска исследуемого образца, г.
- навеска исследуемого образца, г.
За окончательный результат принимают среднее арифметическое значение результатов двух параллельных определений, допускаемые расхождения между которыми не должны превышать 0,2 %.
Вычисление проводят до третьего десятичного знака.
для всех остальных продуктов:
Делают водную вытяжку из 50 г тщательно измельченного (растертого с дистиллированной водой) в фарфоровой ступке исследуемого продукта и осаждают в ней белки трихлоруксусной кислотой, как описано в п. 2.2.1.
Отфильтровав осадок, отбирают 100 см3 фильтрата и прибавляют к нему для осаждения фосфатов и углекислых солей 2 г сухого хлорида бария и 2 н раствор гидроксида натрия до сильнощелочной реакции на лакмус. После 15-минутного отстаивания жидкость фильтруют через сухой бумажный фильтр в колбу.
Отбирают по 25 см3 фильтрата в три колбы с притертыми пробками. В одну из них вносят 10 капель розоловой кислоты и производят нейтрализацию раствора сначала 0,5 н раствором соляной кислоты, а затем 0,1 н раствором гидроксида натрия. Две другие колбы служат для определения аминного азота формольным титрованием. Для этого в них вносят израсходованное количество 0,5 н раствора соляной кислоты и 0,1 н раствора гидроксида натрия, затем приливают по 15 см3 формалина, предварительно нейтрализованного щелочью, и оттитровывают 0,1 н раствором гидроксида натрия в присутствии фенолфталеина до яркого розового окрашивания.
Массовую долю аминного азота 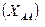 в процентах вычисляют по формуле:
в процентах вычисляют по формуле:
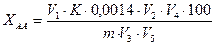 , (2.8)
, (2.8)
где 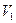 - объем 0,1 н раствора гидроксида натрия, израсходованного на титрование, см3;
- объем 0,1 н раствора гидроксида натрия, израсходованного на титрование, см3;  - объем водной вытяжки в мерной колбе, см3;
- объем водной вытяжки в мерной колбе, см3;  - объем водной вытяжки, взятый для осаждения белков, см3;
- объем водной вытяжки, взятый для осаждения белков, см3;  - объем водной вытяжки, взятый для осаждения белков с учетом объема трихлоруксусной кислоты, см3;
- объем водной вытяжки, взятый для осаждения белков с учетом объема трихлоруксусной кислоты, см3; 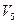 - объем фильтрата, взятого для титрования, см3;
- объем фильтрата, взятого для титрования, см3; 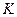 - коэффициент пересчета на точный 0,1 н раствор гидроксида натрия;
- коэффициент пересчета на точный 0,1 н раствор гидроксида натрия; 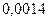 - количество азота эквивалентное 1 см3 0,1 н раствора гидроксида натрия;
- количество азота эквивалентное 1 см3 0,1 н раствора гидроксида натрия; 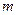 - масса навески исследуемого продукта, г.
- масса навески исследуемого продукта, г.
За окончательный результат принимают среднее арифметическое значение результатов двух параллельных определений, допускаемые расхождения между которыми не должны превышать 0,2 %.
Вычисление проводят до третьего десятичного знака.
Вопросы для самоконтроля
1. Что означают термины «сырой протеин» и «истинный протеин»? На чем основано их определение?
2. Как определяют переводной коэффициент общего азота на общий белок?
3. В каких продуктах определяют аминный азот? На чем основан метод его определения?
4. В мороженой треске азот летучих оснований составляет 45 мг %. Дайте заключение о степени свежести.
5.
ЛАБОРАТОНАЯ РАБОТА № 4
