Работа 4. Фенолы, ангидриды и амиды. Реакции конденсации
Цель работы
Целью работы является проведение реакций окисления и конденсации для фенола и его производных.
Теоретическая часть
Фенолы – ароматические соединения, имеющие гидроксильные группы, непосредственно связанные с ароматическим ядром. По числу гидроксилов различают одноатомные, двухатомные и многоатомные фенолы. Простейший из них – оксибензол называют фенолом. Оксипроизводные толуола (метилфенолы) называют орто-, мета- и паракрезолами, а оксипроизводные ксилолов – ксиленолами. Фенолы ряда нафталина называют нафтолами. Простейшие двухатомные фенолы называются: о – диоксибензол – пирокатехин, м – диоксибензол – резорцин, n- диоксибензол – гидрохинон.
Многие фенолы легко окисляются, при этом часто образуется сложная смесь продуктов. В зависимости от окислителя и условий реакции можно получить различные продукты. Так, при парофазном окислении (t=5400) о – ксилола получают фталевый ангидрид. Качественной реакцией на фенолы является проба с раствором хлорного железа, при этом образуется окрашенный ион. Фенол дает краснофиолетовую окраску, крезолы – голубую, другие фенолы – зеленую.
Реакция конденсации представляет собой внутримолекулярный или межмолекулярный процесс образования новой С-С-связи, обычно протекающий при участии конденсирующих реагентов, роль которых может быть самой различной: оказывает число каталитическое действие, давать промежуточные реакционноспособные продукты, просто связывать отщепляющуюся частицу, смещая равновесие в системе.
Реакция конденсации с отщеплением воды катализируется разнообразными реагентами: сильными кислотами ,сильными щелочами (гидроокисями, алкоголятами, амидами, гидридами щелочных металлов, аммиаком, первичными и вторичными аминами).
Порядок выполнения работы
В данной работе проводится проверка возможности окисления фенолов и образования фталеинов реакцией конденсации.
3.1 Окисления фенола и нафтола
Окисление проводится раствором марганцево-кислого калия в присутствии раствора углекислого натра (соды).
3.1.1 оборудование и реактивы:
- пробирки;
- пипетки;
- фенол – водный раствор;
- нафтол - водный раствор;
- маргацевокислый калий (0,5 % - ный водный раствор);
- углекислый натрий (5 % - ный водный раствор);
3.1.2 Проведение опыта:
а) в пробирку поместить 1 мл водного раствора фенола или нафтола;
б) прилить 1 мл раствора углекислого натра (соды);
в) приливать по каплям раствор марганцевокислого калия при встряхивании пробирки. Наблюдать за измененим окраски раствора.
Окисление фенолов обычно протекает по различным направления и ведет к образованию сложной смеси веществ. Более легкая окисляемость фенолов, по сравнению с ароматическими углеводородами, обусловлена влиянием гидроксильной группы, резко повышающей подвижность атомов водорода при других атомах углерода бензольного яда.
3.2 Образование фталеинов.
3.2.1 Получение фенолфталеина.
Фенолфталеин образуется при реакции конденсации фенола со фталевым ангидридом в присутствии концентрированной серной кислоты.
Фталевый ангидрид вступает в конденсацию с фенолами, давая производные трифенилетана. Конденсация сопровождается отщеплением воды за счет кислорода одной из карбонильных групп ангидрида и подвижных атомов водорода бензольных ядер двух молекул фенола. Введение водоотнимающих средств, таких как концентрированная серная кислота, очень облегчает эту конденсацию.
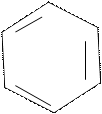
Фенол образует фенолфталеин по следующей реакции:
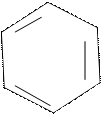 ОН HO OH
ОН HO OH
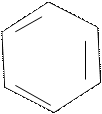
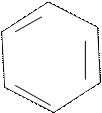
 / \ /
/ \ /
\ / \ /
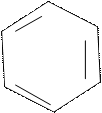
 H H С
H H С
/ O \ / \
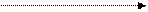 О + C2O
О + C2O
\ С / \ С /
|| ||
O O
3.2.1.1 Оборудование и реактивы:
- пробирки;
- пипетки;
- электроплитка;
- фталевый ангидрид;
- фенол;
- серная кислота концентрированная;
- серная кислота разбавленная 1:5;
- раствор едкого натрия(5-10 %-ный);
3.2.1.2 Проведение опыта:
а) взвесить 0.1-0.3 г фталевого ангидрида и поместить в пробирку;
б) в эту же пробирку добавить примерно вдвое большее количество фенола;
в) встряхнуть несколько раз содержимое пробирки и осторожно добавить к нему 3-5 капель концентрированной серной кислоты, продолжая встряхивать;
г)нагреть пробирку на электроплитке до появления темно-красного окрашивания;
д) охладить пробирку и добавить в нее 5 мл воды;
е) к полученному раствору добавить по каплям раствор щелочи и наблюдать изменение окраски;
ж) после изменения окраски к содержимому пробирки добавить несколько капелл разбавленной серной кислоты до возвращения первоначальной окраски или до обесцвечивания.
3.2.2 Получение флуоресцеина.
Флуоресциин образуется при реакции конденсации резорцина с фталевым ангидридом в присутствии концентрированной серной кислоты.
Двухатомные фенолы с гидроксильными группами в мета – положении, вступая в конденсацию, выделяют две молекулы воды, одну за счет кислорода одной из карбонильных групп ангидрида и подвижных атомов водорода бензольных ядер двух молекул фенола. вторая молекула воды выделяется за счет гидроксильных групп двух молекул фенола с образованием шестичленного кольца.
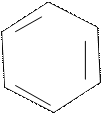
Резорцин образует флуоресцеин по следующей реакции:
 OH HO ОН HO OH
OH HO ОН HO OH

 / \ / \ /
/ \ / \ /
\ / \ /

 H H С
H H С
/ C \ / \
 O О + 2H2O
O О + 2H2O
\ С / \ С /
|| ||
O O
3.2.1.1.Оборудование и реактивы:
- пробирки;
- пипетки;
- электроплитка;
- фталевый ангидрид;
- резорцин;
- серная кислота концентрированная;
- раствор едкого натрия(5-10 %-ный);
3.2.2.1 Проведение опыта:
а) взвесить 0.1-0.3 г фталевого ангидрида и поместить в пробирку;
б) в эту же пробирку добавить примерно вдвое большее количество резорцина и перемешать встряхивая;
в) к содержимому пробирки осторожно добавит 3-5 капель концентрированной серной кислоты;
г) смесь в пробирке нагреть до появления темно-красного окрашивания. Нагреть на электроплитке;
д) охладить содержимое пробирки и добавить в нее 5 мл воды;
е) в чистую пробирку внести 2-3 капли полученного раствора, добавить 1 мл раствора щелочи и разбавить большим количеством воды. Наблюдать за изменением окраски.
3.2.3 Образование аурина
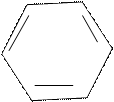
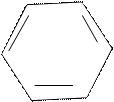
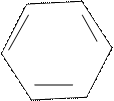
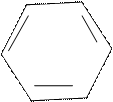
Аурин получается при конденсации щавелевой кислоты с фенолом в присутствии серной кислоты.
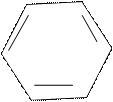
При нагревании в присутствии серной кислоты щавелевая кислота конденсируется с тремя молекулами фенола, отщепляя воду и окись углерода с образованием аурина.
 | |||
 | |||
 H-O- - H H - -OH
H-O- - H H - -OH

 -H . OH O =
-H . OH O =
 | . С = O +3H2O+CO
| . С = O +3H2O+CO
| =С
\ -OH
 H - C
H - C
H - -OH
||
O
3.2.3.1. Оборудование и реактивы:
-пробирки;
- пипетки;
- фенол;
- щавелевая кислота;
- серная кислота концентрированная;
- раствор едкого натрия(5-7 %-ный);
3.2.3.2 Проведение опыта:
а) взвесить 0,02-0,05г щавелевой кислоты и примерно вдвое больше фенола;
б) поместить оба реактива пробирку и перемешать встряхиванием;
в) добавить в пробирку 1-2 капли концентрированной серной кислоты;
г) осторожно нагреть пробирку со смесью до начала кипения и появления интенсивно желтой окраски;
д) охладить пробирку, добавить в нее 3-4 мл воды и встряхнуть. Наблюдать за появившейся окраской;
е) к полученному раствору добавить несколько капель раствора щелочи и наблюдать за изменением окраски;
3.3 Разложение мочевины (амида карбоминовой кислоты) при нагревании.
При нагревании выше температуры плавления мочевина распадается с выделением аммиака. При температуре 1500 -1600 С две молекулы мочевины отщепляют одну молекулу аммиака и дают хорошо растворимый в теплой воде биуреат:
 H2N-OO-NH2+H-NH-OO-NH2 H2N-CO-NH-CO-NH2+NH3
H2N-OO-NH2+H-NH-OO-NH2 H2N-CO-NH-CO-NH2+NH3
Для биуреата характерно образование в щелочном растворе с солями меди ярко-красного комплексного соединения, имеющиге в растворе едкого натра следующий состав:
(NH2CO NH CONH2)2 *2NaOH*Cu(OH)2
3.3.1 Оборудование и реактивы:
- пробирки;
- электроплитка;
- мочевина (карбомид);
- раствор едкого натрия(5-7 %-ный);
- раствор серной меди (1%-ный).
3.3.2 Проведение опыта:
а) взвесить 0,2-0,3г мочевины и поместить в сухую пробирку;
б) нагреть пробирку на электрической плитке;
в) наблюдать за происходящими изменениями: плавлением, выделением аммиака, затвердеванием;
г) охладить пробирку;
д) в охлажденную пробирку добавить 1-2мл теплой воды, взболтать и слить в другую пробирку;
е) к полученному мутному раствору добавить 3-4 капли раствора едкого натра до прозрачности. Затем добавить одну каплю раствора серной кислой меди и наблюдать изменение окраски (появляется красивое фиолетовое окрашивание).
