Беттік керілу беттегі когезия күшінің асимметриясының нәтижесі
Беттік керілу және су-ауа шекарасындағы адсорбция
Сұйықтардың беттік керілуі тамшылардың түзілуіне алып келеді және ол молекулалардың арасындағы тартылу күшіне байланыстыболады(16.1а-сурет). Бұл тартылу күштері будың сұйықтыққаконденсациялануын болдырады. Табиғаты бойынша бұл дисперсиялық, диполь-дипольдік және индукциялық әсерлесу, сонымен қатар сутектік байланыс. Сұйықтық көлемінде молекулалар барлық жағынан тартылыс күшінің әсеріне ұшырайды, беттегімолкула үшін бір бағытта бұндай тартылыс болмайды. Бұндай асимметрия беттікэнергияның пайда болуын болдырады және ол беттік керілутүрінде болады. Осылайша, беттік керілу сұйықтықтағы когезия күшінің тікелей салдарынан болады.
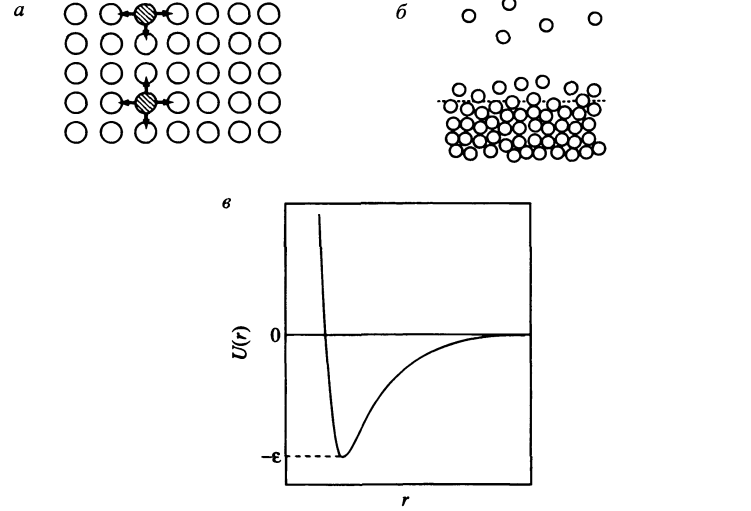
16.1-сурет. а-Беттік керілудің пайда болуы бетте орналасқан молекула үшін тартылыс күштерінің балансының бұзылуынан болады. б-Бетке жақын молекулалар бір-бірінен алыс қашықтықта орналасады, сондықтан жоғарырақ энергияға ие болады(16.1-суреттегі диаграмма). в-Молекулааралық әсерлесу энергиясының молекулааралық қашықтыққа тәуелділігі.
Беттік керілудің басқа молекулалық түсіндіруін сұйықтықтардың когезиялық энергиясымен корреляцияланатын 16.1б-сурет көрсетеді. Бетке жақын молекулалар бір-бірінен салыстырмалы түрде алыс орналасады және осылайша жоғары энергияға ие болады, энергияның қашықтыққа тәуелділігін көрсететін (16.1 в) диаграммадағыдай болады.
Кейбір жеке сұйықтықтардың беттік керілуінің мәндері 16.1-кестеде келтірілген. Беттік керілудің өлшем бірлігі дин/см немесе мН/м. Өте сәтті, бір жүйеден басқасына ауыстыру коэффициенті бірге тең және бұл жүйелердегі беттік керілуінің сандық мәндері бірдей болады. Өйткені сұйықтықтың беттік керілуі беттік энергиямен сәйкес(нақтырақ беттегі еркін беттік энергиямен), оны энергия бірлігімен өрнектеуге болады: эрг/см2 немесе мДж/м2. Бұл жағдайда да ауыстырукоэффициенті бірге тең. 16.1-кестеде көрсетілгендей беттік керілудің сұйықтықтың когезия энергиясымен өзара байланысы: когезия энергиясының ең төмен мәні диэтил эфирінде, ең жоғарғысы сынапта.
Өз кезегінде когезия энергиясы сұйықтықтағы әсер етуші дисперсиялық күшпен анықталады, мысалы, хлороформ мен бромоформның беттік керілуін салыстырсақ, соңғы молекуланың поляризациялануы жоғарырақ, сондықтан бромоформның беттік керілуі хлороформға қарағанда жоғарырақ. Беттік керілудің қалыпты алкандардың тізбегімен салыстырмасынан туындау себебінен, когезия энергиясы сұйықтықтардың еркін көлемімен байланысты, неғұрлым еркін көлем көп болса, соғұрлым когезия энергиясы мен беттік керілу аз болады.
Фазааралық керілу-бұл екі араласпайтын немесе жартылай араласқан сұйықтықтар шекарасындағы беттік керілу немесе беттік еркін энергия. Араласпаудың себебі әсер етуші әр сұйықтықтың молекулааралық когезия күшінің үлкен айырмашылығына байланысты (16.2-сурет). Сондықтан фазааралық бетте толықтырылмаған күш пайда болады.
16.1-ші кесте. 25 с0-та кейбір сұйықтықтар үшін беттік керілу(мН/м)
| Су | |
| Этанол | |
| Хлороформ | |
| Бромоформ | |
| н-Гексан | |
| н-Октан | |
| н-Додекан | |
| н-Гексадекан | |
| Диэтил эфирі | |
| Сынап |
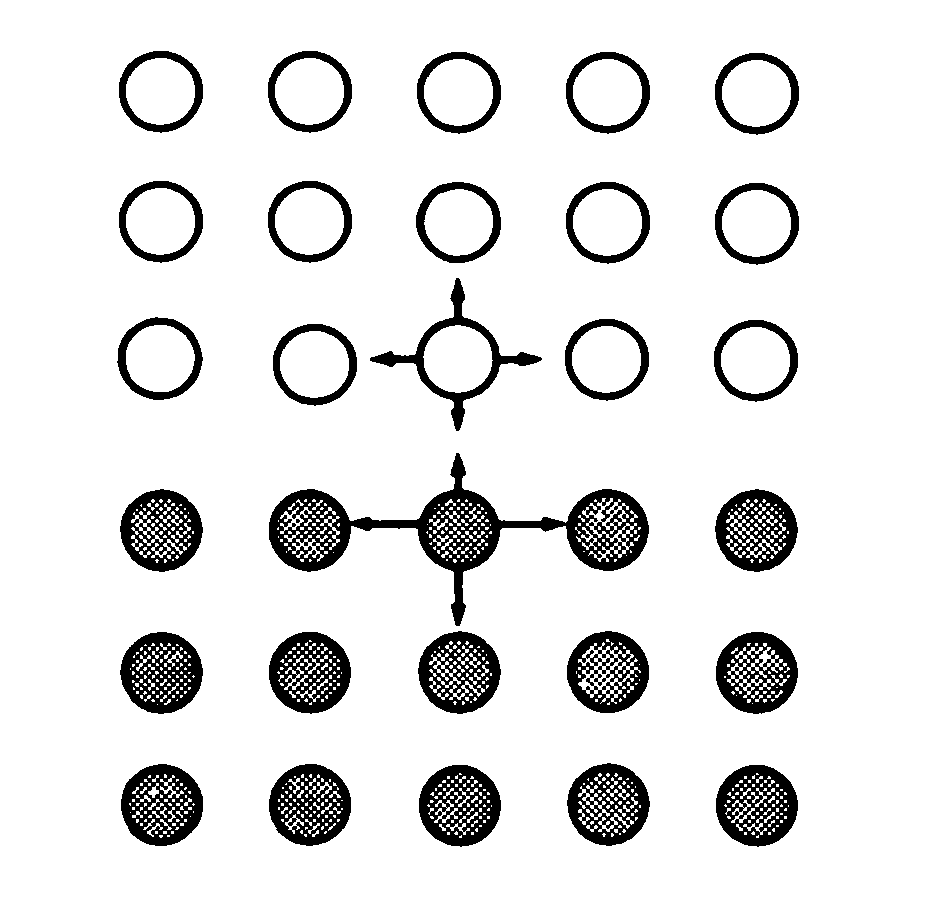
16.2-сурет. Беттік керілу сияқты фазааралық керілу фазалар шекарасында орналасқан молекулалардың тартылу күштерінің балансының бұзылуынан болады.
Когезия күшінің айырмашылығы жоғары болса, фазааралық керілуде жоғары болады. Сұйықтықтың когезия күшінің жеткілікті аз айырмашылығында бір-бірімен араласады. Реттелген ерітіндінің теориясында араласу немесе араласпаудың мәселесі жеткілікті түрде сипатталады(10- тараудан қараңыз).
Фазааралық керілудің өлшем бірлігі беттік керілудің өлшем бірлігімен бірдей. Фазааралық керілу сұйықтықтағы когезия күшінің айырмашылығына тәуелділігімен қатар екі сұйықтықтағы молекула аралық өзіндік әсерлесуіне де тәуелді. Мысалы, фазааралық керілу су-октан шекарасында 51мН/м-ге тең, ал су-октанол шекарасындағы фазааралық керілуі 8мН/м-ге тең. Октанолдың гидроксилдік тобы су фазалы жағына бағытталады және фазааралық керілудің төмендеуіне қатты әсер ететіні анық. Органикалық сұйықтық пен су арасындағы фазааралық керілуді төмендететін полярлы топтан және гидрофобтық бөліктен тұратын бетті-активтік заттар дәл осылай әсер етеді.
