Оценка погрешностей измерений
1.3 Общие положения. При выполнении измерений результат всегда получается с некоторой погрешностью. Погрешностью измерений называют величину 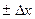 , определяемую из неравенства
, определяемую из неравенства
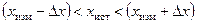 , , | (3.1) |
где 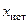 – истинное значение измеряемой величины,
– истинное значение измеряемой величины, 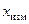 – измеренное значение величины.
– измеренное значение величины.
Поскольку точное значение 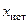 не известно, точно узнать
не известно, точно узнать 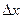 нельзя. Поэтому указывают интервал
нельзя. Поэтому указывают интервал 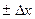 , внутри которого с определенной вероятностью, называемой доверительной вероятностью, расположено значение
, внутри которого с определенной вероятностью, называемой доверительной вероятностью, расположено значение 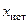 .
.
За лучшую оценку истинного значения результата измерений, принимают
среднее арифметическое ( 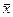 ) из всех величин
) из всех величин 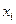 , полученных в процессе отдельных измерений, выполненных в одинаковых условиях:
, полученных в процессе отдельных измерений, выполненных в одинаковых условиях:
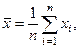 | (3.2) |
где n - число отдельных измерений.
Качество результатов измерений бывает удобно характеризовать не абсолютной погрешностью 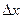 , а ее отношением к найденному значению измеряемой величины
, а ее отношением к найденному значению измеряемой величины 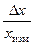 , которое называют относительной погрешностью a и выражают в процентах:
, которое называют относительной погрешностью a и выражают в процентах:
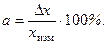 | (3.3) |
Погрешности измерений принято подразделять на систематические, случайные и грубые.
Грубые погрешности (промахи) появляются из-за недостатка внимания экспериментатора. Грубая погрешность обычно существенно превышает случайную.
3.2 Систематические погрешности. Систематические погрешности δ вызываются факторами, действующими одинаковым образом при многократном повторении одних и тех же измерений. Систематическую погрешность можно оценить, сравнив полученные результаты измерений с расчетным значением измеряемой величины, найденным на основании более точных экспериментальных данных, приведенных в справочнике.
3.3 Случайные погрешности. Случайные погрешности обязаны своим происхождением ряду причин, действие которых неодинаково в каждом опыте и не может быть учтено. Чаще всего случайные погрешности подчиняются нормальному закону распределения и могут быть оценены с помощью выборочной средней квадратической погрешности отдельного измерения ( 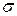 ):
):
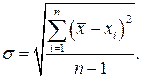 | (3.4) |
При большом числе измерений ( 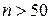 ) можно утверждать, что точное значение измеряемой величины
) можно утверждать, что точное значение измеряемой величины 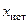 лежит в интервале
лежит в интервале 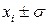 с доверительной вероятностью 0.68 или в интервале
с доверительной вероятностью 0.68 или в интервале 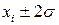 с вероятностью 0.95.
с вероятностью 0.95.
Если для нахождения определенного значения физической величины проводят несколько (n) параллельных измерений, а затем по формуле (3.2) рассчитывают их среднее значение 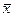 , то средняя квадратическая погрешность среднего арифметического
, то средняя квадратическая погрешность среднего арифметического 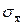 будет меньше погрешности отдельного измерения
будет меньше погрешности отдельного измерения 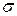 в
в 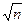 раз:
раз:
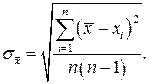 | (3.5) |
В предлагаемых лабораторных работах случайную погрешность измерений следует оценивать по формуле (3.4) на основании нескольких измерений ( 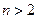 ), выполненных в одинаковых условиях.
), выполненных в одинаковых условиях.
3.4 Учет систематической и случайной погрешностей.
Часто бывает, что систематическая и случайная погрешности близки друг другу и обе определяют точность результата. Тогда можно найти суммарную погрешность 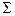 , полагая, что систематической погрешности
, полагая, что систематической погрешности 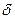 соответствует не бόльшая доверительная вероятность, чем утроенной среднеквадратической погрешности
соответствует не бόльшая доверительная вероятность, чем утроенной среднеквадратической погрешности 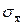 :
:
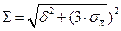 | (3.6) |
3.5 Погрешности косвенных измерений. Измерения подразделяются на прямые и косвенные. При прямом измерении искомую величину определяют непосредственно с помощью измерительного устройства, например находят высоту поднятия жидкости в манометре с помощью измерительной линейки. Результат косвенных измерений вычисляют по данным прямых измерений с помощью формул. Например, в работе № 1 средний тепловой эффект реакции 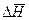 находят по опытным данным с помощью формулы (см. приложение 2)
находят по опытным данным с помощью формулы (см. приложение 2)
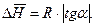
Погрешности прямых измерений могут быть найдены по соотношениям (3.4), (3.5) и (3.6). Если при косвенных измерениях интересующая нас величина 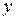 является известной функцией других величин
является известной функцией других величин 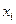 , которые измеряются непосредственно
, которые измеряются непосредственно
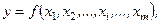 | (3.7) |
то ее абсолютную погрешность 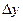 можно найти как
можно найти как
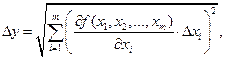 | (3.8) |
где 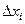 – абсолютная погрешность величины
– абсолютная погрешность величины 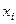 .
.
Лучшим приближением к истинному значению 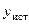 , как и в случае прямых измерений, считают среднее арифметическое значение
, как и в случае прямых измерений, считают среднее арифметическое значение 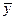 .
.
Среднеарифметическое значение измеряемой величины 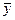 и погрешность результата можно вычислить двумя способами:
и погрешность результата можно вычислить двумя способами:
1. Вычислить 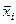 и, подставив эти значения в уравнение (3.7), найти
и, подставив эти значения в уравнение (3.7), найти 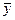 . Затем, определив погрешности
. Затем, определив погрешности 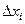 , по уравнению (3.8) найти
, по уравнению (3.8) найти 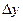 .
.
2. Для каждой группы результатов совместных измерений ( 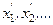 ); (
); ( 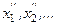 ), …; (
), …; ( 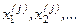 ); …; (
); …; ( 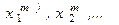 ) найти
) найти 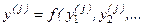 , затем рассчитать среднеарифметическое значение
, затем рассчитать среднеарифметическое значение 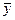 :
:
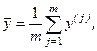 | (3.9) |
а погрешность определения величины вычислить обычным путем:
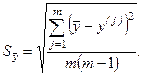 | (3.10) |
Систематическую погрешность косвенных измерений, как и прямых, можно оценить путем сравнения 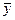 с результатами расчетов, выполненных с использованием справочных данных.
с результатами расчетов, выполненных с использованием справочных данных.
3.6 Требуемая точность вычислений. Целесообразное число значащих цифр в представлении результатов измерений. Во всех случаях нужно придерживаться следующего правила. Погрешность, получающаяся в результате вычислений, должна быть на порядок (т.е. в 10 раз) меньше суммарной погрешности измерений. При этом можно быть уверенным, что в процессе арифметических операций мы ощутимым образом не исказили результата.
Как окончательный результат вычислений записывают числа только с верными цифрами и одной сомнительной (так называется цифра того разряда, в котором содержится первая значащая цифра ошибки). Неверные цифры (правее сомнительной) отбрасывают с соблюдением правил округления. Следовательно, максимальная ошибка округления составит 5 единиц ближайшего отброшенного результата.
3.7 Оценка значимости изменения измеряемой величины. При выполнении предлагаемых лабораторных работ следует руководствоваться правилом: если изменение измеряемой величины превосходит утроенную среднеквадратичную погрешность, то это изменение значимо и является проявлением физико-химической закономерности.
В противном случае обычно считают, что измеряемая величина изменялась под действием случайных факторов.
ТЕРМОДИНАМИКА
| Работа № 1. | ИЗУЧЕНИЕ РАВНОВЕСИЯ РЕАКЦИИ ГАЗИФИКАЦИИ УГЛЕРОДА ЕГО ДИОКСИДОМ |
Целью работы является изучение температурной зависимости равновесного состава газовой фазы в системе «углерод-СО-СО2» при постоянном давлении. Изучаемая реакция газификации твердого углерода углекислым газом
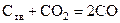 | (1) |
имеет большое значение в металлургической практике, осуществляется во многих металлургических агрегатах, например, в доменных печах и вагранках.
Выполнение данной работы требует знания раздела «Химическое равновесие», включая правило фаз Гиббса, понятие константы равновесия реакции, уравнения изобары и изотермы химической реакции.
Теоретическая часть
Равновесная система, состоящая из твердого углерода и смеси газов СО-СО2, обладает двумя степенями свободы, что следует из правила фаз Гиббса:
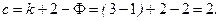 | (2) |
Бивариантность системы означает, что из трех параметров, однозначно характеризующих состояние системы (температура T, общее давление p, концентрация одного из двух компонентов газовой фазы, например %СО, только два могут варьироваться произвольно при неизменных числе и природе равновесных фаз. Если в качестве независимых параметров выбрать внешние, то есть температуру и общее давление, то состав газовой фазы может быть найден из уравнения связи параметров. Этим уравнением является выражение для константы равновесия реакции (1)
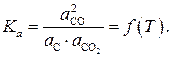 | (3) |
При небольших давлениях термодинамическая активность чистого конденсированного вещества равна единице ( 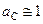 ), а состояние реальных газов можно приближенно описать уравнением Менделеева-Клапейрона, тогда активность компонента газовой смеси
), а состояние реальных газов можно приближенно описать уравнением Менделеева-Клапейрона, тогда активность компонента газовой смеси
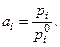 | (4) |
В этом соотношении 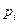 и
и 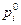 - соответственно парциальное давление компонента в данных условиях и в стандартном состоянии. Поскольку
- соответственно парциальное давление компонента в данных условиях и в стандартном состоянии. Поскольку 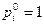 атм, то для компонентов системы (1)
атм, то для компонентов системы (1)
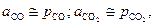 | (5) |
если давления измерены в атмосферах.
Следует обратить внимание на то обстоятельство, что активность газа как величина безразмерная, лишь численно равна его парциальному давлению, выраженному в атмосферах.
С учетом сказанного выражение (3) для константы равновесия принимает вид
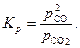 | (6) |
Поскольку парциальное давление газа связано с общим давлением p и его объемным процентом очевидным равенством
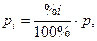 | (7) |
то уравнение (6) может быть представлено в виде
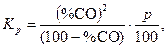 | (8) |
поскольку 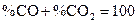 .
.
Константа равновесия химической реакции является функцией температуры, поэтому фиксация T и общего давления p однозначно определяет состав газовой фазы, что и подтверждается правилом фаз Гиббса (2).
Изучаемая реакция протекает с поглощением тепла ( 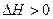 ), и в соответствии с уравнением изобары химической реакции
), и в соответствии с уравнением изобары химической реакции
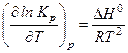 | (9) |
ее константа равновесия увеличивается при возрастании температуры. Поэтому с ростом температуры при постоянном давлении происходит увеличение содержания СО в равновесной газовой фазе, то есть происходит смещение равновесия в сторону образования продукта реакции. Сказанное иллюстрирует рис. 2, на котором приведена температурная зависимость равновесного содержания СО в газовой фазе при различных давлениях в системе. Из анализа уравнения (8) следует, что с увеличением общего давления p имеет место снижение концентрации монооксида углерода при постоянной температуре.
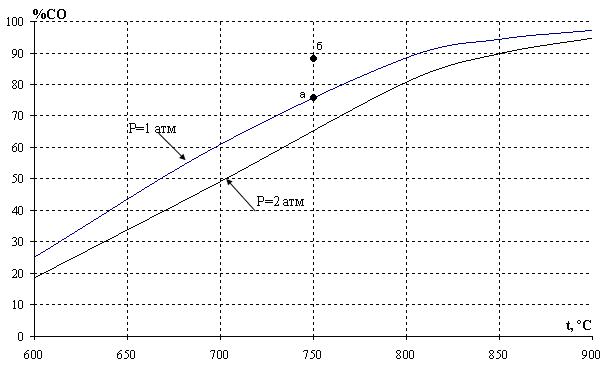
Рис.2. Зависимость равновесного содержания монооксида углерода от температуры при различных давлениях
Отмеченные выше закономерности находятся в соответствии с принципом смещения равновесия Ле-Шателье, согласно которому в равновесной системе при изменении внешних параметров развиваются процессы, стремящиеся ослабить внешнее воздействие. Так, росту температуры при постоянном давлении соответствует развитие эндотермического процесса, то есть прямой реакции (1), а при изотермическом увеличении внешнего давления в системе протекает обратный процесс ( 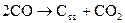 ), сопровождающийся уменьшением числа газовых молей.
), сопровождающийся уменьшением числа газовых молей.
Возможность протекания реакции при фиксированной температуре в заданных условиях определяют по уравнению изотермы. Так, для условий точки б (рис. 2) исходное содержание монооксида углерода (%СОб) превышает равновесное (%СОа), поэтому величина ∆G для реакции (1)
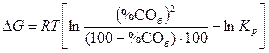 | (10) |
оказывается положительной. Другими словами, в условиях, характеризуемых параметрами точки «б», протекание прямой реакции невозможно, поэтому область, расположенная над изобарой pа, отвечает устойчивому существованию твердого углерода.
Расчет зависимости концентрации СО от температуры при постоянном давлении может быть проведен по методу Темкина-Шварцмана. Для этого необходимо рассчитать величину
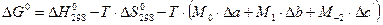 | (11) |
и по известному соотношению
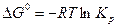 | (12) |
найти константу равновесия, а затем определить величину %СО при заданном p по уравнению (8). Необходимые термодинамические характеристики реагентов приведены в прил. 1.
Тепловой эффект реакции при заданной температуре рассчитывают по уравнению Кирхгофа
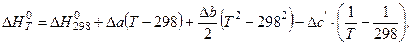 | (13) |
используя справочные данные о теплотах образования и теплоемкостях реагентов (прил. 1).
Среднюю величину теплового эффекта реакции в изученном интервале температур определяют графически по методике, приведенной в прил. 2.
