II. Частные способы получения альдегидов и кетонов
1) Реакция Фриделя-Крафтса
 | + | 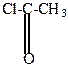 | AlCl3 безв.  -HCl -HCl | 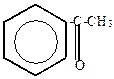 |
| хлористый ацетил (хлорангидрид уксусной кислоты) | ацетофенон |
Механизм – электрофильное замещение в ароматическом ядре.
2) Реакция Гаттермана – получение чисто ароматических альдегидов путем конденсации ароматических углеводородов с С=О.
 | 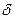 + + C=O + + C=O | +HCl  (+AlCl3) (+AlCl3) |  |
| толуол | п-толуиловый альдегид |
Механизм:
C=O + HCl  | 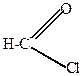 |
| хлористый формил |
Далее как в реакции Фриделя-Крафтса.
| CH3-C6H4-H + | 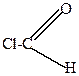 | AlCl3  -HCl -HCl | 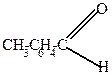 |
| толуол |
3) Реакция Тимана-Реймера
Конденсация фенолов с хлороформом в присутствии щелочей
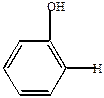 | + | 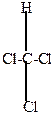 | + 3KOH  -3 KCl -H2O -3 KCl -H2O | 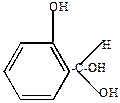 | -H2O  | 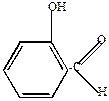 |
| салициловый альдегид |
Физические свойства
Ароматические альдегиды и кетоны – маслянистые жидкости или твердые вещества желтоватого цвета с приятным запахом.
Бензальдегид – миндаль, ацетофенол – черемуха. Мало растворимы в воде.
Химические свойства
Дают многие общие реакции альдегидов и кетонов.
1. Реакции нуклеофильного присоединения и замещения.
Активность ароматических карбонильных соединений в этих реакциях ниже активности карбонильных соединений жирного ряда, особенно низкой активностью обладают чисто ароматические кетоны.
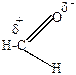 | > | 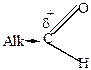 | > | 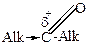 | > | 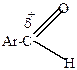 | > | 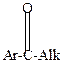 | > |
| > | 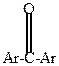 |
Объясняется это следующим. Все углеводородные радикалы обладают электронодонорными свойствами и уменьшают + 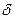 у карбонильного углерода, снижая его способность к восприятию атаки нуклеофильного реагента. В ароматических карбонильных соединениях
у карбонильного углерода, снижая его способность к восприятию атаки нуклеофильного реагента. В ароматических карбонильных соединениях 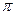 -электронные связи С=О находятся в сопряжении с
-электронные связи С=О находятся в сопряжении с 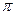 -электронами ядра, происходит более значительное уменьшение +
-электронами ядра, происходит более значительное уменьшение + 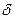 карбонильного углерода, особенно у чисто ароматических кетонов.
карбонильного углерода, особенно у чисто ароматических кетонов.
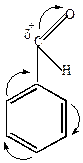
Ароматические альдегиды не дают реакций полимеризации, чисто ароматические кетоны не присоединяют NaHSO3, не присоединяют Mg-органические соединения, не вступают в реакции конденсации друг с другом.
Ароматические альдегиды и кетоны могут присоединять HCN, образовывать оксимы, гидразоны, фенилгидразоны и т.д.
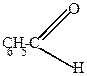 | + HCN  | 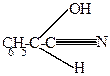 |
| циангидрин бензальдегида |
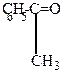 | + H2N-OH  H2O + H2O + | 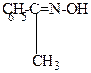 |
| ацетофенон | гидроксиламин | оксим ацетофенола |
2. Перегруппировка Бекмана
Наблюдается при действии на оксимы минеральных кислот.
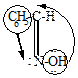 | +H+  |  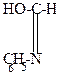 |  | 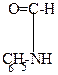 |
| синбензальдоксим | ||||
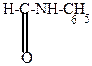 | ||||
| N-фенилформамид |
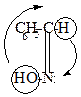 |  |  |  | 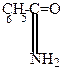 |
| антибензальдоксим | бензамид |
Перегруппировка Бекмана заключается в том, что к радикалу или Н, находящимся в транс-положении к группе ОН, присоединяется к азоту со стороны неподеленной пары, а ее место занимает группа ОН.
Продуктами, образующимися в результате перегруппировки Бекмана, являются замещенные амиды (син- и анти-изомеры образуют различные амиды).
II. Реакции конденсации.
Чисто ароматические не способны к реакциям альдольной конденсации между собой, но для них характерны особые виды реакций конденсации.
1) реакция Канниццаро (самоокисления-самовосстановления)
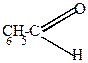 | + | 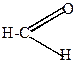 | t + KOH  C6H5-CH2OH + конц. C6H5-CH2OH + конц. | 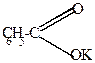 |
| бензальдегид | бензиловый спирт | калиевая соль бензойной кислоты |
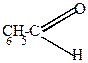 | + | 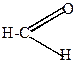 | + KOH  C6H5CH2OH + HCOOK C6H5CH2OH + HCOOK |
Механизм:
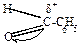 | |||||
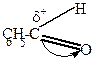 | + OH-  | 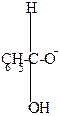 |  | 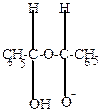 |  OH- + OH- + |
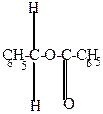 | KOH  омыление омыление |
Омыление
2) Бензоиновая конденсация
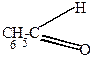 | + | 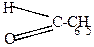 | (KCN)  | 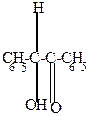 |
| бензоин |
Механизм:
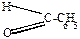 | ||||||
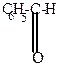 | + HCN-  | 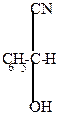 | -H+  | 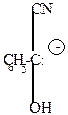 |  | 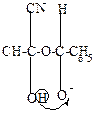 |
| протонная изомеризация | ||||||
 HCN + HCN + | 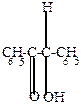 |
3) ароматические альдегиды и кетоны легко вступают в реакции конденсации с карбонилсодержащими соединениями жирного ряда, которые содержат подвижные атомы водорода в 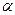 -положении к карбонильной группе.
-положении к карбонильной группе.
