Способы выражения концентрации раствора
Для решения задач этого раздела рекомендуем воспользоваться литературой 6, 8, 10, 16
Молекулярные или истинные растворы состоят из перемешанных друг с другом молекул растворенного вещества и среды. Растворы образуются при самопроизвольном распределении одного вещества в другом в результате диффузии. Но рассматривать раствор как смесь молекул различных веществ нельзя, так как свойства растворенного вещества и растворителя в общей системе раствора изменяются. Например, объем раствора никогда не равен сумме объемов растворителя и растворенного вещества. Полученная система однородна, так как за счет диффузии концентрация во всех микрообъемах выравнивается.
Раствором называется термодинамически устойчивая однофазная конденсированная система переменного состава, состоящая из двух или более компонентов, связанных между собой силами физического и химического взаимодействия.
Основным признаком, характеризующим раствор, является его гомогенность (однородность), как системы переменного состава, может состоять только из одной фазы: жидкой или твердой.
Количественный состав раствора определяется концентрацией, т.е. относительным содержанием каждого из компонентов, составляющих раствор.
Концентрацией называется содержание растворенного вещества в единице массы или объема раствора или растворителя.
Существуют различные способы численного выражения состава растворов: массовые, объемные и безразмерные.
Массовые концентрации:
Массовая доля 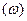 растворенного вещества – это отношение массы компонента, содержащегося в массе раствора.
растворенного вещества – это отношение массы компонента, содержащегося в массе раствора.
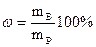 или
или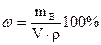 ,
,
где 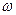 - массовая доля;
- массовая доля;
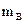 - масса растворенного вещества, г;
- масса растворенного вещества, г;
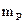 - масса раствора, г;
- масса раствора, г;
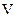 - объем раствора, мл;
- объем раствора, мл;
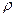 - плотность раствора, г/мл.
- плотность раствора, г/мл.
Пример 1. Кристаллогидрат нитрата железа (III) 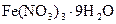 массой 60,6 г растворили в воде массой 250 г. Определите массовую долю нитрата железа (III) в полученном растворе.
массой 60,6 г растворили в воде массой 250 г. Определите массовую долю нитрата железа (III) в полученном растворе.
Решение. Масса полученного раствора составляет
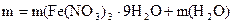 ;
;
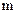 = 60,6+250= 310,6 (г)
= 60,6+250= 310,6 (г)
определяем количество вещества кристаллогидрата, растворенного в воде:
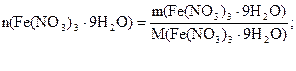
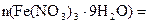 60,6/404=0,15 (моль)
60,6/404=0,15 (моль)
Из формулы кристаллогидрата следует:
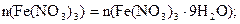
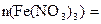 0,15 моль.
0,15 моль.
Находим массу нитрата железа (III), которая содержится в растворе:
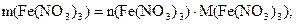
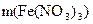 = 0,15 . 242=36,3 (г)
= 0,15 . 242=36,3 (г)
Рассчитываем массовую долю нитрата железа (III) в растворе:
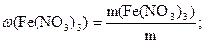
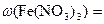 36,3/310,6 = 0,117 или 11,7%.
36,3/310,6 = 0,117 или 11,7%.
Моляльность ( 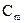 ) – число молей растворенного вещества в 1 кг растворителя.
) – число молей растворенного вещества в 1 кг растворителя.
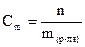 ,моль/кг,
,моль/кг,
где 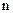 - число молей растворенного вещества;
- число молей растворенного вещества;
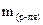 - масса растворителя, кг.
- масса растворителя, кг.
Пример 2. Раствор содержит 10 г 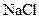 и 100 г воды. Вычислить моляльную концентрацию раствора.
и 100 г воды. Вычислить моляльную концентрацию раствора.
Решение. Определим число молей растворенного вещества:
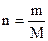 ;
; 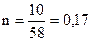 (моль),
(моль),
где 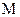 - молярная масса
- молярная масса 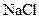 равная 58 г/моль
равная 58 г/моль
Моляльность раствора рассчитаем по формуле: 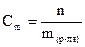
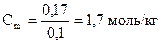
Объемные концентрации:
Молярная концентрация 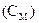 - число молей растворенного вещества в 1 л раствора.
- число молей растворенного вещества в 1 л раствора.
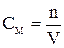 , моль/л
, моль/л
где n - число молей растворенного вещества, моль;
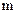 - масса растворенного вещества, г;
- масса растворенного вещества, г;
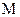 - молярная масса растворенного вещества г/моль;
- молярная масса растворенного вещества г/моль;
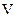 - объем раствора, л
- объем раствора, л
Пример 3. Определите молярную концентрацию раствора, полученную при растворении сульфата натрия массой 21,3 г в воде массой 150 г, если плотность полученного раствора равна 1,12 г/мл.
Решение. Определяем массу полученного раствора:
 ;
;
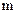 = 21,3 + 150 = 171,3 (г)
= 21,3 + 150 = 171,3 (г)
Вычисляем объем раствора:
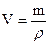 ;
; 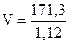 = 153 (мл) = 0,153 (л)
= 153 (мл) = 0,153 (л)
Количество вещества растворенного сульфата натрия равно
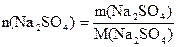 ;
; 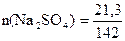 = 0,15 (моль)
= 0,15 (моль)
Рассчитываем молярную концентрацию раствора:
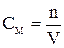 , моль/л
, моль/л
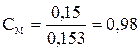 (моль/л)
(моль/л)
Молярная концентрация эквивалента 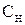 (нормальная концентрация) – количество вещества эквивалента, содержащегося в 1 л раствора.
(нормальная концентрация) – количество вещества эквивалента, содержащегося в 1 л раствора.
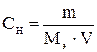 , моль/л
, моль/л
где Мэ = 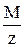 (см. раздел 1,1)
(см. раздел 1,1)
Пример 4. Какой объем 96%-ной кислоты плотностью 1,84 г/см3 потребуется для приготовления 5 л раствора с молярной концентрацией эквивалента равной 0,3 моль/л ?
Решение. Молярная масса эквивалента серной кислоты определяется по формуле:
 (г/моль)
(г/моль)
Находим массу серной кислоты для приготовления 3 л раствора с молярной концентрацией эквивалента 0,3 моль/л, если
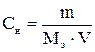 , выразим из этого выражения массу вещества (
, выразим из этого выражения массу вещества ( 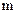 )
)
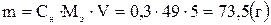
Масса 1  96%-ной кислоты 1,84 г. В этом растворе содержится
96%-ной кислоты 1,84 г. В этом растворе содержится
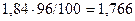 г серной кислоты.
г серной кислоты.
Следовательно, для приготовления 5 л раствора с молярной концентрацией эквивалента 0,3 моль/л надо взять 73,5:1,76=41,76  кислоты.
кислоты.
Пример 5. На нейтрализацию 50  раствора кислоты израсходовано 25
раствора кислоты израсходовано 25  раствора щелочи с молярной концентрацией эквивалента 0,5 моль/л. Чему равна молярная концентрация эквивалента кислоты ?
раствора щелочи с молярной концентрацией эквивалента 0,5 моль/л. Чему равна молярная концентрация эквивалента кислоты ?
Решение. Так как вещества взаимодействуют между собой в эквивалентных соотношениях, то растворы с равными концентрациями эквивалента реагируют в равных объемах. При разных концентрациях объемы растворов реагирующих веществ обратно пропорциональны их концентрациям, т.е.
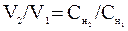 или
или 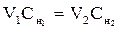
Подставим в последнее выражение известные данные:
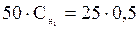 , откуда
, откуда 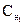 = 25.0,5/50 = 0,25 (моль/л)
= 25.0,5/50 = 0,25 (моль/л)
Безразмерные концентрации:
Мольная доля 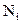 – отношение числа молей растворенного вещества к сумме числа молей всех компонентов раствора.
– отношение числа молей растворенного вещества к сумме числа молей всех компонентов раствора.
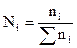
где 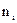 - число молей растворенного вещества.
- число молей растворенного вещества.
Титр 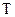 - масса вещества, содержащегося в 1 мл или в 1 см3 раствора.
- масса вещества, содержащегося в 1 мл или в 1 см3 раствора.
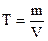 , г/мл.
, г/мл.
Титр связан с молярной концентрацией эквивалента соотношением:
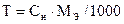
Контрольные вопросы:
101. Из 15 кг 18%-ного раствора при охлаждении выделилось 380 г соли. Чему равна массовая доля охлажденного раствора?
102. Чему равна молярная концентрация эквивалента 25%-ного раствора NaOH плотностью 1,328 г/  ? К 1 л этого раствора прибавили 6 л воды. Вычислите массовую долю полученного раствора.
? К 1 л этого раствора прибавили 6 л воды. Вычислите массовую долю полученного раствора.
103. Из 650 г 55%-ной серной кислоты выпариванием удалили 180 г воды. Чему равна массовая доля оставшегося раствора?
104. Вычислите молярную концентрацию эквивалента и молярную концентрацию 20,8%-ного раствора НNO3 плотностью 1,12 г/  . Сколько граммов кислоты содержится в 7 л этого раствора?
. Сколько граммов кислоты содержится в 7 л этого раствора?
105. Вычислите молярную, молярную концентрацию эквивалента и моляльную концентрации 26%-ного раствора хлорида алюминия плотностью 1,149 г/  .
.
106. Смешали 400 г 20%-ного раствора и 600 г 40%-ного раствора NaCl. Чему равна массовая доля полученного раствора?
107. Для осаждения в виде AgCl всего серебра, содержащегося в 100  раствора AgNO3, потребовалось 75
раствора AgNO3, потребовалось 75  раствора НСl с молярной концентрацией эквивалента 0,3 моль/л. Какова молярная концентрация эквивалента раствора AgNO3? Какая масса AgCl выпала в осадок?
раствора НСl с молярной концентрацией эквивалента 0,3 моль/л. Какова молярная концентрация эквивалента раствора AgNO3? Какая масса AgCl выпала в осадок?
108. Какая масса НNO3 содержалась в растворе, если на нейтрализацию его потребовалось 50  раствора NaOH с молярной концентрацией эквивалента 0,3 моль/л? Каков титр раствора NaOH?
раствора NaOH с молярной концентрацией эквивалента 0,3 моль/л? Каков титр раствора NaOH?
109. Смешали 30  10%-ного раствора HNO3 (пл. 1,056 г/
10%-ного раствора HNO3 (пл. 1,056 г/  ) и 150
) и 150  30%-ного раствора НNO3 (пл. 1,184 г/см3). Вычислите массовую долю полученного раствора.
30%-ного раствора НNO3 (пл. 1,184 г/см3). Вычислите массовую долю полученного раствора.
110. Какой объем 45%-ного раствора КОН (пл. 1,538 г/  ) требуется для приготовления 3л 4%-ного раствора (пл. 1,048 г/
) требуется для приготовления 3л 4%-ного раствора (пл. 1,048 г/  )?
)?
111. Какую массу 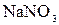 нужно растворить в 300 г воды, чтобы приготовить 20%-ный раствор?
нужно растворить в 300 г воды, чтобы приготовить 20%-ный раствор?
112. На нейтрализацию 26  раствора щелочи с молярной концентрацией эквивалента 0,15 моль/л требуется 167
раствора щелочи с молярной концентрацией эквивалента 0,15 моль/л требуется 167  раствора
раствора 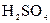 . Чему равны молярная концентрация эквивалента и титр раствора
. Чему равны молярная концентрация эквивалента и титр раствора 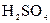 ?
?
113. Какой объем раствора кислоты с молярной концентрацией эквивалента 0,35 моль/л требуется для нейтрализации раствора, содержащего 0,42 г 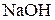 в 40
в 40  ?
?
114. На нейтрализацию 1 л раствора, содержащего 1,25 г 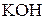 , требуется 50
, требуется 50  раствора кислоты. Вычислите молярную концентрацию эквивалента кислоты.
раствора кислоты. Вычислите молярную концентрацию эквивалента кислоты.
115. Какой объем 18,01%-ного раствора 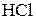 (пл. 1,100 г/
(пл. 1,100 г/  ) требуется для приготовления 1 л 8,17%-ного раствора (пл. 1,050 г/
) требуется для приготовления 1 л 8,17%-ного раствора (пл. 1,050 г/  ) ?
) ?
116. Какой объем 18%-ного раствора карбоната натрия (пл. 1,105 г/  ) требуется для приготовления 5 л 4%-ного раствора (пл. 1,02 г/
) требуется для приготовления 5 л 4%-ного раствора (пл. 1,02 г/  )?
)?
117. Сколько и какого вещества останется в избытке, если к 75  раствора Н2SO4 с молярной концентрацией эквивалента 0,5 моль/л прибавить 125
раствора Н2SO4 с молярной концентрацией эквивалента 0,5 моль/л прибавить 125  раствора
раствора 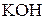 с молярной концентрацией эквивалента 0,3 моль/л?
с молярной концентрацией эквивалента 0,3 моль/л?
118. Смешали 278 г 62%-ного и 132 г 18%-ного раствора серной кислоты. Какова массовая доля полученного раствора?
119. К 4 л 10%-ного раствора 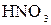 плотностью 1,054 г/
плотностью 1,054 г/  прибавили 3 л 2%-ного раствора той же кислоты плотностью 1,009 г/
прибавили 3 л 2%-ного раствора той же кислоты плотностью 1,009 г/  . Вычислите массовую долю и молярную концентрацию полученного раствора, объем которого равен 7 л.
. Вычислите массовую долю и молярную концентрацию полученного раствора, объем которого равен 7 л.
120. Вычислите молярную концентрацию и молярную концентрацию эквивалента 28%-ного раствора хлорида кальция плотностью 1,178 г/  .
.
Свойства растворов
Для решения задач этого раздела рекомендуем воспользоваться литературой 6, 8, 10, 16.
Важной физико-химической характеристикой твердых и жидких тел является давление пара, определяющее состояние равновесия между конденсированной и газообразной фазами. Чем выше давление пара, тем больше равновесие смещается в сторону процессов сублимации и испарения. Поэтому давление насыщенного пара над раствором используется для объяснения его поведения и свойств.
Понижение давления пара над раствором приводит к изменению температур кипения и замерзания по отношению к чистым растворителям. Известно, что жидкость кипит или кристаллизуется, когда давление ее насыщенного пара становится равным внешнему давлению или давлению насыщенного пара над твердой фазой, в которую она переходит. Раствор вследствие пониженного давления его паров труднее достигает точки кипения или точки кристаллизации. В связи с этим растворы кипят при более высоких и кристаллизуются при более низких температурах, чем чистые растворители. По закону Рауля: повышение температуры кипения или понижение температуры кристаллизации раствора прямо пропорционально моляльной концентрации растворенного вещества:
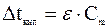 и
и 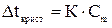
где 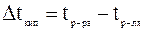
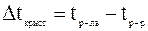
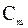 - моляльная концентрация, моль/г
- моляльная концентрация, моль/г
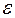 - эбуллиоскопическая константа
- эбуллиоскопическая константа
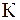 - криоскопическая константа.
- криоскопическая константа.
Закон Рауля имеет практическое значение - по изменению температуры кипения и кристаллизации определяют молекулярные веса неизвестных веществ. Преобразуем математические уравнения закона Рауля. Зная, что
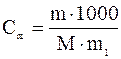
получим
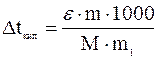 и
и 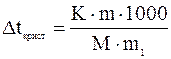 .
.
где М – молярная масса вещества;
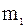 - масса растворителя, г;
- масса растворителя, г;
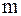 - масса растворенного вещества, г.
- масса растворенного вещества, г.
Пример 1.Раствор, содержащий 32,5 г вещества в 250 г уксусной кислоты, кипит на 2˚C выше, чем чистая уксусная кислота. Вычислить молекулярную массу растворенного вещества. Эбуллиоскопическая константа уксусной кислоты 2,53˚C.
Решение. Из уравнения
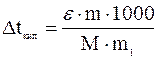
выразим молекулярную массу растворенного вещества:
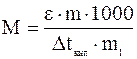 =
=  =164,5 г/моль
=164,5 г/моль
Таким образом, молекулярная масса вещества равна 164,5.
Пример 2. Вычислить температуру замерзания раствора, содержащего 9,0 г глюкозы 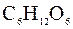 в 100 г воды.
в 100 г воды.
Решение. Согласно уравнению
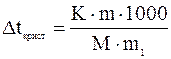
рассчитаем изменение температуры замерзания.
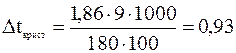 ˚C
˚C
Вычитая 0,93 из температуры замерзания воды, находим понижение температуры замерзания раствора: 0-0,93=-0,93˚C
Контрольные вопросы:
121. Вычислите массовую долю водного раствора глицерина С3Н5(ОН)3, зная, что этот раствор кипит при 100,39˚C. Эбуллиоскопическая константа воды 0,52˚C.
122.Раствор, содержащий 55,4 г неэлектролита в воде объемом 2,5 л, кипит при 100,16˚С. Эбуллиоскопическая константа воды 0,52˚C. Вычислите молекулярную массу неэлектролита.
123.Вычислите молекулярную массу камфоры, зная, что раствор, содержащий 0,04 г этого вещества и бензола массой 20 г, кристаллизуется при температуре на 0,067˚С ниже, чем чистый бензол. Криоскопическая константа бензола 5,1˚C.
124. Для раствора, состоящего из 0,94 г фенола ( 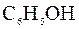 ) и 50 г этилового спирта, повышение температуры кипения составляет 0,232˚С. Эбуллиоскопическая константа этилового спирта 1,16˚C. Вычислите молярную массу фенола.
) и 50 г этилового спирта, повышение температуры кипения составляет 0,232˚С. Эбуллиоскопическая константа этилового спирта 1,16˚C. Вычислите молярную массу фенола.
125. При растворении хлороформа массой 15 г в диэтиловом эфире массой 400 г температура кипения последнего повысилась на 0,635˚С. Вычислите значения молярной массы для хлороформа. Эбуллиоскопическая константа эфира 2,02˚C.
126. При какой температуре должен кипеть раствор, содержащий растворенный неэлектролит количеством вещества 0,062 моль в воде объемом 200 мл?
127. Раствор, содержащий фосфор и бензол, масса которых соответственно равна 0,1155 и 19,03 г, замерзает при 5,150С. Чистый бензол замерзает при 5,4˚С. Криоскопическая константа для бензола 5,1˚C. Найдите молекулярную формулу раствора.
128. Найдите молекулярную формулу серы, зная, что температура кипения чистого бензола на 0,081˚С ниже температуры кипения раствора, содержащего серу массой 0,81г в бензоле массой 100г. Эбулиоскопическая константа бензола 2,57˚C.
129.Раствор, состоящий из 9,2 г иода и 100 метилового спирта, закипает при 65˚С. Сколько атомов входит в состав молекулы иода, находящегося в растворенном состоянии? Температура кипения спирта 64,7˚С, а его эбуллиоскопическая константа Кэ = 0,84˚С.
130. Раствор, содержащий ацетон массой 100 г и глицерин С3Н8О3 массой 2,67 г кипит при 56,73˚С. Температура кипения ацетона 56,3˚С. Вычислите эбуллиоскопическую константу ацетона.
131. Раствор, содержащий глицерин массой 13,8 г в воде объемом 1 л, замерзает при -0,279˚С. Найдите молярную массу глицерина. Криоскопическая константа воды 1,86˚C.
132. Раствор, содержащий 1 г растворенного вещества в 50 г воды, замерзает при -0,81˚С. Найдите молярную массу растворенного вещества. Криоскопическая константа воды 1,86˚C.
133. Насколько градусов понизится температура замерзания, если в бензоле массой 100 г растворить нафталин ( 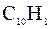 ) массой 4 г. Криоскопическая константа бензола 5,1˚C.
) массой 4 г. Криоскопическая константа бензола 5,1˚C.
134. Насколько градусов повысится температура кипения, если в воде объемом 1 л растворить глюкозу массой 90 г? Эбуллиоскопическая константа воды 0,52˚C.
135. Какую массу глюкозы 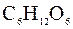 необходимо растворить в воде объемом 100 мл, чтобы температура понизилась на 1˚С. Криоскопическая константа воды 1,86˚C.
необходимо растворить в воде объемом 100 мл, чтобы температура понизилась на 1˚С. Криоскопическая константа воды 1,86˚C.
136. Какую массу глюкозы 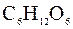 необходимо растворить в 100 мл воды, чтобы температура кипения повысилась на 3˚С. Эбуллиоскопическая константа воды 0,52˚C.
необходимо растворить в 100 мл воды, чтобы температура кипения повысилась на 3˚С. Эбуллиоскопическая константа воды 0,52˚C.
137. Вычислите массовую долю водного раствора метанола СН3ОН, температура кристаллизации которого - 2,79˚С. Криоскопическая константа воды 1,86˚C.
138.При какой температуре замерзает раствор, содержащий 14,4 г глюкозы 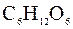 в 200 мл воды. Криоскопическая константа воды 1,86˚C.
в 200 мл воды. Криоскопическая константа воды 1,86˚C.
139. При какой температуре замерзает раствор, содержащий 3 г мочевины в 200 мл воды. Криоскопическая константа воды 1,86˚C.
140. При какой температуре кипят и замерзают водные растворы неэлектролитов, моляльность которых равна 1 моль/кг. Криоскопическая константа воды 1,86˚C. Эбуллиоскопическая константа воды 0,52˚C.
1.8. Ионно – молекулярные (ионные) реакции обмена
Для решения задач этого раздела рекомендуем воспользоваться литературой 4, 6, 8, 14 и таблицей 7.

Электролиты – вещества, которые в растворенном или расплавленном состоянии проводят электрический ток. При растворении в воде или других полярных растворителях электролиты подвергаются электролитической диссоциации, т.е. в большей или меньшей степени распадаются на положительно и отрицательно заряженные ионы – катионы и анионы.
Уравнения диссоциации обычно записываются следующим образом:
НСl = Н+ + С1- КОН = К+ + ОН-
К3РО4 = 3К+ + РО43-
Нужно иметь ввиду, что эти уравнения только приблизительно отображают подлинный процесс диссоциации, поскольку не показано участие молекул растворителя, без которого сама диссоциация невозможна.
Электролиты практически полностью диссоциирующие на ионы называются сильными электролитами. К ним относятся большинство неорганических солей, гидроксиды щелочных металлов, растворимые гидроксиды щелочноземельных металлов, некоторые минеральные кислоты, например, H2SO4, HNO3, HCl, HI, HBr.
Электролиты, диссоциирующие в растворах не полностью, называются слабыми электролитами. К ним относятся почти все органические кислоты, некоторые минеральные кислоты, например,H2CO3, H2S, HNO2, H2SO3, HCN, многие основания металлов, а также NH4OH.
В растворах слабых электролитов устанавливается равновесие между недиссоциированными молекулами и продуктами их диссоциации – ионами. В этом случае можно применить законы химического равновесия и записать выражение константы равновесия. Например, в водном растворе уксусной кислоты устанавливается равновесие:
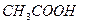 ⇄
⇄ 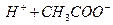
которое характеризуется константой равновесия (константа диссоциации):
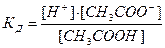 .
.
Величина 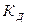 зависит от природы электролита и растворителя, от температуры, но не зависит от концентрации раствора. Она характеризует способность данного электролита распадаться на ионы: чем выше
зависит от природы электролита и растворителя, от температуры, но не зависит от концентрации раствора. Она характеризует способность данного электролита распадаться на ионы: чем выше 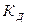 , тем легче электролит диссоциирует.
, тем легче электролит диссоциирует.
В табл. 1 приведены значения констант диссоциации некоторых слабых электролитов.
Количественно процесс электролитической диссоциации выражают с помощью степени диссоциации, т.е. доли молекул, распавшихся на ионы. Её представляют в процентах или в долях единицы:
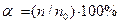 ,
,
где n – число молекул, распавшихся на ионы, n0 – общее число растворенных молекул.
Ионно-молекулярные, или просто ионные, уравнения реакций обмена отражают состояние электролита в растворе. В этих уравнениях сильные растворимые электролиты, поскольку они полностью диссоциированы, записывают в виде ионов, а слабые электролиты, малорастворимые и газообразные вещества записывают в молекулярной форме.
В ионно-молекулярном уравнении одинаковые ионы из обеих его частей исключаются. При составлении ионно-молекулярных уравнений следует помнить, что сумма электрических зарядов в левой части уравнения должна быть равна сумме электрических зарядов в правой части уравнения.
Пример 1. Написать ионно-молекулярные уравнения реакций взаимодействия между водными растворами следующих веществ: а)HCl и NaOH; б) Pb(NO3)2 и Na2S; в) NaClO и HNO3; г) K2CO3 и H2SO4; д) CH3COOH и NaOH.
Решение: запишем уравнения взаимодействия указанных веществ в молекулярном виде:
а) HCl + NaOH = NaCl + H2O
б) Pb(NO3)2 + Na2S = PbS 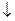 + 2NaNO3
+ 2NaNO3
в) NaClO + HNO3 = NaNO3 + HClO
г) K2CO3 + H2SO4 = K2SO4 + CO2 + H2O
д) CH3COOH + NaOH ⇄ CH3COONa + H2O
Отметим, что взаимодействие этих веществ возможно, ибо в результате происходит связывание ионов с образованием слабых электролитов (H2O, HClO), осадка (PbS), газа (CO2).
В реакции (д) имеются два слабых электролита - CH3COOH и H2O, но так как реакции идут в сторону большего связывания ионов и вода – более слабый электролит, чем уксусная кислота, то равновесие реакции смещено в сторону образования воды. Исключив одинаковые ионы из обеих частей равенства: а) Na+ и Cl 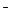 ; б) Na+ и NO
; б) Na+ и NO 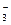 ; в) Na+ и NO
; в) Na+ и NO 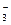 ; г) K+ и SO
; г) K+ и SO 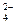 ; д) Na+, получим ионно-молекулярные уравнения реакций, которым соответствуют следующие ионно-молекулярные реакции:
; д) Na+, получим ионно-молекулярные уравнения реакций, которым соответствуют следующие ионно-молекулярные реакции:
а) H+ + OH 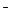 = H2O
= H2O
б) Pb2+ + S 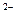 = PbS
= PbS
в) ClO 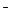 + H+ = HClO
+ H+ = HClO
г) CO 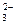 +2H+ = CO2 + H2O
+2H+ = CO2 + H2O
д) CH3COOH + OH 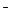 = CH3COO
= CH3COO 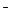 + H2O
+ H2O
Пример 2.Составьте молекулярные уравнения реакций, которым соответствуют следующие ионно-молекулярные уравнения:
а) SO 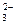 + 2H+ = SO2 + Н2О
+ 2H+ = SO2 + Н2О
б) Pb2+ + CrO 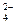 = PbCrO4
= PbCrO4
в) HCO 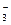 + OH
+ OH 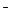 = CO
= CO 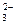 + H2O
+ H2O
г) ZnOH+ + H+ = Zn 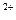 + H2O
+ H2O
Решение: В левой части данных ионно-молекулярных уравнений указаны свободные ионы, которые образуются при диссоциации растворимых сильных электролитов, следовательно, при составлении молекулярных уравнений следует исходить из соответствующих растворимых сильных электролитов. Например:
а) Na2SO3 + 2HCl = 2NaCl + SO2 + H2O
б) Pb(NO3)2 + K2CrO4 = PbCrO4 + 2KNO3
в) KHCO3 + KOH = K2CO3 + H2O
г) ZnOHCl + HCl = ZnCl2 + H2O
Контрольные вопросы:
| 141.Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) хлоридом бария и сульфатом алюминия; б) фосфорной кислотой и нитратом кальция; в) ацетатом калия и серной кислотой. | ||
| 142. Какое из веществ: KCl, FeSO4, Zn(OH)2, NaHCO3 - взаимодействует с раствором гидроксида натрия? Запишите молекулярные и ионно-молекулярные уравнения этих реакций. | ||
143. Составьте по три молекулярных уравнения реакций, которые выражаются ионно-молекулярными уравнениями: а) Zn2+ + H2S = ZnS + 2H+ б) Н+ + ОН- = Н2 О в) CO 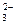 +2H+ = CO2 + H2O +2H+ = CO2 + H2O | ||
| 144. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) FeCl3 и КОН; б) MnSO4 и (NH4)2S; в) CaСО3 и НCl. | ||
145.Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями: а) Pb2+ + H2S = PbS + 2H+ б) Н б) СО 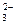 + 2Н+ = H2 O + CO2 в) Ba2+ + SO + 2Н+ = H2 O + CO2 в) Ba2+ + SO 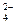 = BaSO4 = BaSO4 | ||
146.Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями: а) СаСО3 + 2Н+ = Са2+ + Н2О + СО2 б) Zn(ОН)2 + 2ОН- = ZnО  + 2Н2О в) Ag+ + Cl- = AgCl + 2Н2О в) Ag+ + Cl- = AgCl | ||
| 147.Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями: а) Cu(ОН)2 + 2Н+ = Cu2+ + 2Н2О б) Fe2+ + 2ОН- = Fe(ОН)2 в) Н+ + OH- = Н2O | ||
| 148.Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) Sn(ОН)2 и NaOH; б) Fe(ОН)2 и Н2SO4; в) CuOHCl и HCl. | ||
| 149. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) K2CO3 и НNO3; б) Zn(ОН)2 и NaOH; в) Ва(ОН)2 и NiСl2. | ||
| 150. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) Na2CO3 и MnSO4; б) К3PO4 и Al2(SO4)3; в) Pb(OH)2 и NaОН. | ||
| 151. Составьте молекулярные уравнения реакций взаимодействия в растворах между а) FeSO4 и Н2S; б) (NH4)2СО3 и НNO3; в) СrCl3 и NaOH. | ||
| 152. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между а) Zn(OH)2 и НСl; б) МgSO4 и КОН; в) NH4 Сl и NaОН. | ||
| 153.Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) АgNO3 и К3PО4; б) Рb(NO3)2 и КСl; в) СuSO4 и Na2S. | ||
154. Составьте по три молекулярных уравнения реакций, которые выражаются ионно-молекулярными уравнениями: а) Fe2+ + S2- 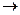 FeS б) SiO32- + 2Н+ FeS б) SiO32- + 2Н+ 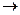 Н2SiO3 Н2SiO3 | ||
| 155.Какое из веществ: NaНСО3, СН3СООН, MnSO4, К2S - взаимодействует с раствором серной кислоты? Запишите молекулярные и ионно-молекулярные уравнения этих реакций. | ||
| 156. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) NaНСО3 и НNO3; б) Аl(ОН)3 и NaOH; в) ВаСl2 и AgNO3. | ||
| 157.Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) H3PO4 и Ва(ОН)2; б) CrCl3 и NH4OH; в) Na2SiO3 и НСl. | ||
| 158.Какое из веществ: Zn(OH)2, НСl, Fe(OH)2 - будет взаимодействовать с гидроксидом калия? Выразите эти реакции молекулярными и ионно-молекулярными уравнениями. | ||
| 159.Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) хлоридом бария и сульфатом алюминия; б) фосфорной кислотой и нитратом кальция; в) ацетатом калия и серной кислотой. | ||
| 160. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) сульфидом натрия и соляной кислотой; б) сульфатом железа (II) и сульфидом калия; в) иодидом натрия и нитратом свинца. | ||
Гидролиз солей
Для решения задач этого раздела рекомендуем воспользоваться литературой 4, 6, 8, 14 и таблицами 4,5.
Вода является очень слабым электролитом, степень ее диссоциации равна 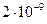 . Полярные молекулы воды в очень небольшой степени диссоциируют на ионы:
. Полярные молекулы воды в очень небольшой степени диссоциируют на ионы:
Н2О = Н+ + ОН- ,
или с учетом гидратации:
2Н2О = Н3О+ + ОН-
На основании законов химического равновесия получим выражение константы диссоциации воды:
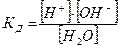 ,
,
отсюда
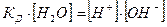
По данным измерения электропроводности при температуре 18 0С 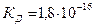 , а молярная концентрация чистой воды
, а молярная концентрация чистой воды 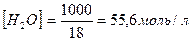 . Получаем значение
. Получаем значение 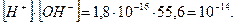 Это произведение
Это произведение 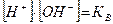 называется ионным произведением воды.
называется ионным произведением воды.
Если 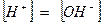 , то концентрация каждого из ионов воды равна
, то концентрация каждого из ионов воды равна 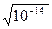 =10-7 моль/л. Ионы водорода являются носителем кислотных свойств, а гидроксид-ионы – щелочных, следовательно, при равенстве их концентраций реакция среды раствора является нейтральной.
=10-7 моль/л. Ионы водорода являются носителем кислотных свойств, а гидроксид-ионы – щелочных, следовательно, при равенстве их концентраций реакция среды раствора является нейтральной.
При 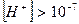 моль/л реакция среды будет кислой, а при
моль/л реакция среды будет кислой, а при 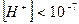 - щелочной. Таким образом, концентрация ионов водорода является мерой его кислотности или щелочности.
- щелочной. Таким образом, концентрация ионов водорода является мерой его кислотности или щелочности.
Более удобен способ выражения реакции среды с помощью отрицательного десятичного логарифма концентрации водородных ионов, именуемого водородным показателем рН:
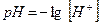
В нейтральной среде рН =7; в кислой – рН < 7; в щелочной – рН > 7.
Растворениеразличных веществ в воде часто сопровождается химическим взаимодействием обменного характера. Процессы подобного типа объединяют под общим названием гидролиза. Гидролиз – это химический процесс обменного разложения вещества с водой.Гидролиз солей – частный случай взаимодействия растворенных солей с водой, где их составные части соединяются с составными частями воды с образованием соответствующего слабого электролита.
Реакцию гидролиза соли можно представить общим уравнением:
МА + НОН ⇄ МОН + НА,
