Предельные одноатомные спирты.
СТРОЕНИЕ ГИДРОКСИЛЬНОЙ
ГРУППЫ.
Связи О–Н и С–О – полярные ковалентные.
Это следует из различий в электроотрицательности кислорода (ЭО = 3,5), водорода (ЭО = 2,1) и углерода (ЭО = 2,4).
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:

Разрыв таких связей происходит преимущественно по ионному механизму.
 Атому кислорода в спиртах свойственна sp3-гибридизация.В образовании его связей с атомами C и H участвуют две sp3-гибридные орбитали, валентный угол C–О–H близок к тетраэдрическому.
Атому кислорода в спиртах свойственна sp3-гибридизация.В образовании его связей с атомами C и H участвуют две sp3-гибридные орбитали, валентный угол C–О–H близок к тетраэдрическому.
В фенолах под влиянием π-электронной системы бензольного кольца для атома кислорода предпочтительней sp2-гибридизация. При этом одна из неподеленных электронных пар находится на негибридной р-орбитали и может участвовать в сопряжении с ароматической π-системой.

ЭЛЕКТРОННЫЕ ЭФФЕКТЫ ОН-ГРУППЫ.
Гидроксигруппа проявляет отрицательный индуктивный эффект (–I-эффект) по отношению к углеводородному радикалу и в спиртах выступает как электроноакцепторный заместитель.
В фенолах, где ОН-группа находится при sp2-гибридном атоме углерода, кроме того, она проявляет положительный мезомерный эффект (+M-эффект), предоставляя неподеленную электронную пару кислорода в π-систему сопряжения бензольного кольца.
ВОДОРОДНЫЕ СВЯЗИ И ФИЗИЧЕСКИЕ СВОЙСТВА
Следствием полярности связи О–Н и наличия неподеленных пар электронов на атоме кислорода является способность гидроксисоединений к образованию водородных связей:
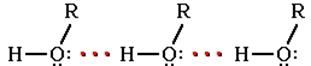
Ассоциация молекул ROH
Это объясняет, почему даже низшие спирты - жидкости с относительно высокой температурой кипения (т. кип. метанола +64,5оС). При переходе от одноатомных к многоатомным спиртам или фенолам температуры кипения и плавления резко возрастают.
Образование водородных связей с молекулами воды способствует растворимости гидроксисоединений в воде:
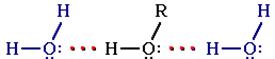
Гидратация молекул ROH
Метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин смешиваются с водой в любых соотношениях. Растворимость фенола в воде ограничена.
СПИРТЫ - соединения, содержащие помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Классификация спиртов.
1.По числу гидроксильных групп:
· одноатомные (одна группа -ОН).
Общая формула CnH2n+1–OH или CnH2n+2O.
· многоатомные (две и более групп -ОН).
Общая формула CnH2n+2Om.
Современное название многоатомных спиртов - полиолы (диолы, триолы и т.д).
Двухатомный спирт – этиленгликоль (этандиол) СH2–CH2
│ │
ОН ОН
Трехатомный спирт – глицерин (пропантриол-1,2,3) СH2–СН–CH2
│ │ │
ОН ОН ОН
2. В зависимости от того, с каким атомом углерода (первичным, вторичным или третичным)связана гидроксигруппа:

3. По строению радикалов, связанных с атомом кислорода:
· предельные, или алканолы (например, СH3CH2–OH)
· непредельные, или алкенолы (CH2=CH–CH2–OH)
· ароматические (C6H5CH2–OH).
НОМЕНКЛАТУРА СПИРТОВ.
В названии появляется суффикс: -«ОЛ» и номер атома углерода, к которому он присоединен.
Нумерация ведется от ближайшего к ОН-группе конца цепи.
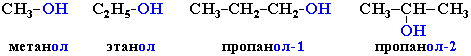
Приведенные выше соединения называют:
метиловый спирт, этиловый спирт, н-пропиловый спирт, изопропиловый спирт.
Метиловый спирт (метанол) CH3-OH

Этиловый спирт (этанол) CH3CH2-OH
В названиях многоатомных спиртов (полиолов) положение и число гидроксильных групп указывают соответствующими цифрами и суффиксами -диол (две ОН-группы), -триол (три ОН-группы) и т.д. Например:

ИЗОМЕРИЯ СПИРТОВ.
Для спиртов характерна структурная изомерия:
*изомерия положения ОН-группы (начиная с С3);

*углеродного скелета (начиная с С4);
например, формуле C4H9OH соответствует 4 структурных изомера:

*межклассовая изомерия с простыми эфирами
(например, этиловый спирт СН3CH2–OH и диметиловый эфир CH3–O–CH3).
ПРЕДЕЛЬНЫЕ ОДНОАТОМНЫЕ СПИРТЫ.
Получение.
| 1. Щелочной гидролиз галогенпроизводных алканов. | CH3–Br + NaOH(водн.) ->CH3–OH +NaBr |
| 2. Гидратация алкенов: присоединение воды к несимметричным алкенам идет поправилу Марковникова с образованием вторичных и третичных спиртов. | CH2=CH2 + H2O –(H+)->CH3CH2OH CH3–CH=CH2 + H2O–(H+)->CH3CHCH3 / ОН ОН / CH3–C=CH2 + H2O –(H+)->CH3 –C–СH3 ô ô СН3 СН3 |
| 3.Восстановление карбонильных соединений. | При гидрировании альдегидов получаются первичные спирты: СН3-С=О + Н2 -(t,kat)-> CH3-CH2-OH ô этанол Н При гидрировании кетонов образуются вторичные спирты: СН3-С=О + Н2 -(t,kat)-> CH3-CH-OH ô ô СН3 СН3 пропанол-2 |
| 4. Гидролиз сложных эфиров. | CH3-C=O + H2O –(H2SO4,t)-> │ OC2H5 -> CH3-COOH + C2H5OH этанол |
| 5. Получение метанола из синтез-газа. | Каталитический синтез метанола из монооксида углерода и водорода CO + 2 H2 ⇄ CH3OH |
| 6. Получение этанола. | Спиртовое брожение глюкозы. С6Н12О6 –(фермент)-> 2С2Н5ОН + 2СО2 |
ХИМИЧЕСКИЕ СВОЙСТВА.
В химических реакциях гидроксисоединений возможно разрушение одной из двух связей:
- С–ОН с замещением или отщеплением ОН-группы
- О–Н с замещением водорода.
| Реакции по связи О – Н | Реакционная способность одноатомных спиртов в реакциях по связи О–Н: CH3OH > первичные > вторичные > третичные. |
| 1.Одноатомные спирты реагируют с активными металлами (Na, K, Mg), образуя соли - алкоголяты (алкоксиды): | 2R–OH + 2Na ->2RO–Na+ + H2 2C2H5OH + 2K ->2C2H5O–K+ + H2 этилат калия (алкоголят) Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла: C2H5OК + H2O ->C2H5OH + КOH |
| 2.Окисление одноатомных спиртов. | 1) Горение: 2CH3OH + 3O2 ->2CO2 + 4H2O 2) Окисление первичных спиртов до альдегидов: Реагенты – CuO (to), O2 (Cu, to), а также дегидрирование при нагревании над медной сеткой. СН3-СН2-ОН +СuO –(to)-> CH3-C=O + Cu + H2O этанол ô этаналь H 2*) Дегидрирование: СН3-СН2-СН2-ОН –(Сu, to)-> CH3-CH2-C=O + H2 пропанол ô пропаналь H 3) Окисление подкисленным раствором перманганата калия приводит к образованию карбоновых кислот: СН3-СН2-ОН + KMnO4 + H2SO4 -> CH3-COOH + MnSO4 + K2SO4 +H2O уксусная кислота 4) При окислении вторичных спиртов любым окислителем образуются кетоны. 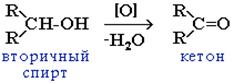 |
| Реакции по связи С–О | Реакционная способность одноатомных спиртов в реакциях по связи С–О: третичные > вторичные > первичные > CH3OH |
| 1. Реакции замещения ОН на галоген: происходит в реакции с галогеноводородами в присутствии сильной кислоты (конц. H2SO4). | 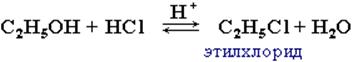 |
| 2.Реакции дегидратации спиртов: 1)Внутримолекулярная дегидратация: образуются алкены. | Внутримолекулярная дегидратация спиртов с образованием алкенов идет в присутствии концентрированной серной кислоты при повышенной температуре:  Правило Зайцева – водород отщепляется от менее гидрогенизированного атома углерода. Правило Зайцева – водород отщепляется от менее гидрогенизированного атома углерода. |
| 2) Межмолекулярная дегидратация: образуются простые эфиры. | При межмолекулярной дегидратации спиртов также происходит нуклеофильное замещение: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. 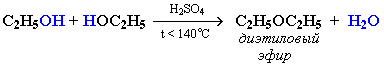 |
| 3) Образование сложных эфиров. | Спирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры. 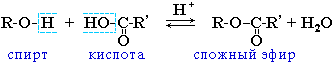 |
МНОГОАТОМНЫЕ СПИРТЫ.
ПОЛУЧЕНИЕ.
| Окисление алкенов холодным водным раствором KMnO4: | R-CH=CH2 + KMnO4 + H2O -> R- CH-CH2 + MnO2 + KOH алкен │ │ диол OH OH |
| Замещение галогенов на гидроксогруппу: | СН2- СН - СН2 + 3KOH -> СН2- СН - СН2 + 3KCl │ │ │ (вод.р-р) │ │ │ Cl Сl Cl OH OH OH |
| Восстановление поликарбонильных соединений: | O=CH – CH =O + H2 –(t,kat)-> CH2-CH2 диальдегид │ │ OH OH |
СВОЙСТВА.
| 1.Кислотные свойства. Этиленгликоль, глицерин вследствие взаимного влияния атомов (-I-эффект ОН-групп) являются более сильными кислотами, чем одноатомные спирты. | Образуют соли не только в реакциях с активными металлами, но и под действием щелочей: HO–CH2-CH2–OH + 2Na -> CH2-CH2 +H2 │ │ ONa ONa HO–CH2-CH2–OH + 2NaOH ⇄ CH2-CH2 +2H2O │ │ ONa ONa |
| 2.Взаимодействуют с раствором гидроксида меди (II) в присутствии щелочи, образуя комплексные соединения (качественная реакция на многоатомные спирты ): |  - ярко-синий раствор гликолята меди. - ярко-синий раствор гликолята меди. |
| 3.Образование сложных эфиров азотной кислоты: реакция с азотной кислотой. | 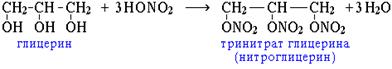 |
| 4. Замещение ОН на галоген: также, как и одноатомные спирты, реагируют с галогеноводородами. | HO–CH2-CH2–OH + 2HBr -> CH2-CH2 + 2H2O │ │ Br Br Можно заместить 1 или 2 группы ОН. |
ФЕНОЛЫ.
Фенолы – гидроксисоединения, в молекулах которых ОН-группы связаны непосредственно с бензольным ядром.

В зависимости от числа ОН-групп различают одноатомные фенолы (например, вышеприведенные фенол и крезолы) и многоатомные. Среди многоатомных фенолов наиболее распространены двухатомные:

Как видно из приведенных примеров, фенолам свойственна структурная изомерия (изомерия положения гидроксигруппы).
ПОЛУЧЕНИЕ.
| 1. Из хлорбензола. | 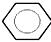 + Cl2 –(AlCl3)-> C6H5Cl + HCl Хлорбензол обрабатывают избытком щелочи, получая водный раствор фенолята натрия: C6H5Cl + 2NaOH –(t,p)-> C6H5ONa + NaCl хлорбензол фенолят натрия Затем фенол выделяют, пропуская углекислый газ. С6H5ONa + CO2 +H2O -> C6H5OH + Na2CO3 + Cl2 –(AlCl3)-> C6H5Cl + HCl Хлорбензол обрабатывают избытком щелочи, получая водный раствор фенолята натрия: C6H5Cl + 2NaOH –(t,p)-> C6H5ONa + NaCl хлорбензол фенолят натрия Затем фенол выделяют, пропуская углекислый газ. С6H5ONa + CO2 +H2O -> C6H5OH + Na2CO3 |
| 2. Из кумола. | Окисление кумола кислородом на катализаторе: 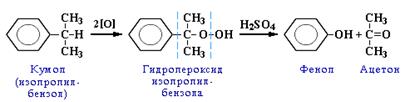 |
СВОЙСТВА ФЕНОЛОВ.
Фенолы являются более сильными кислотами, чем спирты и вода, т.к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается.
Сходство и отличие фенола и спиртов.
| Сходство: как фенол, так и спирты реагируют с щелочными металлами с выделением водорода. Отличие: -фенол не реагирует с галогеноводородами: ОН- группа очень прочно связана с бензольным кольцом, её нельзя заместить; -фенол не вступает в реакцию этерификации, эфиры фенола получают косвенным путем; -фенол не вступает в реакции дегидратации. |
| Кислотные свойства фенолов. | |
| 1. Как и спирты, реагируют с активными металлами. | 2C6H5OH + 2Na ->2C6H5ONa + H2 |
| 2. Реагируют с гидроксидами щелочных и щелочноземельных металлов, образуя соли – феноляты. | C6H5OH + NaOH ->C6H5ONa + H2O |
| Реакции фенола по бензольному кольцу. | |
| 3. Галогенирование. Фенол легко при комнатной температуре взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол): | 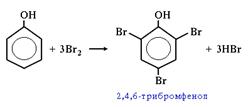 |
| 4. Нитрование. Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов. При использовании концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота). |  |
| 5. Конденсация с альдегидами. С формальдегидом фенол образует фенолоформальдегидные смолы. |  |
| 6. Качественная реакция с хлоридом железа (III). Одноатомные фенолы дают устойчивое сине-фиолетовое окрашивание, что связано с образованием комплексных соединений железа. |
