Тестовые задания: Гетерофункциональные органические соединения.
1. Органические соединения, содержащие в своей структуре несколько разных функциональных групп, называются
1. сложными эфирами
2. полифункциональными соединениями
3. гетерофункциональными соединениями
4. карбоновыми кислотами
5. многоатомными соединениями
2. Химические свойства гетерофункциональных соединений обусловлены наличием
1.карбонильной группы
2.группами, содержащими кислород
3.всех функциональных групп, содержащихся в молекуле
4.углеводородного радикала
5.аминогруппы
3. Аминоспиртами или аминоалкоголями называют спирты, в которых один или несколько атомов водорода замещены
1. аминогруппой
2. остатками углеводов
3. нитрогруппой
4. нитрозогруппой
5. гидроксилом
4. Производные карбоновых кислот, содержащие в радикале альдегидную группу, называются
1. аминоспиртами
2. кетонокислотами
3. гидроксикислотами
4. альдегидокислотами
5. сложными эфирами
5. Производные карбоновых кислот, содержащие в радикале аминогруппу, называются
1.аминоспиртами
2.аминокислотами
3.гидроксикислотами
4.альдегидокислотами
5.амидами кислот
6. Производные карбоновых кислот, содержащие в радикале одну или несколько спиртовых групп, называются
1.аминокислотами
2.кетонокислотами или оксокислотами
3.гидроксикислотами или оксикислотами
4.альдегидокислотами
5.многоатомными спиртами
7. Производные карбоновых кислот, содержащие в радикале кетонную группу, называются
1. аминокислотами
2. кетонокислотами или оксокислотами
3. гидроксикислотами или оксикислотами
4. альдегидокислотами
5. многоатомными спиртами
8. Ацетоуксусный эфир образуется при взаимодействии
1. уксусной кислоты и этилового спирта
2. ацетоуксусной кислоты и метилового спирта
3. уксусной кислоты и аммиака
4. уксусной кислоты и пировиноградной кислоты
5. ацетоуксусной кислоты и этилового спирта
9. Укажите специфическую реакцию для бета-гидроксикислот
1. декарбоксилирование
2. взаимодействие с растворами щелочей
3. межмолекулярная дегидратация, с образованием лактидов
4. внутримолекулярная дегидратация с образованием непредельных кислот
5. окислительное дезаминирование
10. При окислении оксикислот, содержащих первичную спиртовую группу, получаются
1.непредельные карбоновые кислоты
2.альдегидокислоты
3.кетонокислоты
4.фенолокислоты
5.аминокислоты
11. При окислении оксикислот, содержащих вторичную спиртовую группу, получаются
1.непредельные карбоновые кислоты
2.альдегидокислоты
3.кетонокислоты
4.фенолокислоты
5.аминокислоты
12. Укажите число асимметрических атомов углерода в молочной кислоте:
1. 5.
2. 3.
3. 2.
4. 4.
5. 1.
13. Соединению, формула которого
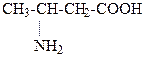 соответствует название
соответствует название
1. бета-аминовалериановая кислота
2. бета-аминоксимасляная кислота
3. альфа-аминомасляная кислота
4. альфа-аминопропионовая кислота
5. 3-аминопропановая кислота
14. Соединению, формула которого
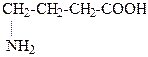 соответствует название
соответствует название
1. бета-аминовалериановая кислота
2. бета-аминоксимасляная кислота
3. альфа-аминомасляная кислота
4. альфа-аминопропионовая кислота
5. гамма-аминомасляная кислота
15. Лактиды – это продукты взаимодействия
1.двух молекул альфа-гидроксикислот
2.молекулы альфа-гидроксикислоты и спирта
3.молекулы спирта и карбоновой кислоты
4.двух молекул спирта
5.двух молекул альфа-аминоксикислот
16.Лактид молочной кислоты образуется из молочной кислоты по реакции
1.внутримолекулярной дегидратации
2.внутримолекулярного дегидрирования
3.междумолекулярной дегидратации
4.междумолекулярного дегидрирования
5.декарбоксилирования
17.Производные ароматических углеводородов, образующиеся в результате замены атомов водорода в бензольном ядре карбоксильной и гидроксильными группами, называют
1.ароматическими спиртами
2.ацилированными фенолами
3.фенолокислотами
4.кислыми фенолами
5.фенолфталеинами
18.Ацетилсалициловая кислота (аспирин) легко подвергается гидролизу с образованием
1. салициловой и уксусной кислот
- салициловой и муравьиной кислот
- бензойной и уксусной кислот
- бензойной кислоты и этанола
- салициловой кислоты и этанола
19. Укажите название кислоты, которое соответствует формуле
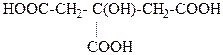
1. салициловая кислота
2. лимонная кислота
3. щавелевоуксусная кислота
4. сульфаниловая кислота
5. бета-гидроксивалериановая кислота
20. Укажите тривиальное название карбоновой кислоты
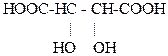
1. яблочная кислота
2. молочная кислота
3. лимонная кислота
4. винная кислота
5. пировиноградная кислота
21. Формула
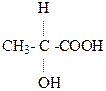 соответствует
соответствует
1. яблочная кислота
2. молочной кислота
3. Д-винной кислоте
4. L-винной кислоте
5. мезовинной кислоте
22. Соединение
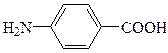 называется:
называется:
1 бензойная кислота
2. сульфаниловая кислота
3. молочная кислота
4. пара-аминофенол
5. пара-аминобензойная кислота
23.Соединение, формула которого
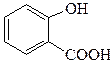 называется
называется
1. салициловая кислота
2. сульфаниловая кислота
3. молочная кислота
4. пара-аминофенол
5. пара-аминобензойная кислота
24. Соединение, формула которого
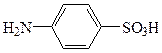 называется:
называется:
1. салициловая кислота
2. сульфаниловая кислота
3. молочная кислота
4. пара-аминофенол
5. сульфобензойная кислота
25. Соединение, формула которого
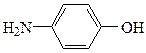 называется
называется
1. салициловая кислота
2. сульфаниловая кислота
3. молочная кислота
4. пара-аминофенол
5. пара-аминобензойная кислота
26. Лекарственный препарат, формула которого
 называется
называется
1.фтивазид
2.стрептоцид или амид сульфаниловой кислоты
3.парацетамол
4.аспирин или ацетилсалициловая кислота
5.амидопирин
27. Биогенный амин, формула которого
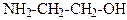 называется
называется
1.норадреналин
2.адреналин
3. дофамин
4.холин
5. коламин
28. Щелочную pеакцию сpеды имеет водный раствор альфа-аминокислоты
1. глицин
2. метионин
3. валин
4. лизин
5. тиpозин
29. К аpоматическим альфа-аминокислотам относятся оба вещества в pяду
1. цистеин, глицин
2. лизин, аланин
3. тиpозин, фенилаланин
4. лейцин, тpиптофан
5. валин, глутаминовая кислота
30. Для обнаpужения альфа-аминокислот, содеpжащих в радикале аpоматические циклы, используется реакция
1. биуpетовая
2. ксантопpотеиновая
3. Шульце-Распайля
4. нингидpиновая
5. pеакция Фоля
31. Разветленное стpоение цепи в алифатическом pадикале имеет альфа-аминокислота
1. валин,
2. сеpин
3. аспаpагин,
4. цистин,
5. глицин.
32. Укажите, в каком ряду указаны незаменимые аминокислоты
1. гистидин, тирозин, цистин
2. метионин, серин, треонин
3. аланин, валин, фенилаланин
4. валин, триптофан, метионин
5. глицин, валин, аланин
33. К иминокислотам относятся обе аминокислоты в ряду
1. серин, валин
2. тирозин, триптофан
3. лейцин, изолейцин
4. пролин, гидроксипролин
5. цистеин, цистин
34. Биогенный амин коламин (2-аминоэтанол) образуется при декарбоксилировании аминокислоты
1. валин
2. гистидин
3. метионит
4. треонин
5. серин
35. Биогенный амин гистамин получается в организме из гистидина реакцией
1. дезаминирования
2. декарбоксилирования
3. гидратации
4. дегидрирования
5. галогенирования
36. Взаимопревращение аминокислот цистеина и цистина лежит в основе важного процесса в клетке
1. реакции дегидратации
2. реакции окисления-восстановления
3. дезаминирования
4. декарбоксилирования
5. реакции гидролиза
37. В организме синтез альфа-аминокислот осуществляется реакцией переаминирования с использованием в качестве исходных веществ
1. альдегидов и кетонов
2. олиго- и полисахаридов
3. омыляемых и неомыляемых липидов
4. первичных и вторичных аминов
5. кетокислоты и аминокислоты
38. В водном растворе кислую реакцию среды на индикатор имеет альфа-аминокислота
1. глутаминовая кислота
2. лейцин
3. изолейцин
4. фенилаланин
5. триптофан
39. К моноаминодикарбоновым кислотам относится
1. метионин
2. аспарагиновая кислота
3. изолейцин
4. аргинин
5. тирозин
40. К нейтральным альфа-аминокислотам относится вещество
1. валин
2. лизин,
3. глутаминовая кислота
4. аспарагиновая кислота
5. аргинин,
41. Аминокислота - серин входит в состав
1. жиров
2. кефалинов
3. ганглиозидов
4. цереброзидов
5. неомыляемых липидов
42. Серосодержащими альфа-аминокислотами являются оба вещества в ряду
1. метионин, цистеин
2. серин, аргинин
3. гистидин, фенилаланин
4. цистин, валин
5. пролин, оксипролин
43. Если при добавлении нингидрина к исследуемому раствору появляется сине-фиолетовое окрашивание, то это указывает на присутствие в растворе
1. белков
2. восстанавливающих дисахаридов
3. альдегидов
4. альфа-аминокислот
5. пептидов
44. Если при действии концентрированной азотной кислоты на раствор белка появляется желтое окрашивание переходящее в оранжевое при добавлении щелочи, то это указывает на присутствие в белках аминокислоты
1. лизина
2. серина
3. валина
4. тирозина
5. аргинина
45. Альфа-аминокислоты, которые не синтезируются в организме человека и должны поступать с пищей, называются
1. гетероциклическими
2. ароматическими
3. алифатическими
4. заменимыми
5. незаменимыми
46. Если при нагревании раствора белка с ацетатом свинца в щелочной среде образуется черный осадок сульфида, то это указывает на присутствие аминокислоты
1. аргинин
2. серин
3. цистеин
4. тирозин
5. валин
47. Биуретовая реакция применяется для обнаружения
1.альдегидов
2.пептидных связей
3.сложноэфирных связей
4.аминокислот
5.многоатомных спиртов
48. Амфотерные свойства аминокислот объясняются
1.расположением аминогруппы относительно старшей группы
2.химическими свойствами аминогруппы и карбоксила
3.количеством функциональных групп
4.способностью аминокислот образовывать пептидные связи
5.способностью аминокислот к реакциям дезаминирования
49. Из аланина (АЛА) и валина (ВАЛ) можно получить дипептиды следующего состава
1. АЛА-ВАЛ
2. АЛА-ВАЛ, ВАЛ-АЛА
3. АЛА-АЛА, АЛА-ВАЛ, ВАЛ-АЛА
4. ВАЛ-ВАЛ, АЛА-АЛА, АЛА-ВАЛ, ВАЛ-АЛА
5. дипептиды из данных аминокислот получить не возможно
50. Защита аминогруппы альфа-аминокислоты при синтезе пептидов проводится за счет реакции
1.гидрирования
2.ацилирования аминогруппы
3.галогенирования аминогруппы
4.дезаминирования
5.образования сложного эфира
51. Белки для третичной структуры для которых характерна альфа-спираль, уложенная в пространстве в виде сферы – глобулы (например, яичный белок, фермент - глобин в составе гемоглобина) – называются
1. фибриллярными
2. глобулярными
3. гидрофобными
4. гидрофильными
5. делокализованными
52. Первичная структура пептидов и белков поддерживается связями
1. водородными
2. ионными
3. пептидными
4. гидрофобными
5. координационными
53. Пептидная или белковая макромолекула является продуктом реакции:
1. полимеризации альфа-аминокислот
2. поликонденсации альфа-аминокислот
3. гидролиза полипептидов
4. гидратации альфа-аминокислот
5. диссоциации альфа-аминокислот
54. При денатурации полипептидной цепи фермент белок теряет
1. ферментативную активность
2. первичную структуру
3. количественный состав аминокислот
4. последовательность аминокислот
5. первичную и вторичную структуру
55. Для обнаружения пептидных связей в пептидах и белках служит
1. ксантопротеиновая реакция
2. нингидриновая реакция
3. биуретовая pеакция
4. реакция Фоля
5. реакция Зинина
56. Аминокислотная последовательность, т.е. порядок чередования альфа-аминокислотных остатков, определяет
1. первичную структуру пептидов и белков
2. вторичную структуру белков
3. третичную структуру белков
4. четвертичную структуру белков
5. нет правильного ответа
57.Инсулин-гормон поджелудочной железы по строению молекулы является
1. простым белком
2. нонапептидом
3. полипептидом
4. аминокислотой
5. сложным белком
58. Аминокислота, формула которой
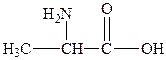 называется
называется
1. треонин
2. триптофан
3. пролин
4. гистидин
5. аланин
59. Аминокислота, формула которой
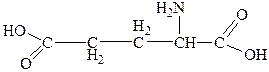 называется
называется
1. треонин
2. аспарагиновая кислота
3. глутаровая кислота
4. гистидин
5. глутаминовая кислота
60. Аминокислота, формула которой
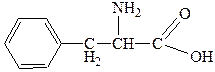 называется
называется
1. треонин
2. триптофан
3. пролин
4. гистидин
5. фенилаланин
