История развития представлений об образовании химической связи
Э. Франкленд в 1852 предложил концепцию, согласно которой каждый элемент образует соединения, связываясь с определённым числом эквивалентов др. элементов, при этом один эквивалент соответствует количеству, требуемому одной валентностью. Ф. А. Кекуле и А. В. Г. Кольбе в 1857 в соответствии с представлениями валентности выдвинули положение, что углерод обычно имеет валентность 4, образует 4 связи с др. атомами. А. С. Купер в 1858 указал, что атомы углерода, связываясь между собой, могут образовывать цепочки. В его записи химические формулы имели очень большое сходство с современными, связи изображались чёрточками, соответствующими валентным связям между атомами. Термин «химическое строение» впервые ввёл А. М. Бутлеров в 1861. Он подчёркивал, сколь существенно выражать строение единой формулой, показывающей, как в молекуле соединения каждый атом связан с др. атомами. Согласно Бутлерову, все свойства соединения предопределяются его молекулярным строением; он высказал уверенность, что точную структурную формулу можно установить по результатам изучения путей синтеза данного соединения. Следующий шаг, заключавшийся в приписывании молекулам пространственной трёхмерной структуры, был сделан в 1874 Я. Х. Вант-Гоффом и Ж. А. Ле Белем.
В 19 в. валентная связь изображалась чёрточкой между символами двух химических элементов. Природа этой связи была совершенно неизвестна. После открытия электрона делались многочисленные попытки развить электронную теорию химической связи. Наиболее успешными были работы американского ученого Г. Н. Льюиса, который в 1916 предложил рассматривать образование химической связи, называемой теперь ковалентной связью, как результат того, что пара электронов становится общей для двух атомов.
Согласно теории химической связи, наибольшей устойчивостью обладают внешние оболочки из двух или восьми электронов (электронные группировки благородных газов). Атомы, имеющие на внешней оболочке менее восьми (или иногда двух) электронов, стремятся приобрести структуру благородных газов. Такая закономерность позволила В. Косселю и Г. Льюису сформулировать положение, которое является основным при рассмотрении условий образования молекулы: «При образовании молекулы в ходе химической реакции атомы стремятся приобрести устойчивую восьмиэлектронную (октет) или двухэлектронную (дублет) оболочки».
Разработка квантовой механики (1925) и использование многих экспериментальных методов (молекулярной спектроскопии, рентгенографии кристаллов, газовой электронографии, методов изучения магнитных свойств) для определения длин связей (межатомных расстояний), углов между связями, числа неспаренных электронов и других структурных параметров молекул и кристаллов привели к более глубокому пониманию природы химической связи.
Образование ковалентной связи можно рассматривать в рамках двух методов квантовой химии: методавалентных связейи метода молекулярных орбиталей.
Метод валентных связей
Предположения Льюиса о том, что химическая связь образуется за счет обобществления двух электронов послужили основой для развития метода валентных связей.
Образование химической связи между атомами водорода является результатом взаимопроникновения (перекрывания) электронных облаков. Вследствие этого перекрывания плотность отрицательного заряда в межъядерном пространстве возрастает, и положительно заряженные ядра притягиваются к этой области. Такая химическая связь называется ковалентной.
Представления о механизме образования молекулы водорода были распространены на более сложные молекулы. Разработанная на этой основе теория химической связи получила название метода валентных связей (метод ВС). В основе метода ВС лежат следующие положения:
1) Ковалентная связь образуется двумя электронами с противоположно направленными спинами, причем эта электронная пара принадлежит двум атомам и находится на орбитали, образовавшейся за счет перекрывания двух атомных орбиталей.
2) Ковалентная связь тем прочнее, чем в большей степени перекрываются электронные
облака. Связь образуется в том случае, когда в атомные волновые функции образующие связь будут иметь одинаковые знаки в области перекрывания.
3) Химическая связь в методе ВС является двухцентровой и локализована в области между ядрами двух атомов ее образующих.
Метод валентных связей (ВС) иначе называют теорией локализованных электронных пар, поскольку в основе метода лежит предположение, что химическая связь между двумя атомами осуществляется с помощью одной или нескольких электронных пар, которые локализованы преимущественно между ними. Число элементарных химических связей, которые способен образовывать атом или ион, равно его валентности. B образовании химической связи принимают участие валентные электроны.
Валентностьатома в данном соединении – это количество общих электронных пар, которые данный атом образует по обменному и донорно-акцепторному механизму с другими атомами. Например, валентность азота в аммиаке (NH3) равна трем, а в ионе аммония (NH4+) – четырем.
Волновая функция, описывающая состояние электронов, образующих связь, называется локализованной орбиталью (ЛО).
Гибридизация орбиталей
Для объяснения фактов, когда атом образует большее число связей, чем число неспаренных электронов в его основном состоянии (например, атом углерода), в методе валентных связей (ВС) используется постулат о гибpидизации близких по энергии атомных орбиталей.
Гибридизация – это прием построения одинаковых по энергии и форме гибридных валентных орбиталей путем линейной комбинации (суммы) АО в методе валентных связей
Гибридизация АО происходит при образовании ковалентной связи, если при этом достигается более эффективное перекрывание орбиталей.
Гибридизация атома углерода осуществляется его возбуждением и переносом электрона с 2s- на 2р-АО
Согласно представлению о гибридизации, химические связи образуются смешанными – гибридными орбиталями (ГО), которые представляют собой линейную комбинацию АО данного атома (s- и p-АО Be, C), обладают одинаковыми энергией и формой, определенной ориентацией в пространстве (симметрией). Так одна s- и одна p-орбиталь дают две sp-ГО, расположенные под углом 180° друг относительно друга (Рис.5.2.а).
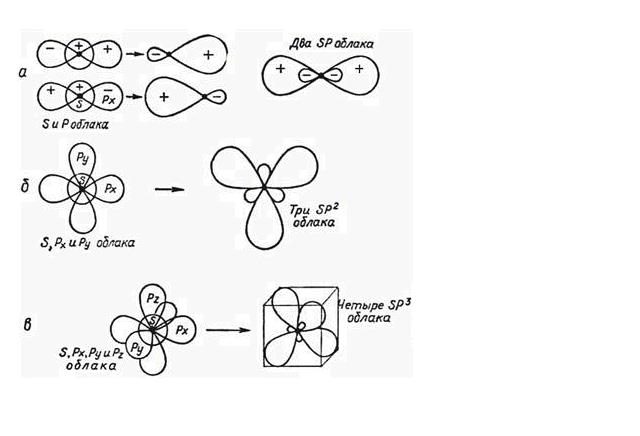
Рис. 5.2. Гибридизация электронных орбиталей: а) - sp-, б) - sp2-, в) - sp3- ГО.
Гибридные sp-орбитали участвуют в образовании двух σ-связей. Остальные две р-орбитали этого же подуровня не гибридизованы и расположены в плоскости перпендикулярной оси симметрии гибридных взаимно перпендикулярно друг другу и образуют в соединениях две π -связи.
Для элементов 2-го периода sp-гибридизация происходит по схеме:
2s + 2px= 2 (2sp)
2py- и 2pz-АО не изменяются. Это состояние характерно для атомов С, N, O с тройной связью. Например, в молекулах ВеН2, ацетилене C2H2, ацетонитриле СН3СN.
Одна s- и две p-орбитали смешиваются, и образуются три равноценные sp2-гибридные орбитали, расположенные в одной плоскости под углом 120°
Они могут образовывать три σ-связи. Третья р-орбиталь остается негибридизованной и ориентируется перпендикулярно плоскости расположения гибридных орбиталей (Рис.5.2. б.). Эта р-АО участвует в образовании π-связи.
Для элементов 2-го периода процесс sp2-гибридизации происходит по схеме:
2s + 2px + 2py = 3 (2sp2)
2pz-АО в гибридизации не участвует.
sp2-Гибридизованное состояние свойственно атому, если сумма числа связанных с ним атомов или число его неподеленных электронных пар равна 3
Углерод в sp2-гибридном состоянии образует простое вещество графит. Это состояние характерно для атомов С, N, O и др. с двойной связью. Например, в молекулах ВН3, SO2, SO3, HCOOH, HCONH2, этилена C2H4, бензола C6H6 (атомы C, О и N).
Одна s- и три p-орбитали одного уровня формируют четыре равноценные гибридные sp3-орбитали, расположенные под углом 109°28' друг к другу (Рис.5.2. в). Они могут образовывать четыре σ-связи.
Так, в молекуле CH4 гибридные орбитали из четырех АО углерода (одной s и трех p), называются sp3-орбиталями, они полностью эквивалентны энергетически и пространственно направлены к вершинам тетраэдра:
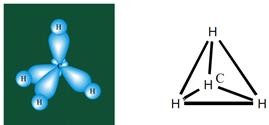
Атомы водорода расположены в вершинах, а улерода - в центре тетраэдраэдрической молекулы метана.
Таким образом, когда один атом образует несколько связей, а его валентные электроны принадлежат разным орбиталям (s и p; s, p и d), для объяснения геометрии молекул в МВС необходимо привлекать теорию гибридизации атомных орбиталей. Основные положения теории следующие:
Введение гибридных орбиталей служит для описания направленных локализованных связей. Гибридные орбитали обеспечивают максимальное перекрывание АО в направлении локализованных σ-связей.
Число гибридных орбиталей равно числу АО, участвующих в гибридизации.
Гибридизуются близкие по энергии валентные АО независимо от того, заполнены они в атоме полностью, наполовину или пусты.
В гибридизации участвуют АО, имеющие общие признаки симметрии.
Гибридные орбитали дают молекулы с углами 180°, 120°, 109°28', 90°. Это правильные геометрические фигуры. Такие молекулы образуются, когда все периферические атомы в многоэлектронной молекуле (или ионе) одинаковы и их число совпадает с числом гибридных орбиталей. Однако, если число гибридных орбиталей больше числа связанных атомов, то часть гибридных орбиталей заселена электронными парами, не участвующими в образовании связи, – несвязывающими или неподеленными электронными парами.
В образовании двойной связи участвуют две поделенные электронные пары, а в образовании тройной связи - три пары. В каждой из этих структур атом углерода приобретает электронную конфигурацию неона, будучи окружен четырьмя поделенными парами электронов.
В молекуле воды H2O aтом кислорода окружен двумя неподелёнными парами электронов и двумя поделенными парами. 2s-Орбиталь несколько более стабильна, нежели 2р-орбитали, так что неподелённые электронные пары прежде всего заполняют 2s-орбиталь. Если бы две связи в молекуле воды были образованы р-орбиталями атома кислорода, то угол между связями был бы равен 90 0, поскольку при угле 900 друг относительно друга р-орбитали имеют максимальную силу связи. Расчёты показывают, что максимальная устойчивость достигается в том случае, когда орбитали, образующие связи в молекуле воды, в небольшой мере имеют также s-характер, соответственно валентный угол между связями несколько больший, чем 90 0. Экспериментальное значение валентного угла в молекуле H2O 104,52, а валентные углы в гидридах H2S, H2Se и H2Te равны 92, 91 и 90 соответственно.
Энергия двойной углерод-углеродной связи на 73 кдж×моль-1 меньше, чем сумма энергий двух одинарных связей, энергия же тройной связи на 220 кдж×моль-1 меньше суммы энергий трёх одинарных связей.
Гибридные орбитали центрального атома образуют сигма-связи (σ-связи) с АО других атомов и формируют пространственную структуру молекулы.
Следует отметить, что молекула принимает определенную геометрию не из-за того, что первоначально происходит та или иная гибридизация центрального атома; представление о гибридизации является удобным инструментом описания реальной формы молекул в рамках метода валентных связей (ВС).
Гибридные орбитали формируются из близких по энергии АО, в частности, sp-,
sp2-, sp3-орбитали – из s- и p-орбиталей одного уровня (ns и np), а sp3d2 –орбитали – из АО соседних (ns, np, (n-1)d), либо одного уровня (ns np nd)
5.6 Резонанс
Правила построения валентных структур на основании представлений о поделенных парах электронов и использования устойчивой орбитали каждого из двух атомов, между которыми образуется ковалентная связь, позволяют написать структурные формулы для очень большого числа веществ, однако для некоторых веществ одна валентная структура не даёт вполне адекватного представления о свойствах. Веществом именно такого рода является, например, озон O3. Спектроскопические исследования озона показали, что атомы в его молекуле расположены под углом 1170 (угол между связями у центрального атома кислорода), а каждая из двух связей кислород - кислород имеет длину 128 пм (1пм = 10-12 м. Есть все основания приписать молекуле озона следующую валентную структуру:
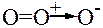
Эта структура представляется удовлетворительной, поскольку каждый из атомов кислорода окружен четырьмя парами электронов, причём некоторые пары поделенные, а некоторые неподелённые. Однако если приписать формальные заряды атомам, разделив поделенные пары электронов поровну между двумя атомами, то центральный атом будет иметь положительный заряд, а атом, связанный с ним одинарной связью, - отрицательный. Такую электронную структуру нельзя считать вполне удовлетворительной, поскольку межатомное расстояние, отвечающее двойной связи, должно быть приблизительно на 21 пм меньше, чем расстояние для одинарной связи, тогда как согласно наблюдениям эти расстояния равны. Такое расхождение можно объяснить, приняв и вторую валентную структуру (В) для данной молекулы:
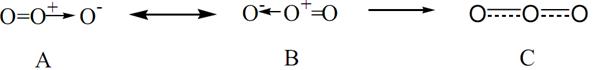
Приведённые структуры эквивалентны. Они называются резонансными или мезомерными и на схемах их объединяют двухсторонними стрелками (↔). При квантовомеханическом рассмотрении молекулы озона ей приписывается волновая функция, которая представляет собой сумму волновых функций для этих двух валентных структур. Установлено, что подобная волновая функция отвечает среднему значению длины связи, одному и тому же для обеих связей, и, кроме того, эта волновая функция соответствует большей стабильности, нежели каждая из волновых функций отдельных валентных структур. Такая дополнительная стабилизация описывается как энергия резонанса, соответствующая резонансу молекулы между двумя структурами. Отсюда следует, что озон нельзя удовлетворительно описать одной валентной структурой обычного типа, тогда как комбинация двух валентных структур приводит к удовлетворительному описанию молекулы в её основном состоянии. Ее можно изобразить симметричной формулой (С), в которой отражена идентичность концевых атомов кислорода в молекуле О3.
Аналогичная ситуация наблюдается при рассмотрении молекулы бензола, строение которой казалось химикам загадочным до разработки (1928-33) теории резонанса (называемая также мезомерией). Кекуле указывал, что четырёхвалентность углерода в бензоле можно показать с помощью структурной формулы с чередующимися простыми и двойными связями. Однако таких структур может быть две:
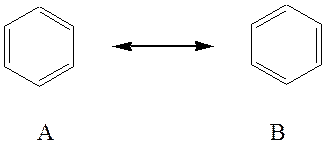
Были предприняты попытки обнаружить изомеры таких веществ, как о-дихлорбензол (атомы хлора присоединены к атомам углерода, связанным двойной связью в случае первого изомера и одинарной связью в случае второго). Однако обнаружить такие изомеры не удалось, и было признано, что все шесть углерод-углеродных связей в бензольном кольце эквивалентны друг другу. Детальное квантовомеханическое рассмотрение бензола показало. что его молекула имеет гексагональную симметрию и что все шесть углерод-углеродных связей эквивалентны. Этот факт позволяет сказать, что основное состояние молекулы бензола может быть представлено двумя структурами Кекуле, налагающимися одна на другую или резонирующими между собой. В соответствии с квантовомеханическими расчётами реальная молекула бензола должна быть приблизительно на 150 кдж×моль-1 устойчивее, нежели гипотетическая молекула, описываемая лишь одной структурой Кекуле. Эта дополнительная устойчивость обусловливает повышенную сопротивляемость бензола гидрогенизации по сравнению с обычными ненасыщенными соединениями.
Молекула бензола в её основном состоянии может быть представлена единственной формулой А или более близкой к реальной структурой Б:
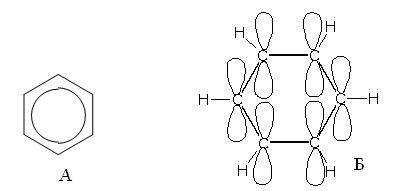
Кружок, проведённый внутри шестиугольника, означает, что данная структура описывает реальную молекулу, то есть отвечает большей устойчивости по сравнению со структурой Кекуле, и отражает эквивалентность всех шести углерод-углеродных связей.
В рамках метода ВС представление о резонансныхструктурах позволяет объяснить пространственное строение многих молекул и ионов, содержащих π-связи. Так, например, пространственная структура частиц BCl3, BO33-, CO32-, NO3- соответствует правильному треугольнику в центре которого расположены атомы бора, углерода и азота, образующие по три σ-связи за счет их sp2-гибридных орбиталей с расположенными в вершинах атомами хлора или кислорода. У каждого центрального атома имеется р-орбиталь не участвующая в гибридизации и ориентированная перпендикулярно треугольнику. При этом на ней у атома бора нет электронов, у атома углерода – один, азота – два электрона. За счет этих орбиталей возможно образование π-связей с ориентированными перпендикулярно плоскости частицы р-орбиталями хлора или кислорода. π-Связь атома бора с атомами хлора или кислорода образуется путем включением их неподеленных пар электронов в поле обоих атомов (донорно-акцепторный механизм). В ионе NO3- неподеленная пара электронов азота включается в образование π-связей с атомами кислорода. Структурные формулы указанных соединений являются несимметричными – одна связь центрального атома с тремя атомами хлора или кислорода отличается от двух других:
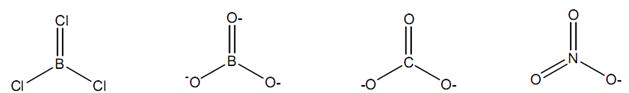
В действительности реальная структура с позиции метода резонанса – это усредненная комбинация трех резонансных структур с двойной связью с каждым из трех атомов хлора или кислорода, причем вклад каждой из них одинаков:
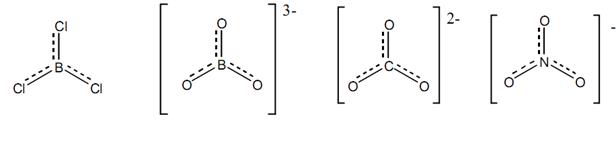
Таким образом, система π-связей BCl3, BO33-, CO32-, NO3- включает четыре р-орбитали атомов, на которых находится 6 электронов.
