Качественная реакция на борат-ион
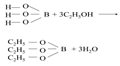
66. Общая характеристика щелочных металлов. Натрий, калий: свойства, биологическая роль.
 Щелочны́е мета́ллы — это элементы I группы главной подгруппы периодической таблицы химических элементов.
Щелочны́е мета́ллы — это элементы I группы главной подгруппы периодической таблицы химических элементов.
литий 3Li
натрий 11Na
калий 19К
рубидий 37Rb
цезий 55Cs
франций 87Fr
радиусы атомов ↑энергия ионизации ↓
способность отдавать электроны ↑
металлические свойства ↑
восстановительная способность ↑
Строение внешнего энергетического уровне ….ns1, в соединениях постоянная степень окисления + 1.
11Na 19К
…ns1 , I, +1
Нахождение в природе:
В свободном виде щелочные металлы в природе не встречаются.
Основные природные соединения натрия:
-галит, или каменная (поваренная) соль NaCl
-мирабилит, или глауберова соль Na2SO4 ∙ 10H2O.
Важнейшие минералы калия:
-сильвинит NaCl ∙KCl
-карналлит KCl ∙MgC12∙ 6H2O
Физические свойства:
-На свежем срезе щелочные металлы - серебристо-белые с металлическим блеском, который на воздухе быстро исчезает вследствие окисления кислородом воздуха.
-Хранят под слоем керосина или в атмосфере инертного газа.
-Щелочные металлы являются легкими и пластичными. Литий - самый легкий металл, его плотность равна 0,534 г/см3 (200 С).
-Это мягкие металлы, по мягкости Na, К, Rb и Cs подобны воску, самым твердым является литий.
-Щелочные металлы легкоплавкие. Так, температура плавления цезия равна 28,50С, температура плавления лития (180,50С).
-Щелочные металлы обладают хорошей тепло- и электропроводностью.
Химические свойства:
Щелочные металлы обладают высокой химической активностью, активность увеличивается в ряду Li – Na – K – Rb – Cs – Fr.
В реакциях они являются сильными восстановителями.
Взаимодействие с простыми веществами.
1. взаимодействие с кислородом.
Щелочные металлы легко окисляются кислородом воздуха, а рубидий и цезий даже самовоспламеняются.
С кислородом литий образует оксид:
4Li + O2 = 2Li2O
Основным продуктом окисления натрия является пероксид натрия: 2Na + O2 = Na2O2
Калий, рубидии и цезии при взаимодействии с кислородом образуют главным образом надпероксиды, например надпероксид (супероксид) калия: К + O2 = KO2
2. щелочные металлы самовоспламеняются во фторе, хлоре, парах брома, образуя галогениды:
2Na + Br2 =2NаВr
3. при нагревании щелочные металлы взаимодействуют со многими неметаллами (водородом, серой, селеном, йодом, азотом, углеродом):2Na + S = Na2S
4. щелочные металлы взаимодействуют с водородом при слабом нагревании, образуя гидриды: 2Na + Н2 = 2NaH
5. натрий и калий реагируя с ртутью образуют амальгамы.
Щелочные металлы взаимодействуют также со многими металлами, образуя интерметаллические соединения, например: Li2Zn, Nа2Sn.
Взаимодействие с водой.
Все щелочные металлы активно реагируют с водой, восстанавливая ее до водорода
2Na + 2Н2О = 2NaOH + H2↑
Активность взаимодействия металлов с водой увеличивается в ряду от лития к цезию. Так, калий при взаимодействии с водой воспламеняется, а рубидий и цезий реагируют со взрывом.
Взаимодействие с кислотами
1. щелочные металлы взаимодействуют с HCl и разбавленной H2SO4 с выделением водорода:
2Na + 2НСl = 2NaCl + H2↑
2. концентрированную серную кислоту щелочные металлы восстанавливают главным образом до сероводорода:
8Na + 5H2SO4 = 4Na2SO4 + H2S↑ + 4Н2О
При этом возможно параллельное протекание реакции восстановления серной кислоты до оксида сepы (IV) - SO2 и элементной серы S.
3. при реакции с разб. азотной кислотой преимущественно получается аммиак или нитрат аммония, а с конц. кислотой - азот или оксид азота (I) 8Na + 10НNO3(разб.) = 8NаNO3 + NН4NO3 + 3Н2О; 8K+ 10HNO3(конц.) = 8KNO3 + N2O + 5H2O
Взаимодействие с оксидами металлов и солями
Щелочные металлы вследствие высокой химической активности могут восстанавливать многие металлы из их оксидов и солей:
ВеО + 2Na = Ве + Na2O; СаСl2 + 2Na = Са + 2NaCl
Биологическая роль:
Ион натрия Na+ - главный внеклеточный ион,
ион калия К+ - основной внутриклеточный ион, их взаимодействие поддерживает жизненно важные процессы в клетках. В организме человека растворимые соли натрия хлорид, фосфат, гидрокарбонат – входят в состав крови, лимфы.
Осмотическое давление крови поддерживается на необходимом уровне за счет хлорида натрия.
67. Щелочноземельные металлы. Соединения кальция: свойства, биологическая роль.
Щё́лочноземе́льные мета́ллы — химические элементы 2-й группы главной подгруппы периодической таблицы элементов: бериллий, магний, кальций, стронций, барий и радий.
Строение внешнего уровня .... ns2
Сильные восстановители.
Образуют основные оксиды типа - RO, которым отвечают основания типа - R(OH)2
В ряду Ве(ОН)2 → Rа(ОН)2 растворимость и основные свойства увеличиваются
Ве(ОН)2 - амфотерное основание.
Ве и Мg несколько отличаются от остальных металлов подгруппы. Ве с водой не взаимодействует, Мg - при нагревании, а остальные Ме активно реагируют при обычных условиях: R + 2H2O = R(OH) + H2
Щелочноземельные металлы с водородом образуют гидриды общей формулы RH2
Соединения Кальция
СаО - негашеная известь (техн. название жженая известь или «кипелка») порошок белого цвета.
В промышленности получается при обжиге известняка, мела и других карбонатных пород:
CaCO3= CaO + CO2
СаО - основной оксид (техн. название гашенная известь, в виде порошка называется – пушенкой)
1. Взаимодействие с водой: СаО+Н2О = Са(ОН)2
2. Взаимодействие с кислотными оксидами и кислотами: СаО+СО2 =СаСО3
СаО + 2НNO3 = Са(NO3)2 + Н2О
3. при высоких температурах реагирует с коксом, образуя карбид кальция: СаО + 3С = СаС2 + СО
Са(ОН)2 - техн. название - гашенная известь, твердое вещество белого цвета, растворим в воде, раствор называется известковой водой, обладает щелочными свойствами: Сa(OH)2 +CO2 = CaCO3↓ + H2O; CaCO3 + H2O + CO2 = Ca(HCO3)2
2. Ca(OH)2 + H2SO4 = CaSO4 + H2O
3. 3Ca(OH)3 + 2FeCl3 = 2Fe(OH)3↓+ 3СаCl2
4. Качественная реакция на катион Ca2+
а) окрашивание пламени в кирпично-красный цвет
б) (NH4)2C2O4 + Ca2+ = CaC2O4↓(белый) + 2NH4+
Соли кальция
СаSO4 ∙ 2Н2О - гипс, как вяжущее средство в строительстве, в медицине - при наложении гипсовых повязок.
Са(SO4)2 ∙ H2O- алебастр.
Са3(РО4)2 - основной компонент фосфоритов и апатитов – сырье для производства фосфорных удобрений, это главный конструкционный материал наших костей.
СаСl2 ∙ 6Н2О - широко применяется в медицине, внутривенные инъекции растворов СаСl2 снижают спазмы сердечно-сосудистой системы, улучшают свертываемость крови, помогает бороться с оттеками, воспалениями, аллергией.
СаСl2 + Са(СlO)2 - хлорная известь - окислитель в качестве отбеливающего и дезинфицирующего средства, а так же для дегазации местности, зараженной стойкими отравляющими веществами.
СаF2 - флюоргий - прозрачные кристаллы, представляют ценность для оптики потому что они пропускают ультрафиолетовые и инфракрасные лучи намного лучше, чем стекло, кварц или вода.
СаС2 – карбид для автогенной сварки и резки металла, для получения ацетилена.
Кальций — распространенный макроэлемент в организме растений, животных и человека. В организме человека и других позвоночных большая его часть находится в скелете и зубах. Ионы кальция участвуют в процессах свертывания крови, а также служат одним из универсальных вторичных посредников внутри клеток и регулируют самые разные внутриклеточные процессы — мышечное сокращение, в том числе секрецию гормонов.
68. Щелочноземельные металлы. Соединения магния: свойства, биологическая роль.
Щё́лочноземе́льные мета́ллы — химические элементы 2-й группы главной подгруппы периодической таблицы элементов: бериллий, магний, кальций, стронций, барий и радий.
Строение внешнего уровня .... ns2
Сильные восстановители.
Образуют основные оксиды типа - RO, которым отвечают основания типа - R(OH)2
В ряду Ве(ОН)2 → Rа(ОН)2 растворимость и основные свойства увеличиваются
Ве(ОН)2 - амфотерное основание.
Ве и Мg несколько отличаются от остальных металлов подгруппы. Ве с водой не взаимодействует, Мg - при нагревании, а остальные Ме активно реагируют при обычных условиях:
R + 2H2O = R(OH)2 + H2
Щелочноземельные металлы с водородом образуют гидриды общей формулы RH2
Соединения магния:
Оксид магния MgO - белый, тугоплавкий порошок, малорастворим в воде, обладает основными свойствами.
МgО+2НСl=МgCl2+ Н2О
MgO+CO2 =MgCO3
Гидроксид магния Мg(OH)2 - типичное основание средней силы.
Получение в лаборатории:
МgCl2 +2КОН = Мg(OН)2↓ + 2КСl
Химические свойства:
1. Мg(OH)2 +2HNО3 = Мg(NO3)2 + 2Н2О
2. Мg(OH)2 = МgO + Н2О
Качественная реакция на Mg2+
MgSO4 +Na2HPO4 +NH4OH = MgNH4PO4↓+ Na2SO4 +H2O
Соли магния:
MgSO4 ∙ 7H2O - горькая английская соль, применяется в качестве слабительного, в виде инъекций - как спазмолитик, противосудорожное и обезболивающее средство.
Mg2Si3O8 · nH2O – трисиликат магния, применение в медицине основано на его адсорбционном действии, поэтому его назначают при гастритах и кишечных заболеваниях.
МgCO3 ∙ Мg(OH)2 ∙ H2O - белая магнезия применяется внутрь при повышенной кислотности желудочного сока, как легкое слабительное, входит в состав зубного порошка.
MgCl2 ∙ 6H2O -водный раствор, для приготовления магнезиального цемента, ксилолита и др. синтетических материалов.
MgCO3 – в производстве теплоизоляционных материалов.
Биологическая роль:
Магний является кофактором многих ферментативных реакций. Магний необходим для превращения креатина фосфата в АТФ — нуклеотид, являющийся универсальным поставщиком энергии в живых клетках организма. Магний необходим на всех этапах синтеза белка. Он участвует в поддержании нормальной функции нервной системы и мышцы сердца, оказывает сосудорасширяющее действие, стимулирует желчеотделение, повышает двигательную активность кишечника, что способствует выведению шлаков из организма (в том числе и холестерина).
69. Жесткость воды: виды жесткости, способы ее устранения.
Жесткость воды – совокупность свойств воды, обусловленная содержанием в воде ионов Са2+ и Мg2+.
Виды жесткости:
1. Карбонатная (или временная) жесткость обусловлена присутствием гидрокарбонатов Са и Мg.
2. Некарбонатная (или постоянная жесткость) обусловлена присутствием сульфатов и хлоридов Са и Мg.
Способы ее устранения:
Карбонатная жесткость
а) кипячением
Са(НСО3)2 = СаСО3↓ +Н2О+СО2↑
б) действием известкового молока или соды
Са(ОН)2 +Са(НСО3)2 = 2СаСО3↓+2Н2О
Са(НСО3)2 +Nа2СО3 = СаСО3↓ +2NаНСО3
Некарбонатная жесткость
а) действием соды
СаSO4 + Nа2СО3 = СаСО3↓ + Nа2SО4
МgSО4 +Nа2СО3 = МgСО3↓ +Nа2SО4
70. Соединения железа в степени окисления +2: свойства, строение важнейших соединений, в том числе и лекарственных.
Оксид железа (II) FеО и гидроксид железа (II) Fе(OH)2
Вещества основного характера, легко взаимодействуют с кислотами:
FeO + H2SO4 = FeSO4 + Н2O
Fe(OH)2 + H2SO4 = FeSO4 + Н2O
Оксид железа (II) можно получить, восстанавливая оксид железа (III) водородом:
Fe2O3 + H2 = 2FeO + Н2О
Гидроксид железа (II) образуется при действии щелочей на растворы солей железа (II):
FеSО4 + 2NaOH = Fe(OH)2↓ + Na2SO4
Эта реакция должна протекать без доступа воздуха, т.к. гидроксид железа (II) легко окисляется до гидроксида железа (III):
4Fe(OH)2 + O2 + 2Н2О = 4Fе(ОН)3
Растворы солей железа(II) бесцветны.
Соли железа (II) под действием окислителей проявляют восстановительные свойства:
Если реакция проходит в кислой среде, то они переходят в соли железа (III)
10FeSO4 + 2KMnO4 + 8H2SO4 = 5Fe2(SO4)3 + 2МnSO4 + K2SO4 + 8Н2О
Качественная реакция на ионы железа (II):
3FeSO4 + 2K3[Fе(CN)6] = Fe3[Fе(CN)6]2↓(турнбулева синь) + 3K2SO4
В живых организмах железо является важным микроэлементом, катализирующим процессы обмена кислородом (дыхания).
В организме взрослого человека содержится около 3,5 грамма железа (около 0,02 %), из которых 75 % являются главным действующим элементом гемоглобина крови, остальное входит в состав ферментов других клеток, катализируя процессы дыхания в клетках.
Недостаток железа проявляется как болезнь организма (хлороз у растений и анемия у животных).
В организм животных и человека железо поступает с пищей (наиболее богаты им печень, мясо, яйца, бобовые, хлеб, крупы, свёкла).
71. Соединения железа в степени окисления +3: свойства, строение важнейших соединений, в том числе и лекарственных.
Оксид железа (III) Fе2O3 и гидроксид железа (ПI) Fе(ОН)3 (проявляют амфотерные свойства)
Fе2O3+ 6НСl = 2FеСl3 + ЗН2О
Fе2O3 + 2KOH = 2KFeO2 + Н2О (феррит калия, соль железистой кислоты НFeO2)
Fе(ОН)3+ 3НСl = FеСl3 + 3Н2О
Fе(ОН)3 + 3KOH = K3[Fе(ОН)6]
Гидроксид железа (III) можно получить действием щелочей на соли железа (III):
FеСl3 + 3КОН = Fе(ОН)3 + ЗKСI
При прокаливании Fе(ОН)3 образуется оксид железа (III):
2Fе(ОН)3 = Fе2O3+ 3Н2О
Растворы солей железа(III) имеют желтую окраску.
Соли железа (III) - слабые окислители.
Под действием восстановителей они переходят в соединения железа (II):
2FeCl3 + 2КI = 2FeCl2 + I2 + 2KCl
Качественная реакция на ионы железа (III):
4FeCl3 + 3K4[Fе(CN)6] = Fe4 [Fе(CN)6]3↓( берлинская лазурь) + 12KCl
Обнаружить ионы Fe3+ можно также по реакции с тиоцианатом калия KNCS или аммония NH4 NCS
FеСl3 + 3KNCS = Fe(NCS)3(кpoвaвo–красный раствор) + 3КСl
В живых организмах железо является важным микроэлементом, катализирующим процессы обмена кислородом (дыхания).
В организме взрослого человека содержится около 3,5 грамма железа (около 0,02 %), из которых 75 % являются главным действующим элементом гемоглобина крови, остальное входит в состав ферментов других клеток, катализируя процессы дыхания в клетках.
Недостаток железа проявляется как болезнь организма (хлороз у растений и анемия у животных).
В организм животных и человека железо поступает с пищей (наиболее богаты им печень, мясо, яйца, бобовые, хлеб, крупы, свёкла).
72. Соединения марганца в степени окисления +7.
Оксид марганца (VII)- Мn2O7 - проявляет кислотные свойства.
1. взаимодействие с водой:
Мn2O7 + Н2O = 2HМnO4
2. оксид марганца (VII) неустойчив и разлагается:
2Mn2O7 = 4MnO2 + 3O2
Получение Мn2O7:
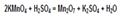
73. Соединения марганца в степени окисления +2, +4.
Оксид марганца (II) МnО и гидроксид Мn(ОН)2
Вещества основного характера, взаимодействуют с кислотами: MnO + 2НСl = MnCl2 + 2Н2O
Mn(OH)2 + 2НСl = MnCl2 + 2Н2O
Mn(OH)2 получают действием щелочей на растворимые соли Mn2+
MnCl2 + 2NaOH = Mn(OH)2 + 2Н2O
Из-за неустойчивости Mn(OH)2 уже на воздухе окисляется, образуя Mn(OH)4
2Mn(OH)2 +О2 + 2Н2O = 2Mn(OH)4
Оксид марганца (IV), или диоксид марганца, МпО2 и гидроксид Мn(ОН)4 (амфотерные вещества)
1. взаимодействие с кислотами
МnО2 + 2H2SO4 = Mn(SO4)2 + 2Н2O
2. сплавление с щелочамиМnО2 + 4KОН = K4MnO4 + 2Н2O (манганит калия - соль марганцеватистой кислоты Н4MnO4)
Оксид марганца (IV) может проявлять свойства как окислителя, так и восстановителя:
4НСl + МnО2 = МnCl2 + Cl2 + 2Н2O (как окислитель)
2МnO2 + 3РbО2 + 6НNО3 = 2НМnО4 + 3Рb(NО3)2 + 2Н2O (как восстановитель)
