Б. Количественное определение витамина Р в препаратах чайного листа
В группу витамина Р объединены соединения фенольной природы с высокой антиоксидантной активностью и способностью укреплять стенки кровеносных капилляров – флавоноиды. К наиболее распространённым флавоноидам относятся рутин (см. рис. ниже), кверцетин.
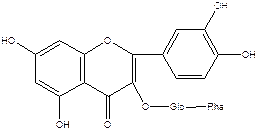
Рутин
Цель работы
Определить процентное содержание витамина Р в чайном листе и сравнить его с содержанием витамина С в картофеле.
Принцип метода
Водные растворы чайного листа титруют 0,02 М KMnO4 в присутствии индикатора индигокармина, так как экспериментально установлено, что 1 мл 0,02 М раствора KMnO4 окисляет 6,4 мкг рутина (витамина Р).
Выполнение работы
Предварительно навеску 0,25 г чая кипятят в 100 мл дистиллированной воды в течение 5 мин. Раствор охлаждают и фильтруют. В дальнейшем используют готовый раствор.
В две конические колбы приливают:
| Реактивы и этапы | Опыт | Контроль |
| Экстракт чая, мл | 2,0 | - |
| Н2О, мл | ||
| Индигокармин, мл | ||
| Титруют 0,02 М раствором KMnO4до появления желтой окраски (без розового оттенка) через переходные тона, мл |
Расчет содержания витамина Р (в %) производят по формуле:
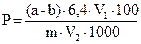 , где
, где
a и b - соответственно объемы 0,02 М KMnO4 (в мл), пошедшие на титрование опытной и контрольной пробы
6,4/1000 – пересчетный коэффициент на миллиграммы рутина
V1 – объем всего раствора чая (100 мл)
V2 – объем, взятый для титрования (2 мл)
m – навеска чая (250 мг)
Выводы
Тестовые задания по теме: «Витамины»
Ответить на каждый вопрос однозначно: «да» или «нет»
1. Каротин является предшественником витамина А.
2. Витамины Е и К представляют собой производные стеринов.
3. Викасол растворим в воде.
4. Кобальт входит в состав витамина В12.
5. Биотин (витамин Н) участвует в фиксации двуокиси углерода ферментами.
6. В состав флавинмононуклеотида (ФМН) входит витамин В2.
7. Участвует ли витамин К в процессе свертывания крови?
8. Известны ли антивитамины В1?
9. Входит ли витамин В6 в состав кофермента А?
10. Участвует ли фолиевая кислота в синтезе пуриновых нуклеотидов?
11. Известна ли точно суточная потребность витамина К для человека?
12. Достаточна ли для детей суточная доза витамина D в количестве 5 мкг?
2) Выбрать один правильный ответ
| В окислительно-восстановительных реакциях не участвует витамин: 1. РР 2. B2 3. A 4. H 5. C | При недостатке витамина D у взрослого человека развивается: 1. склероз 2. рахит 3. цинга 4. остеопороз 5. пеллагра |
3) Найти соответствие
| Витамин | Кофермент |
| 1. Тиамин 2. Никотиновая кислота 3. Пантотеновая кислота 4. Пиридоксин 5. Рибофлавин | А. НАД+, НАДФ+ Б. ТПФ В. ФМН, ФАД Г. ПФ Д. КоА |
3.2. Спектрофотометрическое определение НАДН(Н+) и расчёт чистоты коммерческого препарата
Пиридиннуклеотиды (НАД+, НАДФ+), входящие в качестве коферментов в состав более чем 150 так называемых «пиридинзависимых» дегидрогеназ, играют существенную роль в реакциях окисления-восстановления. Спектрофотометрическое определение образующихся восстановленных форм пиридиннуклеотидов позволяет следить за ходом ферментативной реакции, так как реакция протекает по схеме:
Субстрат + НАД+ ® Продукт реакции + НАДН + Н+ (закисление среды)
Цель работы
Определить чистоту коммерческого препарата НАДН(Н+) восстановленного, учитывая, что при хранении восстановленная форма частично превращается в окисленную.
Принцип метода
В основе метода лежит существенное отличие спектров оптического поглощения окисленной и восстановленной форм кофермента. Измеряя в ходе окислительно-восстановительной реакции оптическую плотность при 340 нм можно установить (зная коэффициент молярной экстинкции e и толщину кюветы) количество динуклеотида в пробе, а соответственно и количество прореагировавшего субстрата.
Спектры поглощения окисленной (сплошная линия) и восстановленной (пунктирная линия) форм никотинадениндинуклеотида в концентрации 10-4 М, рН 7,6
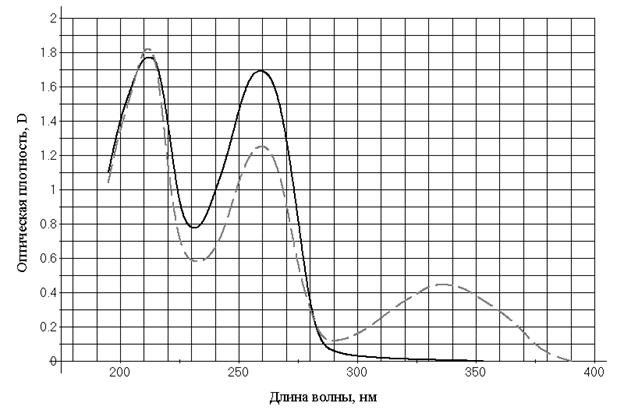
В расчетах исходят из величины коэффициента молярной экстинкции НАДН(Н+) при 340 нм в кювете толщиной 1 см e340 = 6220 М-1.см-1, измеряемой на специальных приборах – спектрофотометрах. ФЭК, к сожалению, не позволяет полностью воссоздать условия, необходимые для определения НАДН(Н+) описанным методом, так как не обеспечивает измерения при этой длине волны. Кроме того, студенческий практикум не оснащен кварцевыми кюветами, а стеклянные кюветы имеют значительное оптическое поглощение в ультрафиолетовой области спектра. Поэтому измерения проводят в более длинноволновой области при λ=366 нм, используя другую величину коэффициента молярной экстинкции НАДН(Н+)
(e366 = 3300 М-1.см-1).
Выполение работы
Навеску динатриевой соли НАДН(Н+) (М = 710 г.моль-1) 35,5 мг растворяют в 5 мл Н2О. Исходный раствор разводят в 50 раз (0,06 мл раствора довести в мерной пробирке дистиллированной водой до 3 мл), рассчитывают молярную концентрацию (с) полученного раствора НАДН(Н+) и измеряют оптическую плотность (D) при l=366 нм против дистиллированной воды в кюветах с длиной оптического пути l = 0,5 см.
Необходимо рассчитать чистоту препарата (т.е. содержание НАДН(Н+) в растворе), учитывая, что концентрация чистого вещества в растворе прямо пропорциональна оптической плотности этого раствора, и зная, что e366 = 3300 М-1.см-1.
Расчеты
Оптическая плотность полученного раствора НАДН(Н+) равна Dпракт.. Теоретически оптическая плотность данного раствора должна быть равной Dтеор = e . с . l. Зная коэффициент молярной экстинкции (e) и, зная молярную концентрацию разведенного раствора, находим Dтеор. Тогда чистота препарата Х, пропорциональная отношению величин оптической плотности, равна:
X = 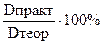
Выводы
Тестовые задания по теме по теме: «Липиды»
1) Ответить на каждый вопрос однозначно: «да» или «нет»
1. Липиды - гидрофильные соединения.
2. Пальмитиновая и олеиновая жирные кислоты содержат одинаковое число атомов углерода.
3. Холестериды - это сложные эфиры холестерина и высших жирных кислот.
4. В состав цереброзидов входит гексоза.
5. Кардиолипин относится к глицеролипидам.
6. Липиды в комплексе с белками выполняют транспортную функцию в организме.
7. Содержит ли арахидоновая кислота четыре двойные связи?
8. Является ли линоленовая кислота незаменимой для человека?
9. Содержат ли фосфатидилхолины атом азота?
10. Могут ли липиды выполнять каталитические функции?
11. Являются ли глицерофосфолипиды основными компонентами клеточных мембран?
12. Регулируют ли сфингенины и церамиды рост и дифференцировку клеток?
2) Выбрать один правильный ответ
| К глицерофосфолипидам не относятся: 1. лецитины 2. плазмалогены 3. кардиолипины 4. ганглиозиды 5. все вышеперечисленные соединения | Незаменимая жирная кислота: 1. олеопальмитиновая 2. стеариновая 3. олеиновая 4. линолевая 5. пальмитиновая |
3) Найти соответствие
| Транспортные формы липидов | % содержание белка |
| 1. хиломикроны 2. ЛПОНП 3. ЛПНП 4. ЛПВП 5. аполипопротеины | А. 100 Б. 45 В. 25 Г. 10 Д. 2 |
Влияние гормонов на содержание глюкозы в крови
Адреналин опосредованно, через рецепторы, усиливает в клетках печени распад гликогена, замедляя его синтез, в результате чего свободная глюкоза поступает из клеток в кровь. Концентрация глюкозы в крови повышается.
Инсулин в печени оказывает прямо противоположное действие на обмен глюкозы, но в первую очередь, он опосредованно, через рецепторы способствует быстрому поглощению глюкозы из крови жировой тканью и мышцами. Концентрация глюкозы в крови снижается.
Цель работы
Убедиться, что введение гормонов изменяет концентрацию глюкозы в крови животных.
Принцип метода
Моделирование биологического эксперимента с использованием лабораторных животных – кроликов.
Выполнение работы
Оцените свои наклонности и выберите для себя роль “хирурга”, “терапевта” или “аналитика”. Хирурги будут брать кровь из ушной вены кроликов в стерильных условиях. Терапевты – рассчитывать и вводить (стерильно) кроликам под кожу живота гормональные препараты. Аналитики – определять концентрацию глюкозы в крови животных до и после введения гормонов. Оценивать результаты будут все, занося полученные аналитиками экспериментальные данные в таблицу.
Следует отметить, что эксперимент не причиняет вреда кроликам при внимательном выполнении всех описанных ниже манипуляций, однако лучше использовать «виртуального» кролика или ограничиться демонстрацией (моделированием) всех ниже перечисленных процедур.
Двух кроликов (натощак) взвешивают, и пока “хирурги” в стерильных условиях берут кровь (1 каплю) из ушной вены кроликов, “терапевты” рассчитывают дозы гормональных препаратов: 1,5 МЕ инсулина и 0,35 мл 0,1% раствора адреналина на 1 кг массы кроликов. Результаты расчетов записываются на доске и проверяются преподавателем. При необходимости коммерческие препараты гормонов разводят стерильным физиологическим раствором. В это время “аналитики” определяют исходные концентрации глюкозы в крови каждого кролика с помощью глюкометра (см. раздел 4.2.Б), а “терапевты” вводят (в стерильных условиях) под кожу живота рассчитанную дозу инсулина одному кролику и адреналина - другому.
Через 30 минут после введения гормонов вновь берется кровь из другой ушной вены кроликов и повторно определяется концентрация глюкозы. Кролику, которому вводили инсулин, дают пить 40% раствор глюкозы.
| Концентрация глюкозы, ммоль/л | ||
| Кролик И (инсулин) | Кролик А (адреналин) | |
| До введения гормонов | ||
| Через 30 мин после введения гормонов | ||
| Разница |
Выводы
Тестовые задания по теме: «Гормоны»
1) Ответить на каждый вопрос однозначно: «да» или «нет»
1. К группе эйкозаноидов относятся: простагландины, простациклины, тромбоксаны и лейкотриены.
2. Гормоны способны регулировать деятельность отдельных ферментов или ферментных систем.
3. Биологическая активность гормонов проявляется при очень низких концентрациях в крови.
4. Альдостерон относится к глюкокортикоидам.
5. Вазопрессин - гормон передней доли гипофиза.
6. Тироксин может синтезироваться из тирозина.
7. Влияет ли деятельность гипофиза на функцию других желез внутренней секреции?
8. Известны ли гормоны циклопептидной структуры?
9. Можно ли синтезировать гормоны искусственным путем?
10. Эффективно ли пероральное применение инсулина?
11. Проникает ли адреналин в цитоплазму клеток?
12. Является ли арахидоновая кислота предшественником простагландинов?
13. Либерины и статины регулируют секрецию тропных гормонов гипофиза.
14. цАМФ и цГМФ - вторичные посредники пептидных гормонов.
15. Аденилатциклазная и протеинкиназная системы обеспечивают многократное усиление гормонального сигнала.
16. Фосфодиэстераза расщепляет циклические нуклеотиды.
17. Кальмодулин - это внутриклеточный Са-связывающий белок.
18. Стероидные гормоны проникают через плазматические мембраны и связываются с внутриклеточными рецепторами.
19. Обладают ли производные витамина D гормональной активностью?
20. Изменяет ли инсулин проницаемость клеточных мембран для глюкозы, аминокислот, ионов К+ и Са2+?
21. Связываются ли мембранные G-белки с ГТФ?
22. Эффективно ли применение инсулина как анаболитического средства при истощении организма?
23. Усиливают ли глюкокортикоиды глюконеогенез?
24. Относится ли инозитол-1,4,5-трифосфат к вторичным посредникам?
2) Выбрать один правильный ответ
| К гормонам пептидного строения нельзя отнести: 1. кальцитонин 2. окситоцин 3. тиролиберин 4. прогестерон 5. глюкагон | В регуляции липидного обмена не участвует: 1. адреналин 2. кортикотропин 3. инсулин 4. гидрокортизон 5. вазопрессин |
| Вторичные посредники гормонального сигнала: 1. диацилглицеролы 2. триацилглицеролы 3. лейкотриены 4. тромбоксаны 5. все вышеперечисленные соединения | К стероидным гормонам нельзя отнести: 1. кортизол 2. альдостерон 3. эстрадиол 4. тестостерон 5. кортикотропин |
3) Найти соответствие, установив последовательность участников передачи гормонального сигнала в клетку
| 1. 2. 3. 4. 5. | А. ц-АМФ Б. G-белок В. аденилатциклаза Г. мембранный рецептор Д. гормон |
3.4. Коллоквиум III по теме «Витамины, липиды, гормоны»
Вопросы, для самостоятельной подготовки
1. Понятие об авитаминозах, гипо- и гипервитаминозах как заболеваниях, связанных с нарушением функции ферментативных систем. Использование витаминов в качестве лечебных препаратов.
2. Витамины группы А. Строение и свойства. Биологическая роль. Провитамины А. Пищевые источники. Всасывание в кишечнике. Гипо- и гипервитаминоз. Суточная потребность.
3. Витамины группы D. Строение и свойства. Провитамины: эргостерин, 7-дегидрохолестерин. Пищевые источники. Биологическая роль. Гипо- и авитаминоз. Гипервитаминоз. Суточная потребность. Применение в клинике.
4. Витамины группы Е. Строение и свойства. Гипо- и авитаминоз. Пищевые источники. Применение в клинике.
5. Витамины группы К. Строение и биологическая роль. Применение в клинике.
6. Витамин В1 . Строение и свойства. Коферментная форма. Роль в обмене веществ. Гипо- и авитаминоз. Пищевые источники. Суточная потребность. Применение в клинике.
7. Витамин В2. Строение и свойства. Коферментные формы. Роль в обмене веществ. Пищевые источники. Суточная потребность.
8. Витамин В6. Строение и свойства. Коферментные формы. Гиповитаминоз. Пищевые источники. Суточная потребность.
9. Витамин В12. Химический состав. Роль в обмене веществ. Пищевые источники. Особенности всасывания. Применение в клинике.
10. Витамин С. Строение и свойства. Биологическая роль. Гипо- и авитаминоз. Применение в клинике. Суточная потребность.
11. Биотин. Строение и свойства. Гипо- и авитаминоз. Пищевые источники.
12. Витамин РР. Строение. Коферментные формы. Гипо- и авитаминоз. Пищевые источники. Роль в обмене веществ. Суточная потребность.
13. Фолиевая кислота. Строение. Распространение в природе. Участие в построении коферментов. Гипо- и авитаминоз.
14. Витамин В3. Строение. Биологическая роль. Суточная потребность.
15. Химия липидов. Строение, классификация, биологическая роль, транспорт в организме.
16. Глицерофосфолипиды и сфинголипиды. Строение и биологическая роль.
17. Биологическая роль стеринов. Химическое строение желчных кислот и их роль в переваривании и всасывании липидов.
18. Химия высших жирных кислот. Строение и биологическая роль.
19. Общие представления о гормонах. Иерархия гормонов. Агонизм и антагонизм их действия.
20. Роль гормонов в регуляции обмена веществ. Механизмы передачи гормонального сигнала.
21. Гормоны мозгового вещества надпочечников. Их синтез и распад. Механизм действия. Роль в регуляции обмена веществ.
22. Гормоны щитовидной железы. Их строение и образование в организме. Гипо- и гипертиреозы.
23. Гормоны поджелудочной железы. Их химическая природа и влияние на обмен веществ. Инсулин и глюкагон.
24. Гормоны стероидной природы. Их строение и механизм действия. Мужские и женские половые гормоны.
25. Гормоны коры надпочечников. Химическая природа и влияние на обмен веществ. Механизм действия.
26. Пути образования и биологическая роль простагландинов, лейкотриенов и тромбоксанов.
27. Гормоны передней доли гипофиза. Химическое строение, биологическое действие.
28. Гормоны гипоталамуса. Строение и биологическая роль.
29. Примеры передачи гормонального сигнала посредством белковых рецепторов. Понятие о G-белках и вторичных посредниках.
30. Гормоны, проникающие внутрь клетки. Внутриклеточные и внутриядерные рецепторы. Регуляция транскрипции.
Варианты письменной части коллоквиума
| 1. Привести характерные симптомы витаминной недостаточности: 1. A 2. K 3. E 4. D 2. Написать формулу кофермента и показать его участие в обменных процессах для витамина: 1. B1 (тиамина) 2. B3 (пантотеновой кислоты) 3. B6 (пиридоксаля) 4. фолиевой кислоты 3. Привести конкретный пример и объяснить функцию: 1. глицерофосфолипида 2. сфинголипида 3. гликолипида 4. стероида | 4. Перечислить участников передачи гормонального сигнала для: 1. адреналина 2. глюкагона 3. стероидных гормонов 4. трийодтиронина 5. Указать основные физиологические эффекты действия: 1. простагландинов 2. кортизола 3. адреналина 4. инсулина 5. Наиболее полно перечислить гормоны: 6. гипофиза 7. поджелудочной железы 8. щитовидной железы 9. коры надпочечников |
Варианты заданий на компьютерном тестировании
Инструкция к тесту: Выбрать все правильные ответы
| 1. Причинами гиповитаминозов могут быть 1. недостаток витамина в пище 2. нарушение транспорта витамина 3. нарушение синтеза кофермента из витамина 4. генетические дефекты апофермента 2. Витамин, суточная потребность в котором для человека наибольшая 1. А 2. В1 3. РР 4. D 5. Е 3. Витамины, содержащие гетероциклы в своей структуре 1. токоферолы 2. холекальциферол 3. пиридоксин 4. ниацин (РР) 5. пантотеновая кислота 4. Витамины, необходимые для переноса атомов водорода 1. тиамин 2. рибофлавин 3. фолиевая кислота 4. никотинамид 5. биотин 5. В состав кофермента А входит витамин 1. В1 2. В2 3. В3 4. В6 5. В12 6. Ингибитором фосфодиэстеразы, разрушающей цАМФ, является 1. АТФ 2. кофеин 3. аспирин 4. NO (оксид азота) 5. цГМФ 6. Кофермент присоединяется к апоферменту 7. в аллостерическом центре 8. в активном центре 9. разнообразными химическими связями 10. всегда очень прочно 8. Насыщенные жирные кислоты 1. олеиновая 2. арахиновая 3. линоленовая 4. пальмитиновая 5. арахидоновая 9. Стероидами являются 1. половые гормоны 2. глюкокортикоиды 3. токоферолы 4. холестерин 5. трииодтиронин 10. В состав клеточных мембран не могут входить 1. глицерин 2. триациглицерины 3. холестерин 4. белки фосфатидилхолин 11. Кальмодулин – это 1. глицерофосфолипид 2. гормон щитовидной железы 3. внутриклеточный Ca-связывающий белок 4. предшественник кальциферола 5. белок сыворотки крови 12. Протеинкиназа С активируется 1. ТАГ 2. МАГ 3. ДАГ 4. ионами Ca2+ 5. цАМФ 13. Недостаток витамина D у взрослого человека может вызвать 1. рахит 2. остеопороз 3. ксерофтальмию 4. макроцитарную анемию 5. цингу 14. Витамин, суточная потребность в котором для человека наименьшая 1. А 2. В1 3. С 4. D 5. Е 15. Витамины, не содержащие гетероциклы в своей структуре 1. ретинол 2. пиридоксин 3. холекальциферол 4. рибофлавин 5. тиамин 16. Витамин, необходимый для переноса аминогрупп 1. пиридоксин 2. рибофлавин 3. тиамин 4. филлохинон 5. никотинамид 17. Антиоксидантами считают витамины 1. Н 2. В6 3. А 4. Е 5. С 18. Аденилатциклаза 1. мембранный фермент 2. цитоплазматический фермент 3. активируется G-белками 4. катализирует образование цАМФ 5. содержит гемм 19. Специфичность действия холофермента определяется 1. липидной простетической группой 2. углеводной простетической группой 3. апоферментом 4. коферментом 5. всеми вышеперечисленными факторами 20. Ненасыщенные жирные кислоты 1. пальмитиновая 2. олеиновая 3. стеариновая 4. арахиновая 5. арахидоновая 21. К стероидам относятся 1. эстрон 2. токоферол 3. менахинон 4. тестостерон 5. трииодтиронин 22. Глицерофосфолипид, не имеющий положительного заряда 1. фосфатидилинозитол 2. фосфатидилэтаноламин 3. фосфатидилхолин 23. Стероидные гормоны 1. проникают в клетку 2. связываются с мембранными рецепторами 3. активируют G-белки 4. стимулируют синтез мРНК 5. участвуют во всех вышеперечисленных процессах 24. К кортикостероидам не относятся 1. кортизон 2. кортиколиберин 3. кортикотропин 4. гидрокортизон 5. альдостерон 25. При недостатке витамина B1 развивается 1. склероз 2. рахит 3. пеллагра 4. цинга 5. бери-бери 26. Потребность в каком витамине увеличивается с возрастом и при тяжелой физической работе 1. B1 2. B2 3. B6 4. B12 5. D 27. Какая пара витаминов содержит атом серы в своем составе 1. тиамин и биотин 2. тиамин и фолиевая кислота 3. пиридоксин и биотин 4. биотин и рибофлавин 28. Витамин, который необходим для переноса CO2-групп 1. тиамин 2. биотин 3. кобаламин 4. пиридоксин 5. аскорбиновая кислота 29. В обмене Ca2+ участвуют 1. витамин Н 2. витамин К 3. витамин D 4. кальцитонин 5. паратгормон 30. Оксид азота (NO) 1. биологически активная молекула 2. синтезируется из лизина 3. синтезируется из аргинина 4. оказывает длительный эффект 31. Коферментом дегидрогеназ могут быть 1. НАД+ 2. ФАД 3. пиридоксин 4. биотин 5. КоА 32. К стеринам относятся 1. ретинол 2. филлохинон 3. токоферолы 4. все вышеперечисленные соединения 5. ни одно из вышеперечисленных соединений 33. Компонентом клеточных мембран не могут быть 1. сфингомиелины 2. цереброзиды 3. белки 4. ТАГ 5. Лецитины 34. Вторичными посредниками в передаче гормонального сигнала могут быть 1. гормон 2. цАМФ 3. мембранные рецепторы 4. ДАГ 5. аденилатциклаза 35. Действие каких гормонов опосредовано G-белками? 1. адреналина 2. норадреналина 3. трииодтиронина 4. гидрокортизона 5. глюкагона 36. Нарушение синтеза коллагена наблюдается при недостаточности витамина 1. E 2. А 3. К 4. С 5. D 37. Витамины, для которых хорошо известны случаи гипервитаминоза 1. B1 2. С 3. D 4. Е 5. А 38. Витамин, содержащий в своей молекуле атом металла 1. B1 2. B2 3. B3 4. B6 5. B12 | 39. Витамин, в составе кофермента переносящий один атом водорода и два электрона 1. тиамин 2. биотин 3. рибофлавин 4. ниацин (РР) 5. пиридоксин 40. Ретиноевая кислота – активная форма витамина 1. А 2. С 3. D 4. Е 5. К 41. Протеинкиназы 1. фосфорилируют белки 2. активируются вторичными посредниками передачи гормонального сигнала 3. дефосфорилируют белки 4. синтезируют цАМФ 5. ингибируются кофеином 42. Коферментом аминотрансфераз служит 1. ФАД 2. ТПФ 3. ПФ 4. биоцитин 5. КоА 43. Незаменимые жирные кислоты 1. линолевая 2. линоленовая 3. арахидоновая 4. арахиновая 5. олеиновая 44. К стероидам не относятся 1. провитамины D 2. гормоны коры надпочечников 3. тиреотропин 4. либерины и статины 5. половые гормоны 45. Остаток глицерина содержат 1. лецитины 2. плазмалогены 3. кардиолипины 4. ганглиозиды 5. церамиды 46. В передаче сигнала пептидных гормонов участвуют 1. G-белки 2. аденилатциклаза 3. внутриклеточные рецепторы 4. протеинкиназы 5. цАМФ 47. GS-белок 1. состоит из трех субъединиц 2. связан с ГДФ 3. ингибирует аденилатциклазу 4. мембранный белок 5. активирует ДНК 48. Водорастворимые витамины 1. ретинол 2. никотиновая кислота 3. кобаламин 4. токоферол 5. биотин 6. филлохинон 49. Водорастворимые витамины 1. рибофлавин 2. ретинол 3. токоферол 4. кальциферол 5. филлохинон 6. пантотеновая кислота 50. Жирорастворимые витамины 1. пиридоксин 2. тиамин 3. ретинол 4. филлохинон 5. фолиевая кислота 6. рутин 51. Коферментная форма витамина B1 1. ТПФ 2. НАД+ 3. ФАД 4. ПФ 5. КоА 52. Коферментные формы витамина B2 1. ТПФ 2. НАД+ 3. ФАД 4. ПФ 5. ФМН 53. Коферментные формы витамина РР 1. ТПФ 2. НАД+ 3. ПФ 4. НАДФ+ 5. КоА 54. Коферментная форма витамина B6 1. ТПФ 2. НАД 3. ПФ 4. ФАД 5. КоА 55. Каротин – предшественник витамина 1. ретинола 2. биотина 3. токоферола 4. рибофлавина 5. филлохинона 56. В процессе свертывания крови участвует витамин 1. А 2. D 3. Е 4. К 5. РР 57. Фолиевая кислота (витамин Bc) участвует в 1. зрительном процессе 2. процессе свертывания крови 3. обмене кальция и фосфора 4. транспорте СО2 5. синтезе пуриновых нуклеотидов 58. Биотин (витамин Н) участвует исключительно в реакциях 1. гидроксилирования 2. трансаминирования 3. дезаминирования 4. карбоксилирования 5. трансметилирования 59. Стероидные гормоны в комплексе с внутриклеточными рецепторами стимулируют 1. репликацию ДНК 2. деградацию белков 3. транскрипцию специфических генов 4. диссоциацию рибосом 5. синтез цАМФ 60. Тиреолиберин – гормон 1. гипофиза 2. гипоталамуса 3. щитовидной железы 4. паращитовидной железы 5. эпифиза 61. Антагонисты инсулина 1. глюкагон 2. кортикотропин 3. адреналин 4. альдостерон 5. соматостатин 62. Биотин и пиридоксальфосфат соединяются с белком через аминокислоту 1. глицин 2. лейцин 3. изолейцин 4. лизин 5. аргинин 63. Авидин связывает витамин 1. рутин 2. ниацин 3. биотин 4. ретинол 5. рибофлавин 64. В растительной пищи полностью отсутствует витамин 1. биотин 2. тиамин 3. кобаламин 4. фолиевая кислота 5. пантотеновая кислота 65. В карбоксилировании остатков глутаминовой кислоты в протромбине участвует витамин 1. С 2. D 3. Е 4. К 5. А 66. Гормональная форма витамина D 1. кальциферол 2. кальцитриол 3. кальцитонин 4. кальмодулин 5. паратгормон 67. Добавление масла к растительной пище способствует всасыванию витамина 1. тиамина 2. биотина 3. рибофлавина 4. аскорбиновой кислоты 5. ретинола 68. Липиды, содержащие остаток фосфорной кислоты 1. МАГ 2. ДАГ 3. ТАГ 4. фосфатидные кислоты 5. простагландины 69. Линолевая кислота согласно номенклатуре обозначается 1. 18 : 1 w 9 2. 18 : 2 w 6 3. 18 : 3 w 3 4. 18 : 0 5. 20 : 4 w 6 70. Церамиды – это 1. витамины 2. гормоны 3. углеводы 4. липиды 5. коферменты 71. Гормоны гипофиза тиролиберин 1. тироксин 2. тиротропин 3. соматостатин 4. соматотропин 72. Гормоны липидной природы 1. адреналин 2. андростерон 3. глюкагон 4. кортизол 5. окситоцин 73. Пептидные гормоны 1. кальцитриол 2. андростерон 3. глюкагон 4. кортизол 5. окситоцин 74. Гормоны – производные аминокислот 1. адреналин 2. андростерон 3. норадреналин 4. кортизол 5. кальцитриол 75. В ядро клетки проникают 1. глюкагон 2. кальцитриол 3. кортизол 4. кортикотропин 5. адреналин 76. С мембранными рецепторами на поверхности клетки связываются 1. глюкагон 2. кальцитриол 3. кортизол 4. инсулин 5. адреналин |
Правильные ответы
| 1.1, 2, 3, 4 2.3 3.1, 3, 4 4.2, 4 5.3 6.2 7.2, 3 8.2, 4 9.1, 2, 4 10.1, 2 11.3 12.3, 4 13.2 14.4 15.1, 3 16.1 17.3, 4, 5 18.1, 3, 4 19.3 20.2, 5 21.1, 4 22.1 23.1, 4 24.2, 3 25.5 | 26.2 27.1 28.2 29.3, 4, 5 30.1, 3 31.1, 2 32.5 33.4 34.2, 4 35.1, 2, 5 36.4 37.3, 5 38.5 39.4 40.1 41.1, 2 42.3 43.1, 2, 3 44.3, 4 45.1, 2, 3 46.1, 2, 4, 5 47.1, 2, 4 48.2, 3, 5 49.1, 6 50.3, 4 | 51.1 52.3, 5 53.2, 4 54.3 55.1 56.4 57.5 58.4 59.3 60.2 61.1, 2, 3, 5 62.4 63.3 64.3 65.4 66.2 67.5 68.4 69.2 70.4 71.3, 5 72.2, 4 73.3, 5 74.1, 3 75.2, 3 76.1, 4, 5 |
Раздел 4: Метаболизм. Биоэнергетика клеток. Химия и обмен углеводов
Введение
Метаболизм – совокупность процессов превращения веществ и энергии в живом организме и обмен организма веществами и энергией с внешней средой, вследствие чего происходит постоянное обновление самого организма. С точки зрения физики живой организм существует за счет увеличения энтропии внешней среды в соответствии со вторым законом термодинамики: DG = DH - TDS, то есть (DSорганизма + DSсреды) > 0, тогда DG< 0 и в самом организме могут происходить упорядоченные процессы.
Организм получает энергию в виде пищевых веществ, расщепляя которые в окислительных процессах катаболизма («метаболическая воронка») трансформирует часть этой энергии в высокоэнергетические (макроэргические) соединения (большей частью в АТФ[††]). Последние, в свою очередь, используются организмом в восстановительных процессах анаболизма в качестве источника энергиидля синтеза собственных высокомолекулярных соединений.
Внутриклеточный метаболизм основных классов питательных веществ – углеводов, белков и жиров – представляет собой разветвленную метаболическую сеть, объединяемую в митохондриях общим амфиболическим путем – циклом трикарбоновых кислот (ЦТК), метаболиты которого участвуют в анаплеротических (восполняющих) реакциях, связывающих обмен разных классов соединений между собой.
Образование АТФ из АДФ и фосфорильного остатка – ферментативный энергозависимый процесс, получивший название фосфорилирование АДФ. В зависимости от источника энергии и механизма образования макроэргической связи различают два основных способа синтеза АТФ:
1) меньший по объему, эволюционно более ранний, который может осуществляться в анаэробных условиях – субстратное фосфорилирование за счет энергии других макроэргических соединений (1,3-бисфосфоглицерат, фосфоенолпируват, сукцинил-КоА, креатинфосфат);
2) сопряженное с дыханием окислительное фосфорилирование, осуществляемое на внутренней мембране митохондрий ферментом АТФ-синтазой за счет энергии разности электрохимических потенциалов DmН+, возникающей при раздельном переносе электронов и протонов в дыхательной цепи митохондрий от восстановительных эквивалентов НАДН(Н+) или ФАДН2 на молекулярный кислород в процессе биологического окисления (хемиосмотическая теория П. Митчелла).
Поскольку в организме человека и животных основное количество восстановительных эквивалентов образуется в результате окислительного распада углеводов, целесообразно начать знакомство с обменом веществ и энергии с изучения химии углеводов и их метаболизма. Метаболизм углеводов составляют катаболические энергообразующие пути (гликолиз, гликогенолиз, петозофосфатный путь окисления глюкозы) и анаболические энергозатратные пути (синтез гликогена и глюконеогенез – образование глюкозы из неуглеводных источников: лактата, аминокислот или глицерина).
Направленность, интенсивность и согласованность протекания метаболических процессов регулируется ферментами под контролем гормональной и нервной системы при участии клеточных рецепторов и вторичных переносчиков сигнала. Нарушение регуляции, как и онтогенетические изменения ферментных систем, приводят к патологии обменных процессов и развитию заболеваний.
В данном разделе приводятся лабораторные работы, демонстрирующие специфичность ферментов, расщепляющих углеводы, методы количественного определения глюкозы и построения «сахарных кривых», кроме того, представлены методики определения активности фермента ЦТК - сукцинатдегидрогеназы и метаболита гликолиза - пирувата.
4.1. Специфичность действия ферментов распада углеводов: амилазы и сахаразы
Крахмал и сахароза – обычные углеводы пищи. Амилаза и сахараза – ферменты, участвующие в расщеплении этих углеводов. Амилаза слюны расщепляет крахмал до мальтозы и, затем, мальтаза расщепляет последнюю до свободной глюкозы. Сахараза кишечного сока расщепляет сахарозу до глюкозы и фруктозы. Источником ферментов могут быть слюна (для амилазы) и пекарские дрожжи (для сахаразы).
Цель работы
Убедиться в специфичности действия амилазы слюны и сахаразы дрожжей на соответствующие субстраты.
Принцип метода
Следят за расщеплением крахмала и сахарозы по образованию глюкозы, которую определяют пробой Троммера (модификация пробы «медного зеркала» на альдегидную группу). Крахмал и сахароза не содержат способной окисляться альдегидной группы и не дают положительной пробы Троммера при нагревании.
Выполнение работы
Слюну разводят 1:5 и полученный раствор используют как источник амилазы. Получение сахаразы осуществляют следующими образом: 10 г пекарских дрожжей тщательно растирают в ступке, добавляют 15 мл воды, перемешивают, фильтруют через складчатый бумажный фильтр. Полученный фильтрат используют как источник фермента.
В 4 пробирки по каплям добавляют следующие реактивы:
| №№ проб | Крахмал | Сахароза | Амилаза | Сахараза | Окраска в реакции Троммера на наличие глюкозы |
| 10 капель | - | 5 капель | - | ||
| 10 капель | - | - | 5 капель | ||
| - | 10 капель | 5 капель | - | ||
| - | 10 капель | - | 5 капель |
Пробы перемешивают и инкубируют при 40°С в течение 10 мин, а затем проводят реакцию Троммера с содержимым каждой пробирки. Результаты записывают в таблицу.
