САМОСТІЙНА АУДИТОРНА РОБОТА. ТЕМА: Оптичні методи аналізу
ТЕМА: Оптичні методи аналізу. Фотометричний та спектрофотометричний метод кількісного аналізу. Фотоколориметричне визначення міді та феруму (III) у препаратах.
АКТУАЛЬНІСТЬ:Фотоколориметричний метод кількісного аналізу характеризується високою чутливістю, селективністю, експресністю, об’єктивністю, можливістю автоматизації і комп’ютеризації процесу аналізу. Все це зумовлює широке використання даного методу в аналітичній та фармацевтичній практиці.
НАВЧАЛЬНІ ЦІЛІ: Сформувати знання принципів і класифікації оптичних методів аналізу, теоретичних основ молекулярно-абсорбційних методів і вміння застосовувати їх в кількісному аналізі.
ЗНАТИ: -техніку виконання операцій в фотоколориметричному методі
аналізу;
-розрахунки процентного вмісту досліджуваної речовини за
результатами аналізу;
-класифікацію та загальну характеристику оптичних методів аналізу;
-поділ інстументальних методів на групи;
-теоретичні основи фотометричних методів;
-схему будови і принцип дії фотоколориметра;
-закони світлопоглинання.
ВМІТИ:-проводити і обгрунтовувати вибір фотометричної реакції для
конкретного випадку;
-проводити вимірювання оптичної густини розчинів;
-готувати серію стандартних розчинів для побудови
калібрувального графіка;
-будувати калібрувальний графік на основі оптичної густини серії
стандартних розчинів;
-кількісно визначати речовини, які застосовуються у фармації,
методом фотоколориметрії;
-розраховувати основні характеристики світлопоглинання;
-вибирати світлофільтри для роботи;
-робити висновки з результатів аналізу і оформляти їх у
вигляді протоколу.
САМОСТІЙНА ПОЗААУДИТОРНА РОБОТА
1.Суть методу фотоколориметрії.
2.Закон Бугера-Ламберта-Бера та причини відхилень від нього. Відповідь обгрунтуйте та запишіть.
3.Будова фотоколориметра й принцип його роботи.
4.Методи визначення концентрації досліджуваної речовини в фотоколориметрії.
5.Яка природа і властивості електромагнітного випромінювання? Що таке довжина хвилі та інтенсивність випромінювання? Відповідь обгрунтуйте та запишіть.
6.Спектр електромагнітного випромінювання: яку область довжин хвиль він охоплює; які довжини хвиль відповідають мікрохвильовій, ІЧ-, видимій та УФ-областям спектру?
7.Кількісне визначення речовин у розчинах фотоколориметричним методом дослідження.
8.Для комплексу купруму з органічним реагентом одержано наступні результати:
| Довжина хвилі, нм | D | Довжина хвилі, нм | D |
| 0,245 | 0,615 | ||
| 0,310 | 0,490 | ||
| 0,395 | 0,310 | ||
| 0,485 | 0,102 | ||
| 0,588 | 0,020 | ||
| 0,615 | 0,010 |
Вкажіть довжину хвилі, найбільш придатну для фотометричного визначення купруму по реакції з даним реагентом.
КОНТРОЛЬНІ ПИТАННЯ
1.Можливості фотоколориметричного методу аналізу.
2.Оптимальні умови фотоколориметричних визначень. Відповідь обґрунтуйте та запишіть.
3.Наведіть приклади фотоколориметричних визначень, напишіть відповідні реакції.
4.Якого типу реакції використовують у фотометричному аналізі для отримання забарвлених сполук?
5.Які вимоги до фотометричних реакцій?
6.Закон Бугера-Ламберта-Бера. Фізичний зміст величин, що входять в нього. Відповідь обґрунтуйте та запишіть.
7.Апаратура, що застосовується у фотоколориметричному методі аналізу. Яка принципова схема цих приладів?
8.В чому полягає фотометричне визначення Cu (II) в купрум сульфаті? Чому визначення не можна проводити на основі власного забарвлення CuSO4•5H2O?
9.Практичне значення методу фотоколориметрії.
10.Способи монохроматизації світла, світлофільтри.
11.Як визначити максимум світлопоглинання?
12.В якому інтервалі значень оптичної густини рекомендується працювати у фотоколориметричному методі?
13.Вибір світлофільтрів та кювет у фотометричному методі аналізу. Відповідь обгрунтуйте та запишіть.
14.Що таке абсорбційність і від чого вона залежить?
15.Як класифікують оптичні методи в залежності від способу реєстрації сигналу?
16.Як підбирають світлофільтр при визначенні йонів феруму? Відповідь обгрунтуйте та запишіть.
17.Які фактори впливають на поглинання світлового випромінювання? Як залежить світлопоглинання від природи речовини, концентрації, товщини поглинаючого шару?
18.Пропускання забарвленого розчину при 535 нм дорівнює 0,68. Розрахуйте оптичну густину цього розчину.
19.Оптична густина досліджуваного розчину дорівнює 63,2 %. Яке пропускання Т цього розчину в процентах?
20.Обчисліть питомий і молярний коефіцієнт поглинання розчину купруму (II) аміакату, якщо у розчині міститься 9,6 мг/дм3 Сu2+ і при вимірюванні у кюветі товщиною 2 см одержана оптична густина 0,127.
21.Для забарвленого комплексу цинку при 465 нм з товщиною кювети 1 см одержані наступні результати:
| № досліду | [Zn2+], г/см3 | Оптична густина |
| 0,002 | 0,105 | |
| 0,004 | 0,205 | |
| 0,006 | 0,310 | |
| 0,008 | 0,415 | |
| 0,010 | 0,515 |
Для отриманих даних:
а) побудуйте калібрувальний графік;
б) знайдіть питомий та молярний коефіцієнти поглинання;
в) визначте процентну концентрацію відповідного розчину, пропускання якого дорівнює 45 %.
22.Наважку калію дихромату масою 0,1471 г розчинили в 100 см3 дистильованої води і довели об’єм дистильованою водою до 500 см3. Виміряли при довжині хвилі 350 нм оптичну густину розчину, яка дорівнювала 0,736 при товщині поглинаючого шару 1 см. Розрахувати молярний та питомий коефіцієнти поглинання калію дихромату при даній довжині хвилі.
23.Розрахувати концентрацію розчину, який вміщує йони Fe3+ за наступними даними: до 1 см3 розчину додали ацетон, розчин амонію роданіду і воду до 100 см3. Колориметрування проводилось в кюветі товщиною 2 см. Оптична густина (при 480 нм) забарвленого розчину дорівнювала 0,75, молярний коефіцієнт світлопоглинання 14000.
САМОСТІЙНА АУДИТОРНА РОБОТА
1.Ознайомитись з методом фотоколориметрії за допомогою дослідів, описаних в даних методичних вказівках.
2.Виготовляти серії стандартних розчинів в методі фотоколориметрії.
3.Виконати лабораторні роботи, вказані в цих методичних матеріалах.
4.Оформити та захистити протокол.
5.Відповідати на запитання, запропоновані викладачем, з використанням записів на дошці.
6.Розв'язувати розрахункові задач, запропоновані викладачем.
Фотоколориметрія
У фотоколориметрії використовують хімічні реакції, при яких визначувана речовина переходить у забарвлену сполуку, що приводить до зміни кольору розчину. Вимірювання світлопоглинання такого забарвленого розчину здійснюють за допомогою фотоелемента. Порівняння інтенсивності забарвлення досліджуваної речовини з інтенсивністю забарвлення розчину відомої концентрації дає можливість визначення вмісту забарвленої речовини в досліджуваному розчині.
Ступінь поглинання світла знаходиться в прямій залежності від концентрації забарвленого компонента і від товщини забарвленого шару. Ця залежність називається законом поглинання світла (закон Бугера-Ламберта-Бера) і виражається рівнянням:
I=І0· 10-ЕCℓ
де І - інтенсивність світлового потоку, що пройшов через розчин;
І0 - інтенсивність падаючого світла;
Е - коефіцієнт поглинання – постійна величина, характерна для кожної речовини і залежить від її природи;
С - концентрація забарвленої речовини в розчині, моль/дм3;
ℓ - товщина кювети, см.
Поглинання світла виражають величиною абсорбційності або оптичною густиною D:
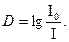
Якщо прологарифмувати рівняння закону Бугера-Ламберта-Бера і змінити знаки на обернені, то рівняння набирає вигляд:
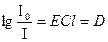
Із цього рівняння видно, що оптична густина розчину прямо пропорційна концентрації забарвленої речовини й товщині шару розчину.
Таким чином, щоб виміряти концентрацію (С) забарвленого розчину, необхідно визначити його оптичну густину, тобто інтенсивність світлового потоку.
Визначення ведуть за схемою:
1.Готують серію стандартних розчинів;
2.Підбирають кювети й світлофільтр;
3.Вимірюють адсорбційність всіх стандартних розчинів;
4.Будують калібрувальний графік розчинів.
5.Готують досліджуваний розчин.
6.Вимірюють абсорбційність досліджуваного розчину.
7.За допомогою калібрувального графіку знаходять вміст йону в досліджуваному розчині.
