Признаки и условия течения химических реакций

В промышленности подбирают такие условия, чтобы осуществлялись нужные реакции, а вредные замедлялись.
ТИПЫ ХИМИЧЕСКИХ РЕАКЦИЙ
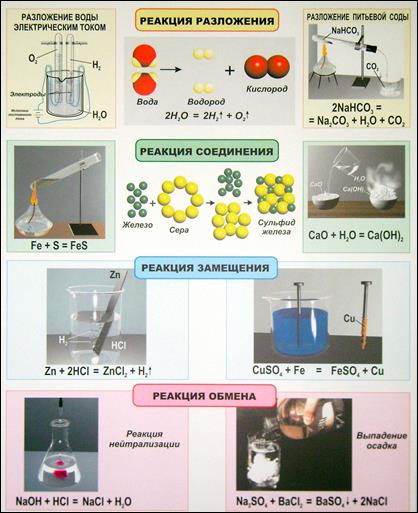
В таблице 12 приведены основные типы химических реакций по числу участвующих в них частиц. Даны рисунки и уравнения часто описываемых в учебниках реакций разложения, соединения, замещения и обмена.
В верхней части таблицы представлены реакции разложения воды и гидрокарбоната натрия. Изображён прибор для прохождения через воду постоянного электрического тока. Катод и анод представляют собой металлические пластинки, погружённые в воду и соединённые с источником электрического тока. В связи с тем, что чистая вода практически не проводит электрический ток, к ней добавляют небольшое количество соды (Nа2СО3) или серной кислоты (Н2SО4). При прохождении тока на обоих электродах происходит выделение пузырьков газа. В трубке, где собирается водород, объём оказывается вдвое большим, чем в трубке, где собирается кислород (о его наличии можно удостовериться с помощью тлеющей лучинки). Модельная схема демонстрирует реакцию разложения воды. Химические (ковалентные) связи между атомами в молекулах воды разрушаются, и из освобождающихся атомов образуются молекулы водорода и кислорода.
Модельная схема реакции соединения металлического железа и молекулярной серы S8 показывает, что в результате перегруппировки атомов в процессе реакции образуется сульфид железа. При этом разрушаются химические связи в кристалле железа (металлическая связь) и молекуле серы (ковалентная связь), а освободившиеся атомы соединяются с образованием ионных связей в кристалл соли.
К другой реакции соединения относится гашение извести СаО водой с образованием гидроксида кальция. При этом жжёная (негашёная) известь начинает разогреваться и образуется рыхлый порошок гашёной извести.
К реакциям замещения относят взаимодействие металла с кислотой или солью. При погружении достаточно активного металла в сильную (но не азотную) кислоту выделяются пузырьки водорода. Более активный металл вытесняет менее активный из раствора его соли.
Типичными реакциями обмена является реакция нейтрализации и реакция между растворами двух солей. На рисунке показано получение осадка сульфата бария. За ходом реакции нейтрализации следят с помощью индикатора фенолфталеина (малиновая окраска исчезает).
Таблица 12
Типы химических реакций
ВОЗДУХ. КИСЛОРОД. ГОРЕНИЕ
Кислород является самым распространённым химическим элементом на Земле. Содержание его в земной коре и гидросфере представлено в таблице 2 "Распространённость химических элементов". На долю кислорода приходится примерно половина (47 %) массы литосферы. Он является преобладающим химическим элементом гидросферы. В земной коре кислород присутствует только в связанном виде (оксиды, соли). Гидросфера также представлена в основном связанным кислородом (часть молекулярного кислорода растворена в воде).
В атмосфере свободного кислорода содержится 20,9 % по объёму. Воздух – сложная смесь газов. Сухой воздух на 99,9 % состоит из азота (78,1 %), кислорода (20,9 %) и аргона (0,9 %). Содержание этих газов в воздухе практически постоянно. В состав сухого атмосферного воздуха также входят диоксид углерода, неон, гелий, метан, криптон, водород, оксид азота(I) (оксид диазота, гемиоксид азота – N2О), озон, диоксид серы, монооксид углерода, ксенон, оксид азота(IV) (диоксид азота – NО2).
Состав воздуха определил французский химик Антуан Лоран Лавуазье в конце XVIII века (таблица 13). Он доказал содержание кислорода в воздухе, и назвал его "жизненный воздух". Для этого он нагревал на печи ртуть в стеклянной реторте, тонкая часть которой поводилась под стеклянный колпак, опущенный в водяную баню. Воздух под колпаком оказывался замкнутым. При нагревании ртуть соединялась с кислородом, превращаясь в оксид ртути красного цвета. "Воздух", оставшийся в стеклянном колпаке после нагревания ртути, не содержал кислорода. Мышь, помещённая под колпак, задыхалась. Прокалив оксид ртути, Лавуазье снова выделил из него кислород и вновь получил чистую ртуть.
Содержание кислорода в атмосфере стало заметно увеличиваться около 2 млрд. лет назад. В результате реакции фотосинтеза поглощался некоторый объём углекислого газа и выделялся такой же объём кислорода. На рисунке таблицы схематически показано образование кислорода при фотосинтезе. В процессе фотосинтеза в листьях зелёных растений, содержащих хлорофилл, при поглощении солнечной энергии происходит превращение воды и углекислого газа в углеводы (сахара) и кислород. Реакцию образования глюкозы и кислорода в зелёных растениях можно записать в следующем виде:
6Н2О + 6СО2 = С6Н12О6 + 6О2↑.
Образующаяся глюкоза превращается в нерастворимый в воде крахмал, который накапливается в растениях.
Таблица 13
Воздух. Кислород. Горение

Фотосинтез представляет собой сложный химический процесс, включающий несколько стадий: поглощение и транспортировку солнечной энергии, использование энергии солнечного света для инициирования фотохимических окислительно-восстановительных реакций, восстановление углекислого газа и образованием углеводов.
Солнечный свет – это электромагнитное излучение разных длин волн. В молекуле хлорофилла при поглощении видимого света (красного и фиолетового) происходят переходы электронов из одного энергетического состояния в другое. На фотосинтез расходуется только небольшая часть солнечной энергии (0,03 %), достигающей поверхности Земли.
Весь имеющийся на Земле диоксид углерода проходит через цикл фотосинтеза в среднем за 300 лет, кислород – за 2000 лет, вода океанов – за 2 млн. лет. В настоящее время в атмосфере установилось постоянное содержание кислорода. Он практически полностью расходуется на дыхание, горение и гниение органических веществ.
Кислород – одно из самых активных веществ. Процессы с участием кислорода называются реакциями окисления. К ним относят горение, дыхание, гниение и многие другие. На таблице показано горение нефти, которое идёт с выделением теплоты и света.
Реакции горения могут принести не только пользу, но и вред. Горение можно остановить, прекратив доступ воздуха (окислителя) к горящему предмету с помощью пены, песка или одеяла.
Пенные огнетушители наполняют концентрированным раствором питьевой соды. При её контакте с концентрированной серной кислотой, находящейся в стеклянной ампуле в верхней части огнетушителя, образуется пена углекислого газа. Для приведения в действие огнетушитель переворачивают и ударяют об пол металлическим штифтом. При этом ампула с серной кислотой разбивается и образующийся в результате реакции кислоты с гидрокарбонатом натрия углекислый газ вспенивает жидкость и выбрасывает её из огнетушителя сильной струёй. Пенистая жидкость и углекислый газ, обволакивая горящий предмет, оттесняют воздух и гасят пламя.
