ПРОГРАММА РАСЧЕТА F – кривой
Па С/П 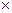 С/П С/П С/П С/П С/П С/П | Ипс Пв ИП2 F X 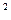 F1/X F1/X | 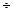 Ипd + П3 Ипd + П3 | ?-? 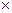 П2 ИП2 П2 ИП2 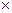 | ИП1 С/П ИП0 С/П | + + БП 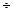 | Пd П1 ИП3 П0 | ИП0 Ипв ИП1 - П1 | + F X 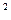 ИП0 ИП3 П2 ИП0 ИП3 П2 | П0 Ипd 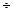 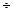 П3 П3 |
Перед обработкой каждого массива данных в регистр Пс внести значение С?
ПРОГРАММА РАСЧЕТА С – кривой
| П0 П3 ИП5 П0 | ИП1 ИП2 ИП3 - П1 | + F X 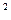 ИП1 ИП5 П2 ИП1 ИП5 П2 | П1 ИП0 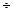 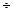 П3 П3 | С/П 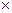 С/П С/П П4 С/П С/П П4 | П2 ИП4 F X 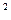 F1/X П5 F1/X П5 | ИП0 + П5 С/П | 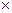 П4 ИП4 П4 ИП4 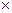 | ИП3 С/П ИП1 С/П | 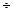 БП БП 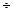 |
ПОЛУЧЕНИЕ СУЛЬФАТА АММОНИЯ
1.Короткие сведения о процессе.
Сульфат аммония получают на основе реакции нейтрализации серной кислоты аммиаком.
Сульфат аммония представляет собой белые, прозрачные, тонкие кристаллы с формой удлиненного ромба. Размер кристаллов зависит от условий их образования и может колебаться от сотенных долей мм до 4мм и больше. Удельный вес кристаллического сульфата аммония составляет 1.77 г/см3.
Сульфат аммония находит широкое применение в сельском хозяйстве в качестве удобрений. Полезным элементом для почвы в сульфате аммония является азот.
По содержанию азота сульфат аммония стоит на одном из первых мест среди вторых азотных удобрений. Так, сульфат аммония содержит 21.5% азота, селитра чилийская -15.5%.
Для характеристики сульфата аммония как удобрения большое значение имеет размер его кристаллов. Очень мелкие кристаллы легко разносятся ветром и в почве распределяются неравномерно. Мелкие кристаллы тяжело отделить от влаги, поэтому они легко слеживаются, что усложняет введение их в грунт. Производству сульфата аммония с большими кристаллами уделяют значительное внимание.
Сульфат аммония из аммиака коксового газа получают в аппарате называемом сатуратором.
В сатураторах коксовый газ барботируют через раствор серной кислоты. Аммиак при этом вступает в реакцию с кислотой, и образовывает как продукт нейтрализации, сульфат аммония. При излишке кислоты образовывается кислая соль - бисульфат аммония:
3NH3 + 2H2SO4 = NH4HSO4 + (NH4)2SO4
По мере насыщения раствора аммиака кислая соль переходит в среднюю, т.е. в сульфат аммония:
NH4HSO4 + NH3 = (NH4)2SO4
Реакция между аммиаком и серной кислотой сопровождается выделением тепла. Количество теплое, что выделяется, имеет большое значение для процесса производства. На каждый килограмм сульфата аммония, который образующегося выделяется около 20000 кДж. В сатураторе одновременно образовываются сульфат и бисульфат аммония. Бисульфат аммония лучше растворим в воде и слабом растворе серной кислоты, чем сульфат аммония и потому при достижении насыщения раствора в первую очередь выпадают кристаллы сульфата аммония.
Кристаллы сульфата аммония оседают на дно сатуратора, и оттуда непрерывно откачиваются вместе с маточным раствором центробежным насосом в кристаллоприемник. Из кристаллоприемника маточный раствор стекает в сатуратор, а кристаллы поступают на центрифугу. Оптимальная температура процесса 60-70 0С.
2.Цель работы:
Определение выхода сульфата аммония и составление материального баланса при нейтрализации раствора серной кислоты аммиаком.
Приборы и материалы:
1. Нейтрализатор на 250 см3. 
2. Поглотительная склянка (2 шт.).
3. Термометр на 100 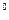 С.
С.
4. Мерная колба на 100 см3
5. Бюкс.
6. Пипетка на 10 см3.
7. Колба Эрленмейера на 250 см3.
8. Колба Бунзена, воронка Бюхнера.
9. Фильтровальная бумага.
Реактивы:
1. Насыщенный раствор (NН4)2S04.
2. 20 % раствор аммиачной воды.
3. 75 % раствор серной кислоты.
4. 0,5мол/дм3 раствор серной кислоты.
5. 0.5мол/дм3 раствор NaОН.
6. Метилоранж.
3. Описание экспериментальной установки
В качестве нейтрализатора (1) применяет коническая колба, закрытая сверху пробкой с тремя отверстиями, в которые вставлены термометр и 2 трубки для ввода и вывода смеси газа и воздуха.
Нейтрализацию раствора серной кислоты проводят смесью аммиака и воздуха, полученной в процессе просасывания воздуха водоструйным насосом (4) через 20%-ный раствор аммиака, залитого в поглотительную склянку (2). Газ, выходящий из нейтрализатора (1) проходит через вторую поглотительную склянку (3), где проходит улавливание непрореагировавшего аммиака.
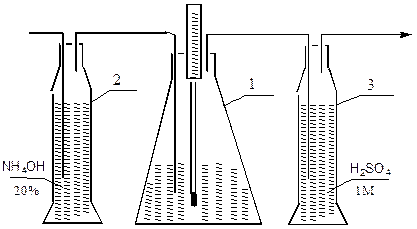
Рис.1 Схема лабораторной установки
Ход работы:
В поглотительную склянку 2 наливают 100-200 мл 20%-ного раствора аммиака. Готовят смесь насыщенного раствора сульфата аммония и 75%-ної серной кислоты с таким расчетом, чтобы содержание Н2SO4 в смеси составил приблизительно 25%, что отвечает пусковым условиям в заводском процессе.
Для приготовления смеси в фарфоровую склянку емкостью 0,5 л наливают 100 см3 насыщенного раствора сульфата аммония и прибавляют осторожно, при помешивании 35 мл 75%-ной серной кислоты. Из полученной смеси отбирают пробу (3-5 мл) для определения кислотности исходного раствора, смесь что оставшуюся загружают в нейтрализатор 1. В склянку 3 наливают 100-200 мл 0.1М Н2SO4 . К склянке 3 присоединяют водоструйный насос и ведут опыт к получению осадка сульфата аммония. Полученный осадок (NH4)2SO4 отфильтровывают на водоструйном насосе, промывают маточным раствором, оставляют сушиться.
4.Методика анализа
1. Определение содержания летучего аммиака в аммиачной воде:
Содержание летучего аммиака определяют до и после опыта, а потом рассчитывают количество аммиака, израсходованного на получение сульфата аммония.
Определения производят прямым титрованием. Отбирают бюреткой 10 см3 аммиачной воды и помещают в мерную колбу на 100 см3 , в которую заранее наливают до половины объема дистиллированную воду, потом доказывают уровень к метке и хорошо взбалтывают. Отобрав пипеткой 10 см3 раствора в колбу, где уже находится 25-30 см3 дистиллированной воды, прибавляют 1-2 капле метилоранжа и титруют раствором Н2SO4
Процентное содержимое аммиака в аммиачной воде рассчитывают по формуле:
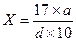
где: Х - содержимое аммиака в аммиачной воде, %:
а - количество кислоты, которая пошла на титрование, см3;
а 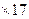 - содержание NH3 в граммах в 1 дм3 исследуемой воды;
- содержание NH3 в граммах в 1 дм3 исследуемой воды;
d - удельный вес исследуемой аммиачной воды при 20 °С.
2. Определение кислотности смеси.
Определение кислотности смеси проводят к началу опыта и после получения сульфата аммония.
Отбирают из нейтрализатора 5 мл смеси с помощью пипетки, часть смеси выливают в предварительно взвешенный бюкс. После чего бюкс взвешивают снова. В начале опыта берут для анализа навеску 2-3г, после опыта - 7-10г. Навеску смывают из бюкса небольшим количеством воды в коническую колбу. Пробу дополнительно разбавляют водой и титруют 0,5н. раствором NаОН в присутствии индикатора к переходу от розового крашения к оранжевому.
Содержание серной кислоты в смеси определяют по формуле:
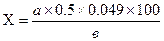
где: Х - содержание серной кислоты в смеси, % ;
а - количество щелочи, которая пошла на титрование:
0,049 - количество кислоты в г, что отвечает 1 см3 1 г раствора луга;
в - навеска, г.
5. Требования, которые предлагаемы к отчету
В отчете необходимо отобразить:
1. Условия, необходимые для получения сульфата аммония.
2. Схему установки и короткое описание проведенной работы.
3. Сводную таблицу полученных результатов и их обработку.
4. Расчет выхода сульфата аммония по аммиаку или по кислоте.
5. Выводы по проведенной работе.
6. Материальные балансы сатуратора.
Список литературы, которая рекомендуется
1. Мухленов И.П. Общая химическая технология. Г., "Высшая школа"1988 р
2. Мухленов И.П. Расчеты химико-технологических процессов .Л., ” Химия" , 1986г.
3. Общая химическая технология. - Под ред. А. Г.Амелина, М.,"Химия", 1977.
4. Практикум по общей химической технологии.. "Высшая школа". Г., 1979.
ГАЗО-ЖИДКОСТНАЯ ХРОМАТОГРАФИЯ
Для разделения, анализа и исследование веществ и их смесей, которые переходят без разложения в парообразное состояние, наибольшее применение получила газовая хроматография.
ХРОМАТОГРАФИЯ - это физико-химический метод разделения и анализа смесей газов, паров, жидкостей или растворенных веществ сорбционными методами в динамических условиях. Она основана на разном распределении компонентов смеси между двумя фазами - недвижимой и подвижной.
Вещества, которые составляют недвижимую фазу, называются сорбентами. Недвижимая фаза может быть жидкой или твердой.
К газо-жидкостной хроматографии (ГЖХ) относятся все варианты газовой хроматографии, у которой как недвижимую фазу используют слой жидкости, нанесенный на поверхность твердого носителя (зернистый, мелкодисперсный или внутренняя стенка колонки).
Газохроматографический процесс осуществляют в специальных приборах, которые называют газовыми хроматографами. Несмотря на разные технические решения, габариты и характеристики, принцип устройства хроматографов один. Каждый из них имеет хроматографическую колонку с системой: регулирования ее температуры; системой подачи потока газа-носителя; системой подготовки и введения анализируемой смеси; системой которая анализирует (детектор) и системой регистрации результатов деления и анализа.
Механизм деления смеси в данном случае основан на разной растворимости ее компонентов в поглощающей среде. В газовой фазе молекулы всех компонентов двигаются практически с одинаковыми скоростями. Однако молекулы разных компонентов в сорбированном состоянии находятся разное время, которое зависит от сил взаимодействия с поверхностью недвижимой фазы. В результате протекания сотен тысяч актов сорбции и десорбции происходит накопление разницы общих скоростей перемещения компонентов в колонке и молекулы разных компонентов выходят из колонки через различные промежутки времени.
СИСТЕМА ПОДГОТОВКИ ГАЗОВ
Система подготовки газов предназначена для установки, стабилизации и измерения скорости потока газа-носителя и дополнительных газов (если они необходимы для питания детектора), а также для очистки газов. Особенно важное значение имеет установка и стабилизация оптимальной, для данного анализа, величины расхода газа-носителя. Недостаточная стабильность газовых потоков часто является причиной неустойчивой нулевой линии, которая затрудняет количественную обработку хроматограмм. Установка и необходимая стабилизация газовых потоков осуществляется совокупностью нескольких элементов, основными из которых являются дроссель, регулятор давления и регулятор расхода.
Измерение величины газовых потоков производят с помощью мыльно-пленочного измерителя, реометров и ротаметров. Наибольшую точность измерения обеспечивает мыльно-пленочный измеритель. Расход измеряют за временем прохождения мыльной пленкой известного объема калиброванной стеклянной трубки.
ДОЗИРУЮЩИЕ УСТРОЙСТВА
Дозирующие устройства (дозаторы) предназначены для введения в колонку определенного количества анализируемой смеси.
Введение жидких смесей в колонку делают с помощью специальных шприцев через термостойкое резиновое уплотнение. Действие шприцев основано на вытеснении поршнем определенного объема жидкости из калиброванного цилиндра шприца. Дозируемый объем жидкости заключен в стеклянный калиброванный цилиндр на котором нанесена шкала в микролитрах. В качестве поршня используется проволока из нержавеющий стали. Недостатком такого шприца является относительно большой объем иглы (до 2 мкл). Часть жидкости, которая находится в игле, не выдавливается со шприца при полном введении поршня в цилиндр, но частично испаряется при введении иглы в испаритель. Количество жидкости, которая выходит из иглы, зависит от глубины введения и времени пребывания иглы в испарителе и не подвергается непосредственному контролю, что является источником невоспроизводимости величины пробы. Этого недостатка не имеют шприцы, в которых дозирующий о6ъем заключен в самой игле - это микрошприцы с плунжером в виде провода который передвигается в игле. Герметичность обеспечивается фторопластовым сальником, помещенным в основании иглы. Общим недостатком шприцев является малая механическая прочность, которая вызывает необходимость очень осторожного обращения с ними.
ИСПАРИТЕЛЬ
Испаритель представляет собой металлический блок, который нагревается до определенной температуре, с каналом для введения и испарения жидкой пробы. В канал подается поток газа-носителя. С одной стороны канал закрыт пробкой из термостойкой резины. Из другой стороны канала присоединена хроматографическая колонка. Игла шприца с анализируемой жидкостью вводится через термостойкое уплотнение в канал испарителя. Введенная проба быстро испаряется и переносится потоком газа-носителя в колонку.
ХРОМАТОГРАФІЧНА КОЛОНКА
Различают три разновидности хроматографических колонок: насадочные (набивные). микронасадочные и капиллярные. Наибольшее распространение получили насадочные колонки, которые представляют собой трубки , изготовленные из металла (нержавеющий сталь, медь), стекла, или фторопласта с внутренним диаметром от 2 до 10 мм длиной от 0.5 до 3 м. Внутренняя полость трубок заполняется инертным твердым носителем, покрытым тонкой пленкой нелетучего сорбента.
Трубкам придается U-образная, спиральная или зигзагообразная форма.
ДЕТЕКТОРЫ
Хроматографический детектор представляет собой устройство, предназначенное для выявления и количественного определения компонентов анализируемой смеси, которые выходят из колонки в потоке газа-носителя. Регистрация вещества осуществляется за счет преобразования физических или физико-химических свойств бинарных смесей (компонент - газ-носитель в сравнении с чистым газом-носителем) в электрический сигнал.
В настоящее время для газовой хроматографии предложено около 50-ти детекторов. Наибольшее распространение получили два: детектор теплопро водности (катарометр) и детектор ионизации пламени.
1.Детектор по теплопроводности (катарометр).
Работа детектора теплопроводности основана на изменении температуры нагретых нитей (чувствительных элементов) в зависимости от теплопроводности окружающего газа. Для получения дифференциального сигнала через одну камеру катарометра (измерительную) проходит газ, который выходит из хроматографической колонки, через другую (сравнительную) - чистый газ-носитель.

Рис. 1: Схема включения четырехплечевого катарометра в сеть.
Нагретые чувствительные элементы в сравнительной и измерительной камерах обдуваются потоком газа-носителя, и их сопротивление приобретает определенное значение. При прохождении через детектор бинарной смеси, которая состоит из газа-носителя и обусловленного компонента, который отличается от чистого газа-носителя теплопроводностью, в измерительной ячейке изменяется теплообмен и изменяется температура чувствительного элемента и, как следствие, его сопротивление.
Расхождение сопротивлений чувствительности элементов является функцией мгновенной концентрации компонента в газовом потоке и измеряется с помощью моста Уитстона.
2. Ионизационно-пламенный детектор
Ионизационно-пламенный детектор (ДІП) представляет собой камеру, в которой поддерживается водородное пламя, которое является источником ионизации. В камеру вводятся необходимые для поддержки пламени водород и воздух. Водород подается в детектор в смеси с газом-носителем через канал горелки, а воздух - через другой канал и распространяется равномерно диффузором.
Горелка, которая является одним из электродов, изолирована от корпуса детектора и соединена с источником стабилизированного напряжения. Второй электрод, который называется коллектором, расположен над горелкой. Во внешнюю цепь электрода детектора включен электрометр, который измеряет ток между электродами детектора.
Поскольку в пламени чистого водорода число ионов очень мало, сопротивление межэлектродного газового пространства слишком большое и ток детектора очень мал. При внесении с газом-носителем анализируемых органических веществ число ионов в пламени резко увеличивается, сопротивление пламени падает и во внешней цепи детектора регистрируется соответствующий рост ионного тока.
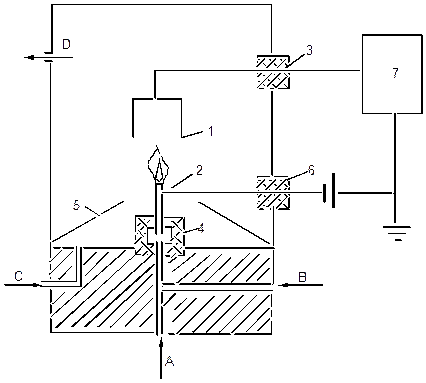
Рис. 2. Схема ионизационно-пламенного детектора:
электрод-коллектор; 2-горелка; 3-изолятор электрода-коллектора; 4-изолятор горелки; 5-диффузор; 6-изолятор питания; 7-электрометр.
А-газ-носитель; В-водород; С-воздух; D-газы и продукты горения.
СИСТЕМА ТЕРМОСТАТИРОВАНИЯ
Система термостатирования необходима для поддержания оптимального температурного режима хроматографических колонок, детекторов, и дозирующих устройств. Система термостатирования предназначена для обеспечения изотермического режима работы колонок. В неё входит термостат, в который помещены колонки и детектор, которые требуют термостатирования и автоматического регулятора, по шкале которого устанавливается температура анализа.
Термостат представляет собой камеру с двойными стенками, пространство между ними заполненный термоизоляционным материалом. Вращение вентилятора создает интенсивный направленный поток воздуха, проходящий через колонки и электрическими нагревателями.
