В 1898 году М. Кюри обнаружила, что торий обладает радиоактивностью. Именно радиоактивность- основная причина нынешнего интереса к элементу с порядковым номером 90
В периодической системе 232Th расположен в четвертой группе. Торий - металл серебристого цвета, легко подвергается механической обработке. Он очень легко окисляется, поэтому его хранят под слоем керосина. Торий способен проявлять степени окисления +4, +3, +2, наиболее устойчивой является +4. Только одно соединение тория - его двуокись ThО2 имеет самостоятельное применение, остальные же важны лишь для науки и… для производства тория.
Основными источниками тория являются торийсодержащие минералы (монацит, ортит). Методы выделения тория предусматривают отделение его от сопутствующих редкоземельных элементов. В технологии для этой цели используется, в основном, экстракция тория ТБФ( трибутилфосфатом) после его отделения от основной массы редкоземельных элементов дробным осаждением менее растворимого сульфата тория.
Основными источниками тория являются торийсодержащие минералы (монацит, ортит). Методы выделения тория предусматривают отделение его от сопутствующих редкоземельных элементов. В технологии для этой цели используется, в основном, экстракция тория ТБФ после его отделения от основной массы редкоземельных элементов дробным осаждением менее растворимого сульфата тория. Методы соосаждения со специфическим (La, Ce) и неспецифическим Te(OH)3, BiPO4 носителями используются для получения препаратов 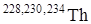 , применяемых в качестве радиоактивных индикаторов.
, применяемых в качестве радиоактивных индикаторов.
Применение тория. Элементом особой важности, стратегическим металлом торий стал лишь после второй мировой войны.
Как и всякий четно-четный изотоп (четное число протонов и нейтронов), торий-232 не способен делиться тепловыми нейтронами. Но под действием тех же нейтронов с торием происходит вот что:
Th232 + n -> Th233 -> Pa233 -> U233
А U233 - отличное ядерное горючее, поддерживающее цепное деление и имеющее некоторое преимущество: при делении его ядер выделяется больше нейтронов. Каждый нейтрон, поглощенный ядром плутония-239 или урана-235, дает 2.03-2.08 новых нейтронов, а уран-233 - намного больше - 2.37.
Применение тория в качестве ядерного горючего затруднено прежде всего тем, что в побочных реакциях образуются изотопы с высокой активностью. Главный из таких загрязнителей - уран-232 - альфа- и гамма-излучатель с периодом полураспада 73.6 года. Его использованию препятствует и то обстоятельство, что торий дороже урана. Уран легче выделить. Некоторые урановые минералы (уранит, урановая смолка) - это простые окислы урана. У тория таких. простых минералов (имеющих промышленное значение) нет. А попутное выделение из редкоземельных минералов осложнено сходством тория с элементами семейства лантана.
Главная проблема получения делящегося материала из тория состоит в том, что он изначально не присутствует в реальном реакторном топливе, в отличие от U-238. Для использования ториевого воспроизводства высокообогащенный делящийся материал (U-235, U-233, Pu-239) должен использоваться в качестве топлива реактора с включениями тория по большей части только для возможности воспроизводства (т.е. не происходит или происходит незначительное выделение энергии, хотя сгорание U-233, полученного на месте, может внести вклад в выделение энергии). С другой стороны, тепловые бридерные реакторы (на медленных нейтронов) способны использовать U-233/торий цикл воспроизводства, особенно если в качестве замедлителя использовать тяжелую воду.
Торий является перспективным материалом для ядерной энергетики. Делящимся элементом при этом служит 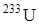 , образующийся по схеме:
, образующийся по схеме:
Торий является перспективным материалом для ядерной энергетики. Делящимся элементом при этом служит 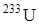 , образующийся по схеме:
, образующийся по схеме:

Достоинство тория как топливного материала определяется высокой температурой его плавления, отсутствием фазовых переходов, высокой механической прочностью и радиационной устойчивостью металлического тория и ряда его соединений. Использование тория в ядерной энергетике способно решить проблему истощения природных запасов урана. Из других областей применения тория представляет интерес его использование как катализатора, а также в качестве легирующих присадок к магнитным сплавам, используемым в авиационной и ракетной технике.
Торий вначале использовался в производстве светящихся красок. Особенно широко его применяли для нанесения на стрелки и циферблат часов. Однако , вскоре была обнаружена повышенная смертность среди работников, имеющих дело с этими красками. Как оказалось продукт распада тория радий-228 накапливается в костях, что и вызывало смертность работающих с красками. Сам торий очень опасен при попадании в кровь, так как вызывает осаждение протеина.
11.10 ПРОТАКТИНИЙ 91Pa
Как и для многих других элементов, для протактиния Д. И. Менделеев оставил клетку, назвав будущий элемент экатанталом. Экатантал оказался протактинием.
История открытия протактиния - одна из страниц истории поисков радиоактивных элементов и изотопов в природе. Протактиний почти одновременно обнаружили О. Ган и Л. Мейтнер в Германии и Ф. Содди и Дж. Кренстон в Англии. Новый радиоактивный элемент был обнаружен при переработке минералов урана точно так же, как полоний, радий, актиний. Это был самый долгоживущий изотоп элемента №91- протактиний-231 с периодом полураспада 35000 лет. Протактиний порожден распадом урана-235 по схеме:
 U
U 


 Ac
Ac 
В природе он находится в таких же количествах, как и радий ( 340 мг на 1 т урана).Поэтому протактиний принадлежит к числу наименее распространенных элементов на Земле. Кроме протактиния-231 в природе существует протактиний-234. Он также продукт распада урана, но период его полураспада очень мал.
Кроме этих двух изотопов протактиния, сейчас известны еще 17 изотопов с массовыми числами от 216 до 238 и периодами полураспада от долей секунды до нескольких дней. Все они получаются искусственным путем в цепочках радиоактивных распадов, идущих при облучении урана-238 и тория-232 протонами, дейтронами и альфа-частицами.
Протактиний –самый неактиноидный актиноид. По своим свойствам он сходен с Nb, Ta, Zr, Hf, Ti. Это блестящий металл светло-серого цвета, покрытый на воздухе тонкой пленкой оксида. По твердости протактиний близок к урану. Интересным свойством протактиния является его сверхпроводимость при 2˚ К.
Металлический протактиний может быть получен термическим разложением его галогенидов на вольфрамовой нити при высокой температуре и давлении 10-3 – 10-4 Па. Изучение химии протактиния осуществлялось методами классической химии с использованием долгоживущего изотопа 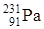 . Протактиний легко реагирует с водородом. Степени окисления протактиния +5, +4,+3,+2, из которых наиболее устойчивой является +5. Протактиний в степени окисления +5 в большей мере является аналогом тантала и ниобия, чем соседних актиноидов (урана, нептуния, плутония). Для протактиния (+5) в водных растворах характерна очень большая склонность к гидролизу и полимеризации с образованием коллоидных форм. В ионной и молекулярной формах
. Протактиний легко реагирует с водородом. Степени окисления протактиния +5, +4,+3,+2, из которых наиболее устойчивой является +5. Протактиний в степени окисления +5 в большей мере является аналогом тантала и ниобия, чем соседних актиноидов (урана, нептуния, плутония). Для протактиния (+5) в водных растворах характерна очень большая склонность к гидролизу и полимеризации с образованием коллоидных форм. В ионной и молекулярной формах  (+5) существует только в концентрированных растворах сильных минеральных кислот или в растворах, содержащих комплексующие агенты.
(+5) существует только в концентрированных растворах сильных минеральных кислот или в растворах, содержащих комплексующие агенты.
Основными методами выделения протактиния являются соосаждение, экстракция и хроматография. Наилучшими носителями являются фосфат циркония и гидроксид марганца (1У).
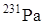 применяется как источник получения
применяется как источник получения 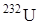 и
и 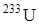 по реакции (n,г)
по реакции (n,г)

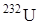 - используется как автономный изотопный источник тока,
- используется как автономный изотопный источник тока, 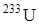 используется в качестве ядерного топлива .
используется в качестве ядерного топлива .
УРАН
Уран- 92 –ой элемент Периодической системы Менделеева, последний и самый тяжелый из существующих в природе элементов. Этот элемент занимает в современной жизни особое место.
Главный элемент ядерной энергетики и сырье для получения другого главного энергетического элемента- плутония, он причастен ко многим открытиям ХХ века . Уран помог раскрыть тайны атома, стал источником невиданной мощи. Он основа современной « алхимии», превращения элементов и получения новых.
Открыл уран немецкий химик Клапрот в 1789 г., выделив из саксонской смоляной руды черное металлоподобное веществ, и назвал его ураном Более пятидесяти лет это вещество считалось металлом и только в 1841 году францезский химик Пелиго доказал, что это окисел урана UO2. Прошло еще 55 лет и в 1896 году Беккерель обнаружил, благодаря урану, явление радиоактивности. В 1903 году Д. И. Менделеев
Химические свойства урана изучены методами классической химии.
Степени окисления урана +3, +4, +5, +7.
Для урана в металлическом состоянии характерно взаимодействие с водородом, азотом и другими элементами. В свободном состоянии уран, серебристый металл большой плотности, в порошкообразном состоянии он пирофорный.
Соединения урана обладают большой склонностью к комплексообразованию, гидролизу.
Выделение урана из природных объектов производится путем кислотного или карбонатного выщелачивания его после предварительного обогащения руды. Окончательное извлечение урана осуществляется методами осаждения, экстракции, сорбции и т.д.
ТРАНСУРАНОВЫЕ ЭЛЕМЕНТЫ
Основным методом получения Np, Pu, Am является облучение урана, нептуния, плутония медленными нейтронами:


Наиболее сложной проблемой является их отделение от облучаемого элемента и друг от друга. Решение этой задачи основано на том, что для каждого элемента рассматриваемой группы характерна своя устойчивая степень окисления: для урана +6, для нептуния +5, для плутония +4, для америция +3. Наиболее эффективными являются ионообменные и экстракционные методы. Меньшее значение для целей разделения и выделения этих элементов имеют осадительные методы.
Химия водных растворов этих элементов исследована с использованием микрохимии из-за их высокой массовой активности
Практическое использование элементов рассматриваемой группы определяется их ядерно-физическими характеристиками, а не химическими свойствами. Многие изотопы рассматриваемых элементов способны к делению под действием нейтронов и используются в качестве ядерного топлива. К наиболее важным из них относятся  , делящиеся под действием медленных нейтронов.
, делящиеся под действием медленных нейтронов.  служит источником получения ядерного топлива -
служит источником получения ядерного топлива -  .
.
Кроме того важной областью применения рассматриваемых элементов является изготовление на основе  изотопных источников. Эти источники могут быть использованы для получения электрической энергии, теплоты и механической энергии. Изотопные источники на основе
изотопных источников. Эти источники могут быть использованы для получения электрической энергии, теплоты и механической энергии. Изотопные источники на основе  использовались в космических летательных аппаратах для термостатирования замкнутых объектов с электронной аппаратурой, для жизнеобеспечения космических орбитальных станций и снабжения их электроэнергией.
использовались в космических летательных аппаратах для термостатирования замкнутых объектов с электронной аппаратурой, для жизнеобеспечения космических орбитальных станций и снабжения их электроэнергией.
 используется для создания стимуляторов сердечной деятельности.
используется для создания стимуляторов сердечной деятельности.
 имеет очень большое сечение деления и следовательно, малую критическую массу, что позволяет использовать его в качестве ядерного топлива в небольших реакторах, пригодных для космических исследований. Изотопы
имеет очень большое сечение деления и следовательно, малую критическую массу, что позволяет использовать его в качестве ядерного топлива в небольших реакторах, пригодных для космических исследований. Изотопы  и
и  , испускающие г – кванты с малой энергией используют в качестве источников возбуждения в рентгенофлюоресцентном анализе. В свободном состоянии нептуний, плутоний, америций – серебристые металлы большой плотности, в порошкообразном состоянии они пирофорны.
, испускающие г – кванты с малой энергией используют в качестве источников возбуждения в рентгенофлюоресцентном анализе. В свободном состоянии нептуний, плутоний, америций – серебристые металлы большой плотности, в порошкообразном состоянии они пирофорны.
Наиболее распространенными методами получения этих элементов в металлическом состоянии является восстановление их фторидов щелочами или щелочноземельными металлами или электролиз расплавов их солей.
Все эти металлы сплавляются друг с другом в широком интервале концентраций и проявляют способность образовывать интерметаллические соединения.
11.13 ТРАНСАМЕРИЦИЕВЫЕ АКТИНОИДЫ (96Cm, 97Bк, 98Cf, 99Es, 100Fm, 101Md, 102No, 103Lr)
Особенностью изучения химии этих элементов является необходимость использования методов радиохимии. Это обусловлено невозможностью получения большинства указанных элементов в весомых количествах, а также их чрезвычайно высокой массовой активностью.
Все элементы от кюрия до фермия получены в виде металлов.
Для всех рассматриваемых элементов, за исключением 102, основной степенью окисления является +3. Известны также для этих элементов степени окисления +4 и +2. У этих элементов высокая склонность к комплексообразованию. Эти элементы способны образовывать металлоорганические соединения Ме (С5Н5)3.
Получают их бомбардировкой актиноидов тяжелыми ионами.
Для отделения актиноидов друг от друга и от лантаноидов используются процессы экстракции и ионного обмена. Кроме экстракции для целей выделения и разделения рассматриваемых элементов применимы почти все известные варианты хроматографических методов.
Практическое применение тяжелых актинидов так же как и легких, обусловлено их физико-химическими свойствами.
Так изотопы кюрия  используются для приготовления изотопных источников тока.
используются для приготовления изотопных источников тока.  - являются удобным материалом для изготовления источников нейтронов с большой интенсивностью потока.
- являются удобным материалом для изготовления источников нейтронов с большой интенсивностью потока.
Изотопы  - находят применение для изготовления б – источников.
- находят применение для изготовления б – источников.
 могут найти применение в качестве ядерного топлива.
могут найти применение в качестве ядерного топлива.
ТРАНСАКТИНОИДЫ
Трансактиноидные элементы характеризуются заполнением 6d и 7s – уровней атома. К ним относятся элементы, начиная со 104 и кончивая 118. В соответствии с актиноидной гипотезой последним из 5 f элементов должен быть элемент №103 лоуренсий (5f14 6d1 7s2 ).
Основным методом получения важнейших изотопов 104-106-го элементов является облучение актиноидов Pu, Am 96Cm, 97Bк, 98Cf ускоренными тяжелыми ионами углерода, кислорода и неона. Принципиально важным, с этой точки зрения, должно было оказаться открытие элемента №104 и изучение его свойств. Это позволило бы подтвердить или опровергнуть актиноидную гипотезу. Элемент № 104 был синтезирован в 1964 году в Дубне группой Флерова, облучением 242Pu ядрами 22Ne
 Pu+
Pu+  Ne®
Ne®  Db+ 4 10n
Db+ 4 10n
Первоначально элемент был назван курчатовием, а в последствие дубнием. В настоящее время получены изотопы дубния с массовыми числами 257-261. Их периоды полураспада от 11 мин у курчатовия 258 до 70 с у курчатовия 261. Элемент был идентифицирован чешским ученым Зварой с помощью специальных экспрессных методов анализа. Было показано, что дубний резко отличается по своим свойствам от предыдущих элементов. Как было обнаружено в химическом отношении дубний ведет себя подобно гафнию и элементам 1У В группы; его электронная конфигурация 5f14 6d2 7s2.С открытием дубния стало ясно, что он, не являясь актиноидом ведет себя подобно лантаноидам.
Дубний и более тяжелые элементы можно назвать трансактиноидами.
Чуть позже были синтезированы элементы с атомными номерами 105-107.
Эти элементы являются аналогами тантала (дубний, вольфрама (сиборгий) и рения( борий).
 Br(
Br(  О, 5n)
О, 5n)  Db
Db 
 .
.

Сечения активации этх реакций очень малы и резко уменьшаются с возрастанием атомного номера образующегося составного ядра. Более благоприятным с этой точки зрения является использование в качестве материала мишени ядер свинца и висмута, а качестве бомбардирующих частиц- ионов хрома и более тяжелых элементов. Использование такой комбинации позволило получить элементы с порядковыми номерами 106 и 107:  Период полураспада 7.10-3 с.
Период полураспада 7.10-3 с.
Отправным моментом при получении еще более тяжелых элементов является гипотеза о существовании островов стабильности, предложенная еще в 1925 году немецким ученым Р. Свинне. Сущность этой гипотезы заключается в том, что элементы, ядра которых содержат магическое число нейтронов и протонов, соответствующее заполненным нейтронным или протонным оболочкам, должны обладать повышенной устойчивостью к альфа распаду и спонтанному делению. Эта гипотеза инициировала многочисленные теоретические и экспериментальные исследования.
В основе методов химической идентификации при синтезе и поиске в природе сверхтяжелых элементов должно лежать прогнозирование химических свойств на основании ожидаемого их положения в периодической системе Менделеева.Например предполагается, что элементы с порядковыми номерами 112-118 должны быть относительно более летучими, чем элементы с пор. Номерами 80-86 от ртути до радона. Поэтомку для отделения элементов 112-118 от актиноидов и поиска их среди продуктов ядерных реакций целесообразно использовать метод возгонки.
Экспериментальные исследования включают попытки искуственного получения короткоживущих изотопов сверхтяжелых элементов особенно в области 110-114
При этом в качестве мишени используются 94Pu, 95Am, 96Cm, 97Bк, 98Cf, а в качестве бомбардирующих частиц кальций-20, хром-26 и цинк-30.
Успехи в синтезе трансурановых элементов и синтез трансактиноидов поставили вопрос впрямую о верхней границе периодической системы.
Синтез нептуния и плутония позволил выделить в проблеме конца системы два аспекта: о естественной границе и о возможном пределе синтеза искусственных элементов. Можно предполагать, что на Земле последним природным элементом является плутоний.
Если рассматривать периодический закон в космическом масштабе то проблема конца системы становится неоднозначной и непосредственно смыкается со вторым аспектом- пределом устойчивости атомных ядер.
Достижения современной ядерной физики и химии позволяют более определенно судить и о возможности синтеза новых искусственных сверхтяжелых элементов. Эта проблема также неоднозначна.
