Физико-химичеовие свойства аминокислот
В зависимости от рН кодного раствора а-карбоксильные и «-аминогруппы аминокислот существуют в одной из следующих взаимопревращаемых форм:
химическим свойствам аминокислоты, имеющие в своем составе аминные и карбоксильные группы, являются амфотерными электролитами.
Помимо а-амино- и а-карбоксильной групп, в общем заряде молекулы в составе кислых и основных аминокислот (табл. 4) есть еще и третья ионогенная группа в боковой цепи. Такие аминокислоты несут дополнительный отрицательный или положительный заряд. Биполярность молекул аминокислот обусловливает такие их свойства, как хорошая растворимость в воде, высокие значения диэлектрических постоянных и температуры плавления.
В курсе органической химии рассматриваются химические реакции, характерные для аминокислот: солеобразова-ние (по NН2- и СООН-группам), окисление и восстановление (по НS-и S—S-группам), алкилирование, ацилирование и этерификация (по NН2-, ОН- и СООН-группам), амиди-рование (по СООН-группам), нитрование и галоидирование (по ароматическому ядру), фосфорилирование и сульфити-рование (по ОН-группам) и т. д.
Некоторые из указанных реакций протекают в живых организмах.
Функциональные группы аминокислот разнообразны, что позволяет обнаруживать большинство их с помощью цветных реакций. Многие из них, очень чувствительные и специфичные, выявляют даже малые количества аминокислот в составе сложных смесей, биологическом сырье растительного и животного происхождения, белках.
Реакция с нингадрином лежит в основе количественного определения аминокислот и белков.
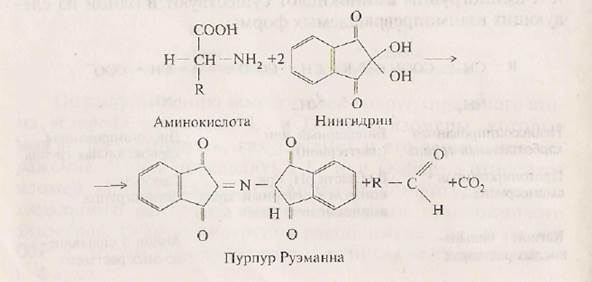
При взаимодействии нингидрина с ос-аминогруппой образуется продукт сине-фиолетового цвета с максимумом поглощения при 580 нм; интенсивность окраски при этом пропорциональна количеству аминокислоты. Аминокислота пролин дает с нингидрином желтое окрашивание (максимум поглощения при 440 нм). Эту реакцию используют в различных видах хроматографии для идентификации и количественного определения аминокислот.
Аминогруппы аминокислот (пептидов, белков) могут вступать в реакцию с карбонильными группами альдегидов и восстанавливающих Сахаров. Это реакции меланоидинообра-зования. Их схематично можно представить в виде двух стадий: 1) окислительно-восстановительное взаимодействие карбонильных групп и аминогруппы с образованием бесцветных промежуточных продуктов; 2) альдегидно-аминная полимеризация промежуточных продуктов и альдегидная конденсация с образованием темноокрашенных сложных соединений, называемых меланоидинами.
В результате реакций меланоидинообразования расщепляются как аминокислота, так и сахар: из аминокислоты образуются соответствующий альдегид, аммиак и оксид углерода (IV), а из сахара — фурфурол (из пентоз) или оксиметилфурфурол (из гексоз). Например, реакция лейцина с ксилозой протекает следующим образом:
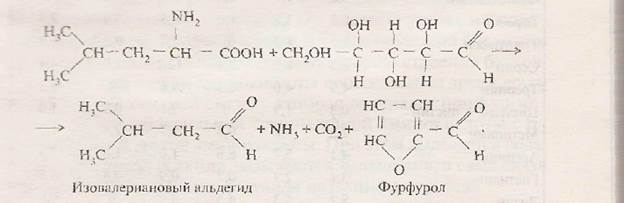 |
Получаемые из аминокислот альдегиды обладают приятным запахом. Сочетание запахов разных альдегидов определяет аромат многих пищевых продуктов. Фурфурол (оксиметилфурфурол) легко вступает в дальнейшие реакции, образуя меланоидины. Появление последних обусловливает потемнение ряда продуктов при их изготовлении и хранении. Особенно интенсивно протекают реакции меланоидинообразования при повышении температуры: во время сушки овощей, плодов, выпечки хлеба, жарении орехов, кофе, консервировании молока, изготовлении кондитерских изделий, солода, сахарных растворов, при тепловой обработке вина и т. п.
