Диаграмма растворимости вода – анилин
На рисунке 6 представлена диаграмма растворимости системы вода – анилин, которая относится к случаю ограниченной растворимости одной жидкости в другой. Взаимная растворимость жидкостей в этой системе увеличивается с ростом температуры.
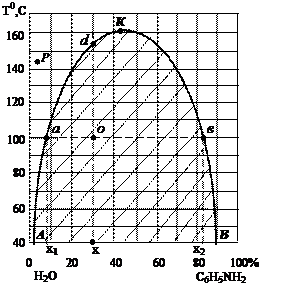 |
Рис. 6. Диаграмма системы H2O – C6H5NH2 (вода – анилин)
Кривая АКВ называется бинодальной кривой растворимости или кривой расслоения, ветвь АК отражает растворимость анилина в воде, ветвь ВК указывает на растворимость воды в анилине в зависимости от температуры.
Бинодальная кривая АКВ делит диаграмму на две области: гомогенную, лежащую над кривой и гетерогенную, находящуюся под кривой расслоения.
Фигуративные точки гомогенной области, например точка Р, изображают состояния однофазной условно дивариантной системы (S = 2 – 1 + 1 = 2).
Фигуративные точки, лежащие внутри гетерогенной области, например точка О, изображают состояние двухфазной условно моновариантной системы (S = 2 – 2 + 1 = 1).
Каждая точка, лежащая на бинодальной кривой, отражает сопряженную фазу. Точки ветви АК отвечают насыщению воды анилином, а точки ветви ВК отвечают насыщению анилина водой.
По диаграмме растворимости можно определить состав исходной смеси и состав двух сопряженных растворов, которые образуются при расслоении системы.
Например, рассмотрим исходную смесь двух жидкостей, которая содержит 70% воды и 3% – анилина (состав х).
Эта смесь будет расслаиваться при обычных условиях и даже при нагревании системы до 1550С. И только выше этой температуры (выше точки d) смесь будет гомогенной, однофазной, т.е. при этих условиях жидкости неограниченно растворимы друг в друге.
При температуре, например 1000С рассматриваемая смесь представляет собой два сопряженных раствора.
Состав образующихся двух растворов можно определить следующим образом: через точку О надо провести изотерму до пересечения с бинодальной кривой, которая является границей фазового поля (точки а и в).
Опуская перпендикуляры из этих точек на ось состава, определяют состав обоих образующихся растворов.
Состав одного из сопряженных растворов определяется точкой х1 (93% Н2О, 7% C6H5NH2), состав другого – точкой х2 (84% C6H5NH2, 16% Н2О).
По правилу рычага можно определить и относительные массы сопряженных растворов: mр-ра состава х1.ℓао = mр-ра состава х2.ℓов,
где ℓ – длина плеча.
Точка К разделяет бинодальную кривую на две ветви и называется верхней критической точкой растворения, а соответствующая ей температура – верхней критической температурой растворения. Выше этой температуры смесь любого состава имеет неограниченную растворимость и представляет собой однофазную гомогенную жидкую систему (S = 2 – 1 + 1 = 2).
|
проводят несколько изотерм (коннод) и соединяют их середины, тогда эта прямая будет проходить через точку К, которая и указывает на ВКТР.
