Особенности и преимущества ФХМА
Как уже отмечалось, ФХМА предназначены для определения малых содержаний различных веществ и элементов (≤10–5%), но почти все ФХМА, (за исключением кулонометрии) являются относительными и поэтому требуют предварительного эталонирования, т.е. установления функциональной зависимости между используемым аналитическим сигналом (Y) и концентрацией аналита (c) по стандартным образцам или растворам, которые анализируются химическими методами – и в этом проявляется неразрывная связь ФХМА с химическими методами анализа.
К преимуществам ФХМА можно отнести следующие:
1. Высокая чувствительность, позволяющая определять до 10–12 г аналита.
2. Высокая экспрессность (скорость выполнения анализа).
3. Возможность проведения анализа неразрушающими методами и без разложения проб.
4. Возможность включения в цепь автоматического контроля и регулирования технологических процессов.
СПЕКТРОСКОПИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
Общие положения
Спектроскопические методы анализа основаны на взаимодействии электромагнитного излучения с веществом. Происходящие при этом взаимодействии изменения энергетических состояний атомов, молекул или ионов вещества и являются источником аналитической информации о его качественном и количественном составе.
В связи с двойственной природой электромагнитного излучения – волновой и карпускулярной для характеристики применяют также различные, хотя и взаимосвязанные, параметры. Основной волновой характеристикой электромагнитного излучения является длина волны l (нм, Å) или волновое число  (см–1), а также частота излучения
(см–1), а также частота излучения  (с–1, Гц), где с – скорость света в данной среде (в вакууме с=3×1010 см×с–1).
(с–1, Гц), где с – скорость света в данной среде (в вакууме с=3×1010 см×с–1).
Согласно корпускулярной природе электромагнитное излучение является потоком дискретных частиц энергии – фотонов. Взаимосвязь между волновыми и корпускулярными характеристиками излучения описывается уравнением Планка:
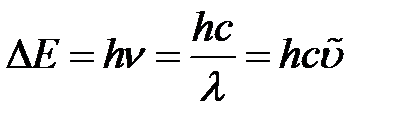 ,
,
где ∆E – изменение энергии частицы, поглотившей или испустившей квант света 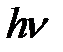 , энергия которого измеряется в джоулях (Дж) или электроновольтах (эВ), h – постоянная Планка (6.63×10–34 Дж×с или 4.14×10–15 эВ×с).
, энергия которого измеряется в джоулях (Дж) или электроновольтах (эВ), h – постоянная Планка (6.63×10–34 Дж×с или 4.14×10–15 эВ×с).
Энергия кванта излучения тем больше, чем меньше его длина волны. Так в ультрафиолетовой и видимой области (200-760 нм) энергия квантов света составляет, соответственно 6.0–1.5 эВ. В инфракрасной области (≥ 1 мкм) энергия кванта менее 1 эВ. В полном соответствии с энергией квантов различного диапазона длин волн поглощаемое излучение обладает различными возможностями изменения энергетического состояния при его поглощении. Поэтому, если в ультрафиолетовой и видимой областях спектра энергии кванта излучения достаточно на изменение всех видов переходов энергетического состояния (электронного, колебательного и вращательного) частиц взаимодействующего вещества, то в инфракрасной области энергии кванта хватает на изменение только колебательной и вращательной составляющих энергии молекулы.
Таким образом, испускание или поглощение квантов электромагнитного излучения анализируемым веществом позволяет получить характеристические сигналы в виде спектров[*] испускания или поглощения. При этом частота или длина волны излучения или поглощения определяется составом вещества. Интенсивность испускаемого или поглощаемого излучения (аналитического сигнала) пропорциональна количеству частиц, т.е. количеству (концентрации) определяемого вещества в пробе.
