Виды химических связей в органических соединениях

7. Механизмы реакций. Гомо- и гетеро литический разрыв связи. Механизм электрофильного присоединения. Радикальное присоединение.
Основные механизмы протекания реакций
Мы выделили три основных типа реагирующих частиц — свободные радикалы, электрофилы, нуклеофилы и три соответствующих им типа механизмов реакций:
• свободнорадикальные;
• электрофильные;
• нуклеофилъные.
Кроме классификации реакций по типу реагирующих частиц, в органической химии различают четыре вида реакций по принципу изменения состава молекул: присоединения, замещения, отщепления, или элиминирования (от англ. to eliminate — удалять, отщеплять), и перегруппировки. Так как присоединение и замещение могут происходить под действием всех трех типов реакционноспо-собных частиц, можно выделить несколько основных механизмов протекания реакций.

Кроме этого, мы рассмотрим реакции отщепления, или элиминирования, которые идут под воздействием нуклеофильных частиц — оснований.
7. Элиминирование

Гомолитический разрыв связи — разрыв, когда каждому атому отходит по одному электрону. Характерен для обменного механизма образования ковалентной связи.
Гетеролитический разрыв связи — разрыв, когда в результате образуются положительно и отрицательно заряженные частицы, т.к. оба электрона из общей электронной пары остаются при одном из атомов. Характерен для донорно-акцепторного механизма образования ковалентной связи.

Реакции электрофильного присоединения (англ. addition electrophilic reaction) — реакции присоединения, в которых атаку на начальной стадии осуществляетэлектрофил — частица, заряженная положительно или имеющая дефицит электронов. На конечной стадии образующийся карбкатион подвергается нуклеофильной атаке.
В органической химии чаще всего атакующей электрофильной частицей является протон H+.
Несмотря на общность механизма различают реакции присоединения по связи углерод—углерод и углерод—гетероатом.
Общий вид реакций присоединения по двойной связи углерод-углерод:

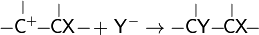
Реакции электрофильного присоединения распространены среди алкенов и алкинов и широко используются в промышленном химическом производстве и лабораторных синтезах.
Реакции радикального присоединения — реакции присоединения, в которых атаку осуществляют свободные радикалы — частицы, содержащие один или несколько неспаренных электронов. При этом радикалы могут атаковать как другие радикалы, так и нейтральные частицы.
Реакции радикального присоединения обозначают AdR.
Реакции свободно-радикального присоединения характерны для алкенов, которые часто вступают в них вместо реакций электрофильного присоединения в присутствии источника свободных радикалов
Механизм реакции радикального присоединения включает в себя следующие стадии:
Первая стадия — инициирование цепи. Она может начаться спонтанно, фотохимически, электрохимически, посредством нагревания или путем химического иницирования[2].
Вторая стадия — развитие цепи. На этой стадии радикалы реагируют с молекулами, образуя продукты реакции и новые радикалы.
Третья стадия — обрыв цепи или рекомбинация свободных радикалов.

Реакции радикального замещения ускоряются в условиях генерирования свободных радикалов и замедляются в присутствии веществ, улавливающих свободные радикалы.
Радикальное присоединение идет против правила Марковникова (эффект Хараша). Вызвано это повышенной стабильностью третичных, аллильных и некоторых других радикалов, образующихся при присоединении атакующего радикала в определённую позицию в молекуле.
8. Типы гибридизации в органических соединениях: алканы,алкины,алкены. SP-,SP2,-SP3 – гибридные орбитали
sp3 – гибридизация
Все четыре валентные орбитали участвуют в гибридизации. Валентный угол 109о28’ (тетраэдр). Атомы углерода образуют только простые (σ) связи – соединение насыщенное.
sp2 – гибридизация
Образуются три гибридные и одна негибридная орбиталь. Валентный угол 120о (плоские структуры, правильный треугольник). Гибридные орбитали образуют σ–связи. Негибридные орбитали образуют p-связи. sp2–Гибридизация характерна для непредельных соединений с одной p - связью.
sp – гибридизация
Образуются две гибридные и две негибридные орбитали. Валентный угол 180о (линейные структуры). Атом углерода в состоянии sp-гибридизации принимает участие в образовании двух двойных связей или одной тройной связи.
Каждый атом углерода в молекулах алканов находится в состоянии sp3-гибридизации — все 4 гибридные орбитали атома С идентичны по форме и энергии, 4 связи направлены в вершины тетраэдра под углами 109°28'.
Алки́ны (иначе ацетиленовые углеводороды) — углеводороды, содержащие тройную связь между атомами углерода, образующие гомологический ряд с общей формулой CnH2n-2. Атомы углерода при тройной связи находятся в состоянии sp-гибридизации.
Алке́ны (олефины, этиленовые углеводороды) — ациклические непредельные углеводороды, содержащие одну двойную связьмежду атомами углерода, образующие гомологический ряд с общей формулой CnH2n. Атомы углерода при двойной связи находятся в состоянии sp² гибридизации, и имеют валентный угол 120°.
