Химические свойства альдегидов и кетонов
· Реакции окисления:
Реакция протекает легко:
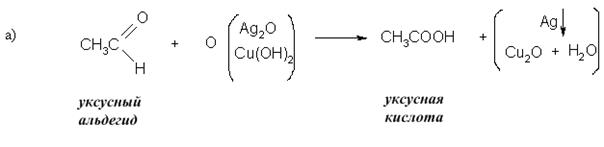
Реакция протекает трудно, лишь в жестких условиях:

Разрыв цепи кетонов при окислении происходит по правилу Попова: карбонильная группа остается с меньшим радикалом.
· Реакции восстановления (алюмогидрид лития – катализатор):

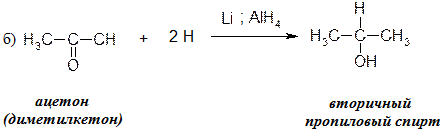
· Реакции альдольной конденсации протекают лишь с теми альдегидами, в которых присутствует водород у α-углеродного атома. Реакция может протекать как под влиянием щелочей, так и под влиянием кислот.
Так, альдольная конденсация под влиянием щелочей протекает в водных растворах по механизму AdN.
1 стадия: образование карбоаниона
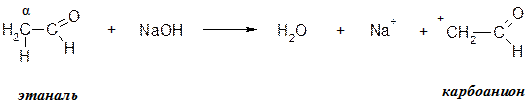
2 стадия: нуклеофильная аптека карбоанионом положительно заряженного углерода группы С=О с образованием алкоксид – иона

3 стадия: алкоксид-ион в водной среде присоединяет Н+ из КОН с образованием альдоля (альдегид + алкоголь)
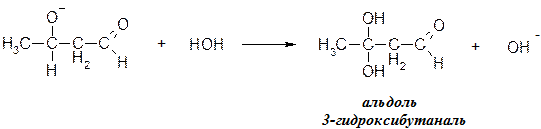
Таким путем под влиянием ферментов идет образование лимонной кислоты в цикле ТКК, нейраминовой кислоты в нервных клетках.
Часто альдольная конденсация сопровождается воды и образованием α,β-ненасыщенного карбонильного соединения (кротоновая конденсация):
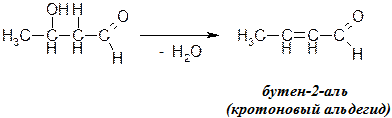
· Взаимодействие со спиртами (образование полуацеталей и ацеталей):

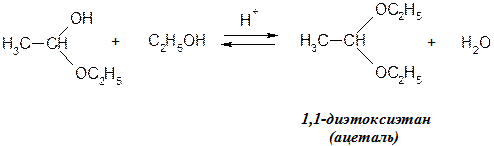
Моносахариды на 95,5% существуют в клетке в виде полуацеталей (внутренних).
Многократно повторенная реакция образования циклических ацеталей лежит в основе получения природных полисахаридов (крахмала, клетчатки).
· Галоформные реакции, приводящие к образованию водорода, хлороформа, бромоформа. Галоформные реакции протекают вследствие появления С–Н кислотности у α-углерода под влиянием отрицательного индуктивного эффекта (-I-эффект) рядом расположенной карбонильной группы.
1 стадия: образование трихлорзамещенного альдегида
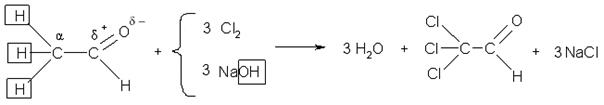
Трихлоруксусный
Альдегид (хлораль)
Галогены обладают (-)I – эффектом.
2 стадия: непрочное соединение – трихлоруксусный альдегид легко расщепляется под действием NaOH, так как оба его углерода несут частичные положительные заряды (δ+)

Галоформная реакция используется как способ получения карбоновых кислот и для обнаружения метилкетонов (ацетона) и ацетальдегида – йодоформная проба – в биологических жидкостях.
· Реакции присоединения – отщепления AN – E (образование оснований Шиффа):
1 стадия: нуклеофильная атака аминами карбонильного атома углерода

2 стадия: стабилизация биполярного иона
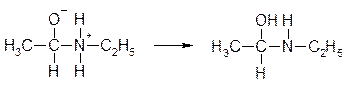
3 стадия: отщепление (элиминирование) с образованием основания Шиффа
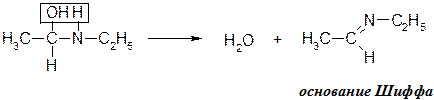
В организме образование оснований Шиффа идет при биосинтезе аминокислот из кетокислот и при распаде аминокислот через стадию переаминирования.
