Электролиз. Применение электролиза в технике
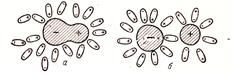
Чистая дистиллированная вода – это хороший диэлектрик. Раствор кислоты в воде – хороший проводник. Диполи воды, возникающие в результате действия электрического поля, окружают молекулу кислоты и «растаскивают» ее на ионы (рис.21).
Распад молекул на ионы под действием растворителя называют электролитической диссоциацией. 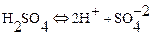
|
Рисунок 21. Электролитическая диссоциация
Рассмотрим процесс прохождения электрического тока в электролите. В электролитическую ванну налит раствор серной кислоты и опущены две платиновых пластины. Пластины называются электродами.Электрод, соединенный с (+) источника тока, называется анодом. Электрод, соединенный с (-) источника тока, называется катодом.
В результате электролитической диссоциации в растворе образуются ионы:
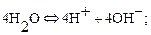
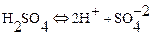
Процессы на катодеПроцессы на аноде
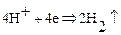
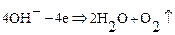
Здесь 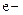 заряд электрона. На катоде выделяется газообразный водород, а на аноде – газообразный кислород. Из раствора уходят части молекул воды, а составные части кислоты остаются в растворе. Прохождение электрического тока через электролиты, сопровождающееся химическими превращениями вещества и выделением его на электродах, называется электролизом.В рассмотренном примере выделение вещества происходит при неактивном аноде, то есть анод выполнен из платины и не растворяется в электролите.
заряд электрона. На катоде выделяется газообразный водород, а на аноде – газообразный кислород. Из раствора уходят части молекул воды, а составные части кислоты остаются в растворе. Прохождение электрического тока через электролиты, сопровождающееся химическими превращениями вещества и выделением его на электродах, называется электролизом.В рассмотренном примере выделение вещества происходит при неактивном аноде, то есть анод выполнен из платины и не растворяется в электролите.
Если в электролитическую ванну налить раствор соли того же вещества, из которого сделан анод, то в процессе электролиза вещество выделится на катоде, а анод растворится. В этом случае анод называют активным, так как он реагирует с электролитом. Таким способом выделяют химически чистые металлы, например медь, серебро (рисунок 22) и т.д.
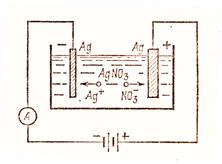 Электролиз применяется также для нанесения слоя одного металла на поверхность другого металла и для электрополировки поверхности металлов.
Электролиз применяется также для нанесения слоя одного металла на поверхность другого металла и для электрополировки поверхности металлов.
Ток в электролите подчиняется закону Ома.
|
Законы электролиза (законы Фарадея)
1-й закон Фарадея: Масса вещества 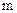 , выделяющегося при электролизе, прямо пропорциональна количеству электричества
, выделяющегося при электролизе, прямо пропорциональна количеству электричества 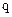 , прошедшего через раствор.
, прошедшего через раствор. 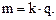
Коэффициент пропорциональности 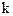 называют электрохимическим эквивалентомвещества. Поскольку
называют электрохимическим эквивалентомвещества. Поскольку 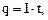 то
то 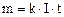 .
.