Количественное определение фенологликозидов
Нормативная документация предусматривает количественное определение арбутина в листьях толокнянки и брусники. Метод определения основан на йодометрическом титровании гидрохинона, полученного после извлечения и гидролиза арбутина. Разработан спектрофотометрический метод определения салидрозида в корневищах с корнями родиолы розовой. Исходя из строения фенольных гликозидов и их УФ спектров, возможно количественное хромато-спектрофотометрическое определение всех представителей этой группы.
На кафедре фармакогнозии и ботаники ИГМУ разработан фотоколориметрический метод количественного определения арбутина в растениях семейства грушанковых (Piraleaceae) для анализа сырья рамишии однобокой (боровой матки – Rhamischia secunda) и грушанки круглолистной (Pyrola rotundifolia).
Методика. Пробу сырья (грушанки круглолистной или рамишии однобокой) измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 1 мм. Около 0,5 г (точная навеска) измельченных листьев помещают в колбу вместимостью 100 мл, прибавляют 50 мл воды и нагревают на плитке, поддерживая слабое кипение в течение 30 мин. Горячее извлечение фильтруют в мерную колбу вместимостью 100 мл через бумажный фильтр диаметром 7 мм, избегая попадания частиц сырья на фильтр. В колбу с сырьем повторно прибавляют 25 мл воды очищенной и кипятят 20 мин. Горячее извлечение вместе с сырьем переносят на тот же фильтр и остаток на фильтре дважды промывают горячей водой (по 10 мл). К фильтрату прибавляют 3 мл раствора ацетата свинца основного, перемещают и по охлаждении доводят объем фильтрата водой очищенной до метки. Колбу помещают на кипящую водяную баню и выдерживают до полной коагуляции осадка. Горячую жидкость полностью отфильтровывают в сухую колбу через бумажный фильтр диаметром 10 см, прикрывая воронку часовым стеклом. От избытка свинца освобождаются добавлением насыщенного раствора сульфата натрия – 2 мл, образовавшийся осадок отфильтровывают через бумажный фильтр в сухую колбу вместимостью 100 мл. Готовят диазотированный сульфанил. Для этого 7 г сульфацил-натрия растворяют в 50 мл воды в мерной колбе вместимостью 100 мл, прибавляют 9 мл концентрированной хлористоводородной кислоты и доводят объем раствора водой до метки; 1 мл полученного раствора помещают в мерную колбу вместимостью 100 мл, ставят на лед, прибавляют 50 мл воды, 0,2 мл 10% раствора натрия нитрита, перемешивают и доводят объем раствора до метки. Раствор применяют свежеприготовленным.
В мерную колбу вместимостью 25 мл переносят 1 мл полученного фильтрата, прибавляют 2,5 мл диазотированного сульфанила и 0,16 мл 10% раствора гидроксида натрия и доводят объем раствора очищенной водой до метки, перемешивают (реакция идет при комнатной температуре, что дает более устойчивое окрашенное соединение) и через 20 мин измеряют оптическую плотность на фотоколориметре КФК-2 при длине волны 490 нм в кювете с длиной рабочего слоя 10 мм, используя в качестве раствора сравнения воду. Количественное содержание арбутина рассчитывают по формуле:
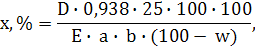
где D – оптическая плотность исследуемого раствора;
0,938 – коэффициент пересчета на безводный арбутин;
25 – общий объем исследуемого раствора;
100 – объем колбы;
w – влажность сырья, %;
E – удельный показатель поглощения арбутина при длине волны 490 нм, равный 221,5;
a – навеска сырья, г;
b – объем извлечения, взятый для анализа.
КУМАРИНЫ
Кумарины – природные соединения, в основе которых лежит бензо – α – пирон, представляющий собой лактон цис – орто - оксикоричной кислоты.
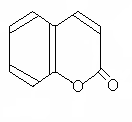
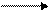
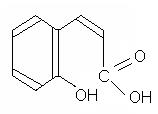
цис – орто – оксикоричная кумарин
кислота
Кумарин – родоначальник соединений этой группы. Впервые это соединение было выделено в 1980 году Фогелем из плодов растения диктерикс семейства бобовые. Позднее кумарины были обнаружены в 50 годах различных семейств. В развитии химии кумаринов большой вклад внес ученый Шпет, из отечественных ученых – Никонов и Кузнецова. В настоящее время известно 1,5 тыс. растений, содержащих кумарины. Для 150 соединений установлена химическая структура и изучена фармакологическая активность. В природе чаще всего встречаются простые производные кумаринов. В растениях чаще всего они находятся в свободном состоянии в виде агликонов, редко бывают гликозидированы.
Кумарины широко распространены в растительном мире, чаще встречаются в высших растениях, редко в грибах и лишайниках. Они наиболее типичны для семейств бобовые, сельдерейные, рутовые, камнеломковые.
Кумарины локализуются в различных органах растений, чаще всего в корнях, коре, плодах. У сельдерейных кумариновые соединения могут локализоваться в эфирно – масличных канальцах. Очень часто в одном растении может быть от 5 до 10 кумаринов различной структуры. Содержание кумаринов в разных растениях, например у фенхеля, колеблется от 0,2 до 10%.
В зависимости от концентрации в плодах, кумарины могут выступать в роли ингибиторов или активаторов роста, способствуют прорастанию семян. Они обладают защитными свойствами при некоторых заболеваний растений, так как проявляют противомикробные свойства. Многие кумарины обладают спазмолитической активностью; коронарорасширяющее действие оказывают виснадин и дигидросамидин из корней вздутоплодника сибирского.
Некоторые кумарины обладают фотодинамической активностью, т.е. способны повышать чувствительность кожи к ультрафиолетовым лучам, и поэтому находят применение в терапии витилиго такие препараты, как аммифурин из плодов амми большой, бероксан из плодов пастернака посевного, псорален из плодов псоралеи костянковой.
Кумарины обладают антикоагулянтными свойствами. Дикумарол был предложен как препарат для профилактики и лечения тромбозов и тромбофлебитов. Он впервые был обнаружен в старом лежалом сене, в котором много было донника, такое сено вызывало кровотечение у порезанных животных. На основе дикумарола получены синтетические препараты, обладающие более высокими антикоагулянтными свойствами.
Некоторым кумаринам свойственна антимикробная активность (остхол из жгун–корня); ряд кумаринов обладают эстрогенной активностью, гонадотропным действием (куместролы клевера). Таким образом, кумарины характеризуются разнообразным действием на организм человека, однако широкого использования в медицине они не получили из-за отсутствия оптимальных лекарственных форм, создание которых затруднено плохой растворимостью кумаринов в воде.
Классификация кумаринов
Все известные кумарины в зависимости от химической структуры делят на следующие группы.
