Химические свойства аминокислот
1.Аминокислоты проявляют амфотерные свойства и кислот и аминов, а также специфические свойства, обусловленные совместным присутствием указанных групп. В водных растворах АМК существуют в виде внутренних солей (биполярных ионов). Водные растворы моноаминомонокарбоновых кислот на лакмус нейтральны, т.к. в их молекулах содержится равное число -NН2- и -СООН групп. Эти группы взаимодействуют между собой с образованием внутренних солей:
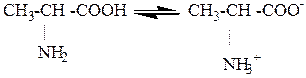
Такая молекула имеет в двух местах противоположные заряды: положительный NН3+ и отрицательный на карбоксиле –СОО-. В связи с этим внутренняя соль АМК имеет название биполярного иона или Цвиттер–иона (Zwitter – гибрид).
Биполярный ион в кислой среде ведет себя как катион, так как подавляется диссоциация карбоксильной группы; в щелочной среде – как анион. Существуют значения рН специфические для каждой аминокислоты, в которой количество анионных форм в растворе равно количеству катионных форм. Значение рН при котором общий заряд молекулы АМК равен 0, называется изоэлектрической точкой АМК (pIАК).
Водные растворы моноаминодикарбоновых кислот обладают кислой реакцией среды:
HООС-СH2-СH-СOOH « - OOC-CH2-CH–COO - + H+
| |
NH2 NH3+
Изоэлектрическая точка моноаминодикарбоновых кислот находится в кислой среде и такие АМК называют кислыми.
Диаминомонокарбоновые кислоты обладают в водных растворах основными свойствами (участие воды в процессе диссоциации показывать обязательно):
NH2 NH3+
| |
NH2-(CH2)4-CH-COOH + H2O « NH3+-(CH2)4-CН–COO - + OH-
Изоэлектрическая точка диаминомонокарбоновых кислот находится в при рН>7 и такие АМК называют основными.
Являясь биполярными ионами, аминокислоты проявляют амфотерные свойства: они способны образовывать соли как с кислотами, так и с основаниями:
Взаимодействие с соляной кислотой HCl приводит к образованию соли:
R-CH-COOH + HCl ® R-CH-COOH
| |
NH2 NH3+Сl-
Взаимодействие с основанием приводит к образованию соли:
R-CH(NH2)-COOH + NaOH ® R-CH(NH2)-COONa + H2O
2. Образование комплексов с металлами – хелатный комплекс. Строение медной соли гликокола (глицина) можно изобразить следующей формулой:

. Почти вся имеющаяся в организме человека медь (100 мг) связана с белками (аминокислотами) в виде этих устойчивых клешневидных соединений.
3. Подобно другим кислотам аминокислоты образуют сложные эфиры, галоген ангидриды, амиды.
4. Реакции декарбоксилирования протекают в организме при участии специальных ферментов декарбоксилаз: получающиеся при этом амины (триптамин, гистамин, серотинин) называются биогенными аминами и являются регуляторами ряда физиологических функций человеческого организма.
5. Взаимодействие с формальдегидом (альдегидами)
R-CH-COOH + H2C=О ® R-CH-COOH
| |
NH2 N= CH2
Формальдегид связывает NН2– группу, -СООН группа остается свободной и может быть оттитрована щелочью. Поэтому данная реакция используется для количественного определения аминокислот (метод Сёренсена).
6. Взаимодействие с азотистой кислотой приводит к образованию гидроксикислот и выделению азота. По объему выделившегося азота N2 определяют его количественное содержание в исследуемом объекте. Эта реакция применяется для количественного определения аминокислот (метод Ван–Слайка):
R-CH-COOH + HNO2 ® R-CH-COOH + N2 + H2O
| |
NH2 OH
Это один из способов дезаминирования АМК вне организма
7. Ацилирование аминокислот. Аминогруппу АМК можно ацилировать хлорангидридами и ангидридами кислот уже при комнатной температуре.
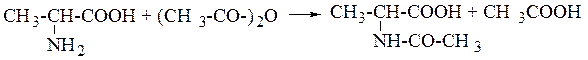
Продуктом записанной реакции является ацетил-α-аминопропионовая кислота.
Ацильные производные АМК широко используются при изучении последовательности их в белках и в синтезе пептидов (защита аминогруппы).
8.Специфические свойства, реакции, связанные с наличием и взаимным влиянием амино- и карбоксильной групп - образование пептидов. Общим свойством a-АМК является процесс поликонденсации, приводящий к образованию пептидов. В результате этой реакции формируются амидные связи по месту взаимодействию карбоксильной группы одной АМК и аминогруппы другой АМК. Другими словами, пептиды – это амиды, образующиеся в результате взаимодействия аминогрупп и карбоксилов аминокислот. Амидная связь в таких соединениях называется пептидной связью (разобрать строение пептидной группы и пептидной связи: трехцентровая р,p-сопряженная система)
 или -NH-CO- или -NH-CO- | Пептидная группа относится к р-,p-сопряженной системе, в составе которой атомы С, О и N образуют s-связи, которые лежат в одной плоскости. За счет образования единого делокализованного 4p-электронного облака вращение вокруг С-N связи затруднено. При этом a-углеродные звенья находятся в выгодном транс-положении. |
В зависимости от числа аминокислотных остатков в молекуле различают ди-, три-, тетрапептиды и т.д. вплоть до полипептидов (до 100 остатков АМК). Олигопептиды содержат от 2 до 10 остатков АМК, белки - более100 остатков АМК.В общем виде полипептидную цепь можно представить схемой:
H2N-CH-CO-NH-CH-CO-NH-CH-CO-... -NH-CH-COOH
| | | |
R1 R2 R3 Rn
Где R1, R2, … Rn – радикалы аминокислот.
Понятие о белках.
Наиболее важными биополимерами аминокислот являются белки – протеины. В организме человека насчитывается около 5млн. различных белков, которые входят в состав кожи, мышц, крови и других тканей. Белки (протеины) получили свое название от греческого слова «protos» - первый, важнейший. Белки выполняют ряд важнейших функций в организме: 1. Строительная функция; 2. Транспортная функция; 3. Защитная функция; 4. Каталитическая функция; 5. Гормональная функция; 6. Питательная функция.
Все природные белки образуются из мономеров аминокислот. При гидролизе белков образуется смесь АМК. Этих АМК – 20.
4. Иллюстративный материал:презентация
5. Литература:
Основная литература:
1. Биоорганическая химия: учебник. Тюкавкина Н.А., Бауков Ю.И. 2014г.
- Сейтембетов Т.С. Химия : учебник - Алматы : ТОО"ЭВЕРО", 2010. - 284 с
- Болысбекова С. М. Химия биогенных элементов : учебное пособие - Семей, 2012. - 219 с. : ил
- Веренцова Л.Г. Неорганическая ,физическая и коллоидная химия : учебное пособие - Алматы : Эверо, 2009. - 214 с. : ил.
- Физическая и коллоидная химия /Под ред.А.П.Беляева.- М.: ГЭОТАР МЕДиа, 2008
- Веренцева Л.Г. Неорганическая, физическая и коллоидная химия,(проверочные тесты) 2009
Дополнительная литература:
- Равич-Щербо М.И., Новиков В.В. Физическая и коллоидная химия. М. 2003.
2. Слесарев В.И. Химия. Основы химии живого. С-Пб.: Химиздат, 2001
3. Ершов Ю.А. Общая химия. Биофизическая химия. Химия биогенных элементов. М.: ВШ, 2003.
4. Асанбаева Р.Д., Илиясова М.И. Теоретические основы строения и реакционной способности биологически важных органических соединений. Алматы, 2003.
- Руководство к лабораторным занятиям по биоорганической химии под ред. Н.А. Тюкавкиной. М., Дрофа,2003.
- Глинка Н.Л. Общая химия. М.,2003.
- Пономарев В.Д. Аналитическая химия ч.1,2 2003
6. Контрольные вопросы (обратная связь):
1. Что преопределяет структуру полипептидной цепи в целом?
2. К чему приводит денатурация белка?
3. Что называют изоэлектрической точкой ?
4. Какие аминокислоты называются незаменимыми?
5. Каким же образом белки образуются в нашем организме?
