Синтез бутилацетата (уксусно-бутилового эфира)
Цель:получение бутилацетата
Реактивы: уксусная кислота (ледяная) – 21 г (20 мл); н-бутиловый спирт – 25 г (31 мл); серная кислота (ρ = 1,84 г/см3) – 3,7 г (2 мл); хлорид кальция безводный; гидрокарбонат натрия, 5%-ный раствор.
Посуда и оборудование: колба круглодонная вместимостью 100 мл; капельная воронка; делительная воронка; холодильник водяной; насадка Дина-Старка; колба Вюрца; термометр; двурогий форштос; баня песчаная.
Теоретические основы
Замена атома водорода амино- или гидроксигруппы остатком кислородсодержащей минеральной, карбоновой или сульфокислоты называется ацилированием.
Метод ацилирования применяется для двух различных целей. В одних случаях введённая ацильная группа сохраняется до образования конечного продукта, в других – ацилирование осуществляется для защиты амино- или гидроксигруппы с освобождением ацила после использования ацилированного продукта в каких-либо реакциях.
Ацилирование спиртов (фенолов) и аминов протекает по механизму
нуклеофильного замещения. Строго установлено, что в этой реакции роль субстратов выполняют ацилирующие агенты, а их взаимодействие с нуклеофилами протекает через стадию образования тетраэдрического промежуточного соединения (I):
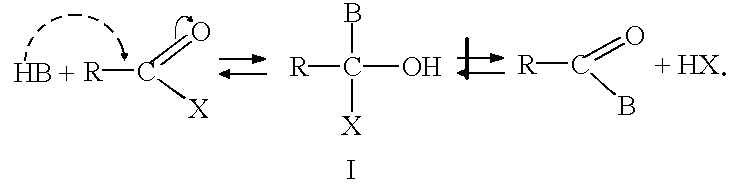
(здесь В = OR', NHR'; X = OH, Hal, OCOR, OR).
Реакции, катализируемые кислотами, протекают с образованием аналогичных промежуточных продуктов. Например, в процессе этерификации реакционноспособной частицей является соединение (II):
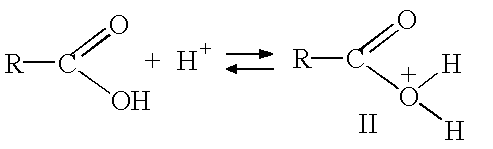
которое, присоединяя молекулу спирта, образу2ет комплекс (III) с последующим отщеплением воды:
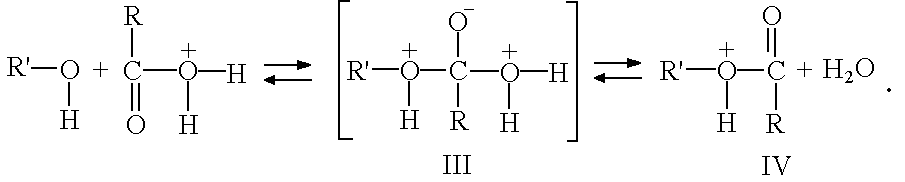
В практике ацилирования широкое применение получили уксусная и муравьиная кислоты, уксусный и фталевый ангидриды, а также хлорангидриды кислот: хлористый ацетил CH3COCl, хлористый бензоил С6H5COCl.
 Экспериментальная часть
Экспериментальная часть
CH3COOH + CH3(CH2)3OH CH3COO(CH2)3CH3 + H2O.
Порядок выполнения работы
В круглодонную колбу, соединённую посредством двурогого форштоса с капельной воронкой и обратным холодильником через насадку Дина-Старка, помещают 20 мл ледяной уксусной кислоты, 31 мл н-бутилового спирта и 2 мл концентрированной серной кислоты. Содержимое нагревают до кипения на песчаной бане. Выделяющаяся при реакции вода отгоняется с бутиловым спиртом в виде азеотропной смеси и попадает в насадку Дина-Старка. По мере накопления жидкость из насадки сливают в небольшой мерный цилиндр, верхний слой (бутиловый спирт) через капельную воронку возвращают в реакционную колбу. Реакция считается законченной, когда выделится всё количество воды, рассчитанное по уравнению реакции, или когда слой воды в насадке перестанет изменяться.
Полученный эфир промывают в делительной воронке сначала водой, затем раствором гидрокарбоната натрия до нейтральной реакции по индикаторной бумажке и вновь водой. Отделив эфир от водного слоя, его высушивают прокалённым хлоридом кальция и перегоняют, собирая фракцию, кипящую при 124-126°С. Выход 27 г (70% от теоретического).
Уксуснобутиловый эфир (бутиловый эфир уксусной кислоты, бутилацетат) – бесцветная жидкость с эфирным запахом, смешивается с этиловым спиртом и диэтиловым эфиром, в воде растворяется слабо (1 г в 100 мл при 25°С).
Температура кипения 124...126°С, 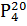 = 0,8820,
= 0,8820, 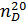 = 1,3941.
= 1,3941.
ИК-спектр: νС=О=1735 см–1.
Контрольные вопросы:
1. Что такое ацитилирование ?
2. По какому процессу происходит ацитилирование ?
3. Опишите физико-химические свойства бутилацетата ?
4. В какие реакции вступает дибутилацетат ?
5. Какие сферы применения бутилацетата вы знаете ?
Лабораторная работа №5
Получение α-нитронафталина
Цель:получить α-нитронафталин
Реактивы: нафталин – 5 г; азотная кислота (ρ = 1,4 г/см3) – 3,9 г; серная кислота (ρ = 1,84 г/см3) – 5,0 мл; этиловый спирт.
Посуда и оборудование:фарфоровый стакан вместимостью 50 мл; термометр; мешалка.
Теоретические основы
Введение в молекулу органического соединения нитрогруппы называется реакцией нитрования.
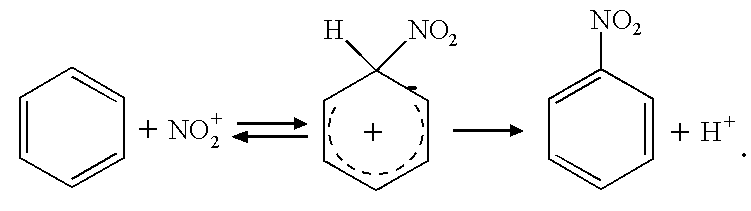
В зависимости от природы субстрата и характера нитрующего агента механизм реакции может быть различным. Так, введение нитрогруппы в ароматическое ядро протекает по электрофильному механизму. Для наиболее распространённого случая нитрования смесью концентрированных азотной и серной кислот на примере бензола его можно представить следующей схемой:
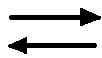
 HNO3 + 2H2SO4 NO2+ + 2HSO4– + Н3О+,
HNO3 + 2H2SO4 NO2+ + 2HSO4– + Н3О+,
Электрофильный характер реакции определяется атакой на молекулу бензола нитроний-катиона NO2+ с образованием промежуточного σ-комплекса и последующим отщеплением прoтона.
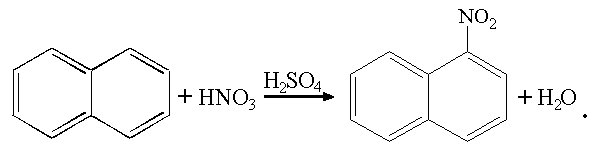 Экспериментальная часть
Экспериментальная часть
Порядок выполнения работы
В фарфоровом стакане, снабжённом мешалкой и термометром, смешивают 5,0 мл серной кислоты с 2,7 мл воды и приливают 3,9 г (2,8 мл) азотной кислоты. К нитрующей смеси, нагретой до 50°С (термометр в смеси), вносят 5,0 г хорошо измельчённого нафталина. Перемешивание с помощью механической мешалки ведут в течение 1 ч при 50°С. Затем температуру повышают до 60°С и перемешивают ещё 1 ч. После охлаждения реакционной массы полученный нитронафталин всплывает на поверхность кислоты в виде пористой лепёшки. Продукт отделяют и промывают в фарфоровой чашке кипящей водой несколько раз. При этом с парами воды отгоняются остатки нафталина. Расплавленный нитронафталин выливают тонкой струёй в холодную воду при сильном перемешивании. Застывший в виде мелких шариков продукт фильтруют и сушат на воздухе. Выход 5,8 г (86 % от теоретического). Очистку α-нитронафталина производят
перекристаллизацией из изопропилового спирта.
α-Нитронафталин – жёлтый кристаллический продукт с ттемпературой плавления 59-60°С. Растворяется в этаноле, эфире, хлороформе, ацетоне.
Контрольные вопросы:
1. Что такое нитрование ?
2. По какому процессу происходит нитрование ?
3. Опишите физико-химические свойства α-нитронафталина?
4. В какие реакции вступает α-нитронафталин?
5. В какой сфере применяется α-нитронафталин ?
6. Чем объясняется токсичность α-нитронафталина ?
Лабораторная работа №6
Синтез n – толуолсульфокислоты
Цель:получение n – толуолсульфокислоты
Реактивы: толуол – 16 мл, серная кислота – 9,5 мл ( ρ =1,835 г/см3), карбонат натрия – 8 г, хлорид натрия – 12 г.
Посуда и оборудование:колба круглодонная длинногорлая (100 мл), холодильник Либиха, стакан химический, воронка Бюхнера, колба Бунзена, прибор для отсасывания.
Теоретические основы
Механизм С-алкилирования ароматического ядра включает участие катализаторов, способствующих образованию карбокатионов:
Alk – Cl + AlCl3 → Alk - Cl … AlCl3 → Alk+ + AlCl4–,
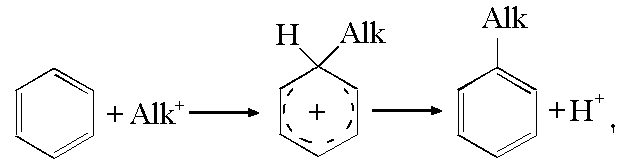
H+ + AlCl4– → HCl + AlCl3.
В синтезе алкилпроизводных ароматического ряда в качестве алкилирующих агентов используются галогеналкилы, спирты и алкены.
Во время взаимодействия ароматического соединения с первичными галогеналкилами, имеющими неразветвлённую цепь углеродных атомов, могут получаться производные с разветвлённой боковой цепью. Например, из бензола и пропилхлорида получается изопропилбензол, из бутилбромида и бензола – втор-бутилбензол.
Экспериментальная часть
n – СН3С6Н4SO3H + NaCI → n – СН3С6Н4SO3Na + HCI.
Порядок выполнения работы
В круглодонную колбу прибора помещают 16 мл толуола и осторожно вносят 9,5 мл концентрированной серной кислоты. Реакционную жидкость в течение 1 ч слабо кипятят, время от времени встряхивая колбу (для перемешивания слоев). Реакция считается законченной, когда слой толуола почти исчезает и из холодильника изредка стекают капли конденсата. Затем теплую реакционную смесь выливают в стакан с 70 мл воды (если смесь начинает кристаллизоваться, то ее надо подогреть) и колбу ополаскивают из промывалки. Кислый раствор осторожно нейтрализуют 8 г карбоната натрия, прибавляя его небольшими порциями, добавляют в раствор 20 г хлорида натрия и нагревают смесь до кипения (если хлорид натрия не растворяется, добавляют еще немного воды). Раствор охлаждают водой со льдом.
Выпавшие кристаллы натриевой соли n-толуолсульфокислоты отсасывают на воронке Бюхнера и отжимают между листами фильтровальной бумаги. Выход – 8 г.
Контрольные вопросы:
1. Что такое С-алкилирования?
2. В чем отличие С-алкилирования, N-алкилирования, S-алкилирования?
3. Опишите физико-химические свойства n-толуолсульфокислоты ?
4. В какие реакции вступает n-толуолсульфокислоты?
5. Какие сферы применения n-толуолсульфокислоты вы знаете ?
Лабораторная работа №7
