Гидратная теория растворов Д.И. Менделеева (представлять).
Растворы – гомогенные (однородные) системы переменного состава, которые содержат два или несколько компонентов и продукты их взаимодействия.
Обязательно одним из компонентов является растворитель, остальные компоненты – растворенные вещества.
Растворителем является то вещество, которое в чистом виде имеет то же состояние, что и раствор. Если же таких компонентов несколько, то растворителем является тот, содержание которого в растворе больше.
Растворы бывают:
1. Жидкие (раствор NaCl в воде, раствор I2 в спирте).
2. Газообразные (смеси газов, например: воздух – 21 % O2 + 78 % N2 + 1 % др. газов).
3. Твердые (сплавы металлов, например: Cu + N, Au + Ag).
Наиболее распространены жидкие растворы. Они состоят из растворителя (жидкости) и растворенных веществ (газообразных, жидких, твердых).
| Жидкие растворы | ||
| жидкость + газообразное вещество (р-р O2 в воде) | жидкость + жидкое вещество (р-р H2SO4 в воде) | жидкость + твердое вещество (р-р сахара в воде) |
Такие растворы могут быть водные и неводные.
Водные – растворы, в которых растворителем является вода.
Неводные – растворы, в которых растворителями являются другие жидкости (бензол, спирт, эфир и др.)
Долгое время на природу растворения существовало две точки зрения: физической и химической. Согласно первой, растворы рассматривались как механические смеси, согласно второй – как нестойкие химические соединения молекул растворенного вещества и растворителя. Последняя точка зрения была высказана Д.И. Менделеевым в 1887 г. и является в настоящее время общепризнанной.
ОСНОВНЫЕ ПОЛОЖЕНИЯ ХИМИЧЕСКОЙ ТЕОРИИ РАСТВОРОВ, созданной Менделеевым, сводятся к следующему:
1. Образование и существование раствора обусловлено взаимодействиями между всеми частицами, как уже существовавшими, так и образующимися при растворении.
2. Раствор является динамической системой, в которой распадающиеся соединения находятся в подвижном равновесии с продуктами распада в соответствии с законом действия масс.
При растворении вещества происходят два процесса, связанные с изменениями энергии системы «вещество – растворитель»:
1) разрушение структуры растворяемого вещества (при этом затрачивается определенная энергия) – реакция эндотермическая.
2) взаимодействие растворителя с частицами растворенного вещества (происходит выделение тепла) – реакция экзотермическая.
В зависимости от соотношения этих тепловых эффектов процесс растворения вещества может быть экзотермическим (∆H < O) или эндотермическим (∆H > O).
Теплота растворения ∆H – это количество теплоты, выделяющееся или поглощающееся при растворении 1 моль вещества.
Теплота растворения для различных веществ различна. Так, при растворении в воде гидроксида калия или серной кислоты температура значительно повышается (∆H < O), а при растворении нитратов калия или аммония резко снижается (∆H > O).
Выделение или поглощение теплоты при растворении есть признак химической реакции. В результате взаимодействия растворенного вещества с растворителем образуются соединения, которые называются сольватами (или гидратами, если растворителем является вода). Многие соединения такого вида непрочны, однако, в ряде случаев образуются прочные соединения, которые легко можно выделить из раствора кристаллизацией.
При этом выпадают кристаллические вещества, содержащие в своем составе молекулы воды, их называют кристаллогидратами (например: медный купорос CuSO4 * 5 H2O – кристаллогидрат); вода, входящая в состав кристаллогидратов, называется кристаллизационной.
Представления о гидратации (соединение вещества с водой) было выдвинуто и развито русским ученым И.А. Каблуковым и В.А. Кистяковским. на основе этих представлений произошло объединение химической и физической точек зрения на растворы.
Таким образом, растворение – это не только физический, но и химический процесс, а растворы – физико-химические системы.
Выводы:
1.Растворы – гомогенные (однородные) системы переменного состава, которые содержат два или несколько компонентов и продукты их взаимодействия.
2.Растворы состоят из растворителя и растворенного вещества.
3.Растворы бывают:
А)Жидкие (раствор NaCl в воде, раствор I2 в спирте).
Б)Газообразные (смеси газов, например: воздух – 21 % O2 + 78 % N2 + 1 % др. газов).
В)Твердые (сплавы металлов, например: Cu + N, Au + Ag).
4.
| Жидкие растворы | ||
| жидкость + газообразное вещество (р-р O2 в воде) | жидкость + жидкое вещество (р-р H2SO4 в воде) | жидкость + твердое вещество (р-р сахара в воде) |
Такие растворы могут быть водные и неводные.
5.Водные – растворы, в которых растворителем является вода.
6.Неводные – растворы, в которых растворителями являются другие жидкости (бензол, спирт, эфир и др.)
7.ОСНОВНЫЕ ПОЛОЖЕНИЯ ХИМИЧЕСКОЙ ТЕОРИИ РАСТВОРОВ:
1.Образование и существование раствора обусловлено взаимодействиями между всеми частицами, как уже существовавшими, так и образующимися при растворении.
2.Раствор является динамической системой, в которой распадающиеся соединения находятся в подвижном равновесии с продуктами распада в соответствии с законом действия масс.
8.При растворении вещества происходят два процесса, связанные с изменениями энергии системы «вещество – растворитель»:
1.разрушение структуры растворяемого вещества (при этом затрачивается определенная энергия) – реакция эндотермическая.
2.взаимодействие растворителя с частицами растворенного вещества (происходит выделение тепла) – реакция экзотермическая.
9.Выделение или поглощение теплоты при растворении есть признак химической реакции.
10. В результате взаимодействия растворенного вещества с растворителем образуются соединения, которые называются сольватами (или гидратами, если растворителем является вода)
.
11.Кристаллические вещества, содержащие в своем составе молекулы воды, называют кристаллогидратами (например: медный купорос CuSO4 * 5 H2O – кристаллогидрат); вода, входящая в состав кристаллогидратов, называется кристаллизационной
12.Растворение – это не только физический, но и химический процесс, а растворы – физико-химические системы.
Виды растворов (знать).
Растворение – процесс обратимый: растворяемое вещество + растворитель ↔ вещество в растворе ± Q.
По соотношению преобладания числа частиц, переходящих в раствор и удаляющихся из раствора, различают растворы насыщенные, ненасыщенные и перенасыщенные.
С другой стороны, по относительным количествам растворенного вещества и растворителя растворы подразделяются на разбавленные (содержат мало растворенного вещества) и концентрированные (содержат много растворенного вещества).
Раствор, в котором данное вещество при данной температуре больше не растворяется, т.е. раствор находится в равновесии с растворяемым веществом, называется насыщенным, а раствор, в котором еще можно растворить добавочное количество данного вещества – ненасыщенным. В перенасыщенных растворах вещества содержится больше, чем в насыщенном. Растворимостью называется свойство вещества растворяться в воде и в других растворителях. Мерой растворимости или коэффициентом растворимости вещества при определенной температуре служит число граммов его, растворяющихся в 100 г воды.
По растворимости в воде твердые вещества условно делят на 3 группы:
1. Вещества, хорошо растворимые в воде (10 г вещества в 100, 0 воды. Например, в 1 л воды растворяется 200 г сахара).
2. Вещества, малорастворимые в воде (от 0, 01 до 10 г вещества в 100 г воды. Например: гипс CaSO4 в 1 л растворяется 2, 0).
3. Вещества, практически нерастворимые в воде (0, 01 г в 100, 0 воды. Например, AgCl – в 1 л воды растворяется 1, 5 * 10-3 г).
Растворимость вещества зависит от природы растворителя, от природы растворенного вещества, температуры, давления (для газов).
Растворимость газов при повышении температуры уменбшается, при повышении давления увеличивается.
Зависимость растворимости твердых веществ от температуры показывает кривая растворимости.
Растворимость многих твердых веществ увеличивается при повышении температуры.
По кривым растворимости можно определить:
1. Коэффициент растворимости веществ при различных температурах.
2. Массу растворенного вещества, которое выпадает в осадок при охлаждении раствора от t10C до t20C.
Процесс выделения вещества путем испарения или охлаждения его насыщенного раствора называется перекристаллизацией. Перекристаллизация используется для очистки веществ.
К сожалению, до настоящего времени не существует теории, позволяющей объединить результаты отдельных исследований и вывести общие законы растворимости. Подобное положение в значительной степени обусловлено тем, что растворимость различных веществ очень различно зависит от температуры.
Единственно, чем можно до некоторой степени руководствоваться – это старинным, найденным на опыте правилом: подобное растворяется в подобном. Смысл его в свете современных взглядов на строение молекул состоит в том, что если у самого растворителя молекулы неполярные или малополярные (например, бензол, эфир), то в нем будут хорошо растворяться от вещества с неполярными или малополярными молекулами, хуже – вещества с большей полярностью и практически не будут растворяться вещества, построенные по ионному типу. Наоборот, растворитель с сильно выраженным полярным характером молекул (например, вода) будет, как правило, хорошо растворять вещества с молекулами полярного и отчасти ионного типов и плохо – вещества с неполярными молекулами.
Выводы:
1.Растворение – процесс обратимый: растворяемое вещество + растворитель ↔ вещество в растворе ± Q.
2.По соотношению преобладания числа частиц, переходящих в раствор и удаляющихся из раствора, различают растворы насыщенные, ненасыщенные и перенасыщенные.
3.По относительным количествам растворенного вещества и растворителя растворы подразделяются на разбавленные (содержат мало растворенного вещества) и концентрированные (содержат много растворенного вещества).
4.Раствор, в котором данное вещество при данной температуре больше не растворяется называется насыщенным, а раствор, в котором еще можно растворить добавочное количество данного вещества – ненасыщенным. В перенасыщенных растворах вещества содержится больше, чем в насыщенном.
5.Растворимостью называется свойство вещества растворяться в воде и в других растворителях.
6.Растворимость вещества зависит от природы растворителя, от природы растворенного вещества, температуры, давления (для газов).
4. Способы выражения концентрации растворов: массовая доля
(знать).
Количественный состав раствора определяется его концентрацией.
Концентрация – это количество растворенного вещества, отнесенное к единице объема.
Различают два типа обозначений концентрации веществ – аналитические и технические.
Аналитические обозначения (молярная концентрация растворенного вещества, молярная концентрация эквивалента, молярность) – употребляются для растворов реагентов, применяемых в анализе веществ. здесь в качестве основной массовой единицы веществ используют моль.
Технические обозначения концентраций широко распространены в технике, медицине, фармации.
Объемный процент употребляют для обозначения концентрации смесей жидкостей или газов.
Массообъемный процент – количество вещества в граммах, содержащееся в 100 мл раствора.
Массовый процент (%) – количество граммов растворенного вещества, содержащееся в 100 г раствора.
Соотношение массы растворенного вещества к массе раствора называют массовой долей, ее выражают в долях единицы или процентах (устар. – процентная концентрация).
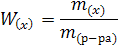
где: W(x) – массовая доля вещества х
m(x) – масса вещества х
m – масса всей системы (раствора)
Масса раствора представляет собой сумму масс растворенного вещества и растворителя: mр-ра = m(в-ва) + m(р-ля)
Например: если массовая доля уксусной кислоты равна 0, 03 (3 %), то это означает, что в растворе уксусной кислоты массой 100 г содержится CH3COOH массой 3 г и воды массой 100 – 3 = 97 г.
Если в условиях задачи указана плотность раствора, тогда предложенная формула выглядит так:

где: ρ – плотность раствора.
