Свойства водных растворов пав
Отметим три основных свойства водных растворов ПАВ:
1. Способность значительно снижать поверхностное натяжение на границе
раздела фаз.
2. Способность к самопроизвольному мицеллообразованию.
3. Солюбилизация.
СПОСОБНОСТЬ ПАВ
СНИЖАТЬ ПОВЕРХНОСТНОЕ НАТЯЖЕНИЕ
НА ГРАНИЦЕ РАЗДЕЛА ФАЗ
Эта способность обусловлена высокой поверхностной
активностью ПАВ: g = 

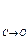 , которая зависит, главным образом, от длины углеводородного радикала; с ее увеличением поверхностная активность возрастает. Как отмечалось в главе 3, правило Дюкло–Траубе гласит: увеличение длины углеводородного радикала на одну группу -СН2- приводит к возрастанию поверхностной активности в 3–3,5 раза.
, которая зависит, главным образом, от длины углеводородного радикала; с ее увеличением поверхностная активность возрастает. Как отмечалось в главе 3, правило Дюкло–Траубе гласит: увеличение длины углеводородного радикала на одну группу -СН2- приводит к возрастанию поверхностной активности в 3–3,5 раза.
При большой длине углеводородных радикалов, когда заметно проявляется взаимодействие между молекулами ПАВ на поверхности, поверхностная активность увеличивается медленнее, чем это следует из правила Дюкло–Траубе. Поверхностную активность коллоидных ПАВ (g) можно приближенно оценить так: для неионогенных ПАВ: g 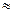

 ;
;
для ионогенных ПАВ: g  ;
;
где 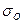
 поверхностное натяжение воды;
поверхностное натяжение воды; 
 – поверхностное натяжение
– поверхностное натяжение
раствора ПАВ при критической концентрации мицеллообразования; ККМ–критическая концентрация мицеллообразования ПАВ; v–число ионов, образующихся при диссоциации одной молекулы ПАВ.
Поверхностная активность ПАВ (g)непосредственно определяет адсорбционную способность ПАВ: чем она больше, тем больше адсорбционная способность. Адсорбируясь на частицах дисперсной фазы, молекулы ПАВ создают на их поверхности адсорбционно-сольватные защитные оболочки, которые из–за соответствующей ориентации молекул ПАВ («хвостом» или «головкой») значи–тельно снижают поверхностное натяжение и препятствуют слипанию или слиянию частиц (рис. 12.2).

Рис. 12.2. Некоторые границы раздела фаз
Моющее действие коллоидных ПАВ основано на совокупности коллоидно–химических процессов.
1. В присутствии ПАВ вследствие уменьшения поверхностного натяжения улучшается смачивание твердой поверхности, жидкость лучше проникает в тонкие капилляры ткани.
2. Молекулы мыла, адсорбируясь на поверхности волокна и частицах твердых или жидких загрязнений, создают адсорбционный слой, что обусловливает возникновение расклинивающего давления. Это способствует от–рыву частиц и переходу в моющую жидкость.
3. Адсорбционные пленки на поверхности частиц загрязнений придают этим частицам высокую агрегативную устойчивость и предупреждают их прилипание к поверхности волокна в другом месте.
4. В присутствии коллоидных ПАВ в растворе образуется пена, которая способствует механическому уносу частиц загрязнений от поверхности.
5. Масляные загрязнения удерживаются в водной среде вследствие солюбилизации, о которой речь пойдет дальше.
Важной количественной характеристикой ПАВ является гидрофилъно–липофилъный баланс (ГЛБ). Числа ГЛБ характеризуют соотношение между гидрофильными и гидрофобными свойствами: чем выше число ГЛБ, тем больше баланс сдвинут в сторону гидрофильных (полярных) свойств ПАВ. Числа ГЛБ определяются экспериментально.
Работами Дэвиса установлена количественная зависимость ГЛБ от состава и структуры ПАВ. Каждая структурная единица вносит свой вклад в число ГЛБ.
Числа ГЛБ по Гриффину составляют:
• для гидрофильных групп: –COOK–21,1; –COONa–19,1; –СООН–2,4;
–ОН–1,9; =О–1,3;
• для гидрофобных: =СH–;–СН2–; –СН3; =С=С – 0,475.
На основании этих данных числа ГЛБ можно рассчитывать по уравнению:
ГЛБ 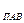 = 7 +
= 7 + 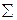 (ГЛБ)Г –
(ГЛБ)Г – 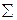 (ГЛБ)Л,
(ГЛБ)Л,
где 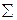 (ГЛБ)Г – сумма чисел ГЛБ всех гидрофильных групп;
(ГЛБ)Г – сумма чисел ГЛБ всех гидрофильных групп; 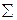 (ГЛБ)Л – сумма чисел ГЛБ липофильных (гидрофобных) групп.
(ГЛБ)Л – сумма чисел ГЛБ липофильных (гидрофобных) групп.
Физический смысл эмпирических чисел ГЛБ состоит в том, что они определяют отношение работы адсорбции молекул ПАВ на границе раздела фазы «масло» к работе адсорбции на той же границе с фазой «вода». В зависимости от числа ГЛБ ПАВ используются для той или иной цели. Так, если ПАВимеют числа ГЛБ от 7 до 9, их используют в качестве смачивателей, от 13 до 15 – в качестве моющих средств, от 15до 16 – в качестве солюбилизаторов в водных растворах.
СПОСОБНОСТЬ
К САМОПРОИЗВОЛЬНОМУ
МИЦЕЛЛООБРАЗОВАНИЮ
Критическая концентрация мицеллообразования ККМлежит обычно в
пределах 10  –10
–10 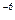 моль/дм
моль/дм 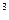 . После достижения этой концентраций в растворе самопроизвольно образуются сферические мицеллы (мицеллы Гартли) и система становится гетерогенной. Состояние коллоидного ПАВ после достижения ККМ можно записать так (без учета гидролиза соли):
. После достижения этой концентраций в растворе самопроизвольно образуются сферические мицеллы (мицеллы Гартли) и система становится гетерогенной. Состояние коллоидного ПАВ после достижения ККМ можно записать так (без учета гидролиза соли):
nRCOОNa  nRCOО
nRCOО 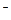 +nNa+
+nNa+ 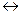 (RСОО
(RСОО  )n+ nNa+
)n+ nNa+
Истинный раствор Лиофильный коллоидный
раствор
Мицелла лиофилъного золя – это ассоциат дифильных молекул, лиофилъные группы которых обращены к растворителю, а лиофобные группы соединяются друг с другом, образуя ядро.
На рис. 12.3 схематически изображена мицелла Гартли. Такая ориентация дифильных молекул в мицелле обеспечивает минимальное поверхностное натяжение на границе «мицелла – дисперсионная среда».
Возникает вопрос – почему образование мицелл происходит самопроизвольно, ведь известно, что образование новой фазы всегда требует затраты энергий.
 Поскольку поверхностное натяжение на границе с дисперсионной средой минимально, энергия, затрачиваемая на образование мицеллы, невелика. Эта энергия с избытком компенсируется выигрышем энергии за счет выведения углеводородных хвостов молекул ПАВ в ядро мицеллы, которое, по сути дела, представляет собой жидкий углеводород, образовавшийся в результате плотной упаковки углеводородных цепей. Этот выигрыш составляет 1,08 kT (k – постоянная Больцмана, Т – тем–пература), т. е. при Т = 298 К величину, равную 2,6 кДж на Рис. 12.3
Поскольку поверхностное натяжение на границе с дисперсионной средой минимально, энергия, затрачиваемая на образование мицеллы, невелика. Эта энергия с избытком компенсируется выигрышем энергии за счет выведения углеводородных хвостов молекул ПАВ в ядро мицеллы, которое, по сути дела, представляет собой жидкий углеводород, образовавшийся в результате плотной упаковки углеводородных цепей. Этот выигрыш составляет 1,08 kT (k – постоянная Больцмана, Т – тем–пература), т. е. при Т = 298 К величину, равную 2,6 кДж на Рис. 12.3
каждую –СН2 – группу. Таким образом, мицеллообразование Мицелла Гартли сопровождается уменьшением свободной энергии системы.
Диаметр мицеллы Гартли равен удвоенной длине молекулы ПАВ.
Число молекул ПАВ, составляющих мицеллу, называется числом ассоциации п. Это число быстро растет в узком интервале концентраций ПАВобычно от 20 до 100 (иногда и более).
Для ионогенных ПАВ п увеличивается при понижении температуры и добавлении электролитов.
Для неионогенных ПАВ повышение температуры приводит к увеличению n, а введение электролитов на число ассоциации не влияет.
Сумма молекулярных масс всех молекул в мицелле называется мицеллярной массой.
При достижении определенной концентрации сферические мицеллы начинают взаимодействовать между собой, что приводит к их деформации. Мицеллы стремятся принять цилиндрическую, дискообразную, палочкообразную, пластинчатую формы. Такие мицеллы называются мицеллами Мак–Бена.
При концентрациях, в 10–50 раз больших ККМ, мицеллы принимают цепочечную ориентацию и вместе с молекулами растворителя образуют жидкокристаллическую структуру.
При дальнейшем увеличении концентрации ПАВ жидкокристаллическая структура переходит в гелеобразную, а затем в твердокристаллическую.
В растворах ПАВ количество вещества в мицеллярной форме может во много раз превышать его количество в молекулярном состоянии. Эти формы находятся в равновесии, состояние которого зависит от концентрации:
Молекулярный раствор  Мицеллы Гартли
Мицеллы Гартли  Дискообразные
Дискообразные 
 Цилиндрические
Цилиндрические Пластинчатые
Пластинчатые 
 Мицеллы Мак-Вена
Мицеллы Мак-Вена
 Жидкокристаллическая структура
Жидкокристаллическая структура 
 Гелеобразная структура
Гелеобразная структура  Твердое кристаллическое ПАВ
Твердое кристаллическое ПАВ
СОЛЮБИЛИЗАЦИЯ
Солюбилизациейназывается явление растворения веществ в мицеллах ПАВ.Солюбилизация —самопроизвольный и обратимый процесс.
В водных мицеллярных системах солюбилизируются вещества, не растворимые в воде, например, бензол, органические красители, жиры. Это обусловлено тем, что ядро мицеллы проявляет свойства неполярной жидкости.
Солюбилизат – вещество, солюбилизированное раствором ПАВ.
Солюбилизатор – ПАВ, которое солюбилизирует неполярную жидкость.
Мольная солюбилизация (Sm) – количество солюбилизатора, отнесенное к 1 молю мицеллярного ПАВ.
Способ включения молекул солюбилизата в мицеллы в водных растворах зависит от природы вещества.
Неполярные углеводороды внедряются в мицеллы, располагаясь в углеводородных ядрах мицелл.
Полярные органические вещества (спирты, амины, кислоты) встраиваются в мицеллу между молекулами ПАВ так, чтобы их полярные группы были обращены к воде, а липофильные части молекул ориентированы параллельно углеводородным радикалам ПАВ.
Для неионогенных ПАВ характерен и третий способ включения солюбилизата в мицеллы: молекулы солюбилизата, например, фенола, не проникают внутрь мицеллы, а закрепляются на их поверхности, располагаясь между беспорядочно изогнутыми полиоксиэтиленовыми цепями.
При солюбилизации неполярных углеводородов в ядрах мицелл углеводородные цепи раздвигаются, в результате размер мицелл увеличивается. Способность коллоидных ПАВ солюбилизировать углеводороды возрастает с ростом концентрации ПАВ. Солюбилизация в водных растворах ПАВ обычно увеличивается с повышением гидрофобности ПАВ и гидрофильности солюби-лизата.
Явление солюбилизации находит широкое применение в различных процессах, связанных с использованием ПАВ, отметим некоторые из них:
• эмульсионная коагуляция;
• изготовление эмульсионных смазочных жидкостей;
• изготовление фармацевтических препаратов;
• изготовление пищевых продуктов. Солюбилизация является важнейшим фактором моющего действия ПАВ. Она также входит, как одно из звеньев процесса обмена веществ, в жизнедеятельность живых организмов.
