Емісійний спектральний аналіз
Емісійний спектральний аналіз – це фізичний метод визначення хімічного складу речовини за її спектром, який емітують збуджені атоми і молекули. Атоми і молекули можуть збуджуватися полум’ям пальника, електричною дугою або іскрою. Атоми досліджуваної речовини випромінюють світло під дією високої температури, яка досягає 2000-3000°C в полум’ї пальника, 3000-7000°C – в електричній дузі і декілька тисяч градусів в іскрі.
Отримане таким способом випромінювання розкладається в спектр – впорядковане за довжинами хвиль випромінювання за допомогою призми або дифракційної гратки спектрального приладу і реєструється фотоелектричним пристроєм.
Емісійні спектри бувають лінійчасті, смугасті та безперервні. Лінійчасті спектри емітують атоми та йони розжарених газів та парів. Смугасті спектри виникають при випромінюванні світла розжареною парою молекул. Суцільні спектри емітують розжарені рідини та тверді тіла.
Оптичний спектр знаходиться в ультрафіолетовій, видимій і інфрачервоній зонах. Довжини хвиль спектральних ліній виражають у нанометрах. Так, наприклад, одна з жовтих ліній атома Натрію має довжину хвилі λ=589,59нм.
Спектральний аналіз широко застосовується у фізиці, астрономії, металургії, хімії, геології, біології, медицині та ін.
Емісійний спектральний аналіз відзначається високою чутливістю визначення, швидкістю проведення дослідження (кілька хвилин), об’єктивністю, універсальністю.
Особливий інтерес представляє полум’яна фотометрія, заснована на безпосередньому вимірюванні випромінювання введеного у полум’я розчину. Полум’яна фотометрія особливо корисна для визначення лужних та лужноземельних металів. Інтенсивність свічення пропорційна концентрації елемента, який визначається. Сторонні елементи сильно впливають на збудження атомів та інтенсивність їх ліній у спектрі.
Спектральний аналіз був відкритий у 1860 р. К. Кірхгофом і Р. Бунзеном. Теорія спектрів створила основу для сучасної теорії будови атома.
Спектроскопія тісно пов’язана з теорією будови атомів та теорією хімічного зв’язку. Внаслідок складності енергетичної системи електронів у важких атомах на основі квантової хімії неможливо надійно розрахувати енергію йонізації й інші характеристики. Зазвичай, такі характеристики розраховуються на основі спектральних властивостей атомів або молекул.
У практиці спектрального аналізу важливо знати залежність між будовою атома та його спектром, оскільки з цим пов’язано вплив температури полум’я, а також вплив інших елементів на інтенсивність лінії компонента, який визначається, та ін. Важливе значення мають резонансні лінії, що відповідають переходу електрона з нормального рівня (n=1) на найближчий рівень (n=2). Ці лінії відповідають першому ступеню збудження „холодного” атома. Через низький потенціал йонізації лужних та лужноземельних металів їх резонансні лінії легко збуджуються навіть при порівняно низькій температурі газового пальника. Наявність резонансних ліній допомогло відкриттю спектрального аналізу. В той же час, це є основою одного із сучасних методів емісійного спектрального аналізу – методу полум’яної фотометрії.
З іншого боку, резонансні лінії мають недоліки. Відомо, що при нагріванні атом переходить у збуджений стан, тобто електрони при цьому переходять на рівні з більш високим квантовим числом. У більш холодних частинах полум’я збуджені атоми переходять у стан з нижчим рівнем енергії. Незбуджені атоми в холодних частинах полум’я можуть безпосередньо поглинати випромінювання, якщо воно відповідає енергетичним характеристикам цих атомів. „Холодний” атом буде особливо легко поглинати саме резонансні лінії, збуджені іншими атомами даного елемента в зонах з більш високою температурою. Дійсно, у „холодних” атомів їх електрони знаходяться на нижньому рівні (n=1) і, поглинаючи відповідний квант енергії, електрон може перейти на найближчий рівень (n=2).
На явищі поглинання резонансних ліній ґрунтується один із сучасних методів кількісного спектрального аналізу – атомно-абсорбційна спектроскопія.
Для визначення складу досліджуваної проби за характерними лініями застосовують якісний спектральний аналіз, який базується на вивченні спектрів емісії.
Для повного аналізу достатньо помістити між електродами 0,1-1мг досліджуваної проби, створити електричну дугу і зафіксувати спектр. Спектр елемента може бути дуже складним, але для виявлення цього елемента в пробі достатньо виявити декілька ліній.
Перевагою спектрального аналізу є можливість за спектром невеликої проби речовини встановити наявність, а інколи і наближений вміст багатьох елементів. Якщо відомо основний склад проби і необхідно лише встановити наявність домішок, то під спектром досліджуваної речовини знімають спектр чистого зразка, що не містить домішок. Це значно полегшує розшифровку спектра, оскільки достатньо ідентифікувати лише ті лінії, які не повторилися у спектрі досліджуваної речовини. Інколи під спектром досліджуваної речовини знімають спектр шуканої домішки.
Абсолютна чутливість спектрального визначення деяких матеріалів складає 10–6-10–8г.
Для якісного спектрального аналізу використовують самі чутливі лінії з малими потенціалами йонізації, так звані останні лінії. Це ті лінії, які при зменшенні вмісту елемента, який визначається, в пробі зникають в останню чергу. Вибір спектрального приладу визначається областю, де розташовані найбільш чутливі лінії досліджуваного елемента, а також дисперсією приладу, тобто його здатністю розділяти близько розташовані лінії.
Для розшифровки спектрів використовують таблиці спектральних ліній та атласи.
В основі кількісного спектрального аналізу лежить залежність між інтенсивністю ліній кожного елемента і концентрацією цього елемента у пробі:
I = a·cb,
де I – інтенсивність спектральної лінії;
c – концентрація елемента в пробі;
a і b – постійні, які залежать від швидкості надходження даного елемента з проби у хмару розряду, умов збудження та самопоглинання спектральних ліній.
Умови збудження можуть змінюватися у кожному новому досліді через коливання напруги електричної мережі, через зміну відстані між електродами, між якими виникає електрична дуга, або різного стану поверхні електродів та ін. Тому вимірювання абсолютної інтенсивності ліній, як правило, не може бути використано для кількісного аналізу. У більшості випадків вимірюють відносну інтенсивність спектральних ліній досліджуваного елемента І1 і елемента порівняння І2. Елементом порівняння може бути елемент проби або спеціально введений елемент. Розрахунок проводиться за формулою:
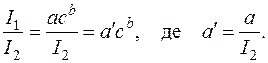
У спектральному аналізі особливі вимоги ставляться до спектральних ліній. Абсолютною чутливістю називають найменшу концентрацію елемента, яка може бути виявленою за даною спектральною лінією. Проте, лінії, що характеризуються високою чутливістю, не завжди придатні для кількісного аналізу. Найбільш чутливими є резонансні лінії, які відповідають переходу електрона з нормального у найближчий збуджений стан. Такі лінії легко збуджуються у будь-якому полум’ї, але вони легко і самообертаються: випромінювання даної довжини хвилі поглинаються атомами того ж елемента в холодних частинах полум’я. тому для них не існує пропорційності між їх інтенсивністю та вмістом елемента в пробі.
Інші лінії залежать від випадкових коливань умов розряду. При визначенні домішок необхідно вибирати такі лінії, на які не накладалися б лінії основного матеріалу, а також інших елементів, що знаходяться в пробі.
Як лінію порівняння для визначення домішок часто беруть слабку лінію основного матеріалу. Інколи буває доцільно ввести в досліджуваний матеріал точну кількість іншого елемента, який не міститься у цих матеріалах. Лінії введеного елемента використовують як лінії порівняння. Лінію порівняння вибирають таким чином, щоб під впливом різних умов розряду інтенсивність її змінювалася приблизно так же, як інтенсивність ліній елемента, що визначається.
Як вже зазначалось, полум’яна фотометрія є частиною емісійного спектрального аналізу. Цей метод базується на термічному збудженні атомів у полум’ї і прямому вимірюванні інтенсивності випромінювання за допомогою фотоелемента або фотопомножувача. Для виділення випромінювання з певною довжиною хвилі використовують монохроматори або відповідні світлофільтри. Температура полум’я, яке використовується в полум'яній фотометрії, невелика і залежить від того, які гази застосовують для цього. При горінні у повітрі ацетилену досягається температура 2100-2400°C, водню – 2000-2100°C, пропану – 1300-2000°C, бутану – 1300-1900°C.
Полум’янофотометричне визначення Натрію і Калію проводиться за лініями Na589,0 та 589,6 і К765,5 та 769,9 нм. Для виділення випромінювання цих ліній використовують світлофільтри з вузькою смугою пропускання при довжині хвилі лінії, яка випромінює. Ці світлофільтри пропускають випромінювання одного елемента і затримують випромінювання інших елементів.
Розчин, що аналізується, розпиляється потоком повітря у розпилювачі типу пульверизатора. Краплини розчину осідають на стінках камери розпилювача і стікають у відстійник, а утворений аерозоль досліджуваного розчину подається у змішувач, де змішується з горючим газам. Потім суміш подається на пальник.
Випромінювання полум’я збирається лінзою і сферичним дзеркалом, подається через діафрагму і світлофільтр на фотоелемент. Сила фотоструму вимірюється гальванометром.
