Классификация коллоидных пав
Эту классификацию можно представить следующей схемой (см. рис. 12.1).
Анионные ПАВ – ПАВ, которые диссоциируют в воде с образованием поверхностно–активного аниона.
Анионные ПАВ составляют большую часть мирового производства всех ПАВ. К ним относятся:
а) карбоновые кислоты (RCOOH) и их соли (мыла) (RCOOM, где М –
металл); например, C 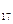 H33COONa – олеат натрия; C
H33COONa – олеат натрия; C 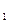
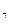 H35COONa –
H35COONa –
стеарат натрия; C15H3ICOONa – пальмитат натрия;
б) алкилсульфаты ROSO2OM;
в) алкиларилсульфонаты RArSO2OM;
г) вещества, содержащие другие типы поверхностно-активных анионов, например фосфаты, тиосульфаты. В качестве ПАВ широкое практическое применение получили соли синтетических жирных кислот фракции C 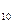 –C
–C 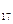 заменяющие кислоты растительного и животного происхождения. Используют соли жирных кислот с различными катионами: с двух– и трехзарядными катионами применяют в углеводородных средах, с однозарядными катионами – в водных средах.
заменяющие кислоты растительного и животного происхождения. Используют соли жирных кислот с различными катионами: с двух– и трехзарядными катионами применяют в углеводородных средах, с однозарядными катионами – в водных средах.
В кислых средах соли карбоновых кислот переходят в слабодиссоциированные и малорастворимые кислоты, а в присутствии некоторых катионов (кальция, магния) образуют нерастворимые соли, что резко снижает эффективность их действия как ПАВ, особенно ухудшает их моющее действие. Большими преимуществами в этом отношении обладают алкилсульфаты и алкилсулъфонаты, которые являются солями сильных кислот и поэтому мо –
стеарат натрия; C15H3ICOONa – пальмитат натрия;
б) алкилсульфаты ROSO2OM;
в) алкиларилсульфонаты RArSO2OM;
г) вещества, содержащие другие типы поверхностно–активных анионов, например фосфаты, тиосульфаты. В качестве ПАВ широкое практическое применение
получили соли синтетических жирных кислот фракции C10–C 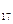 , заменяющие кислоты растительного и животного происхождения. Используют соли жирных кислот с различными катионами: с двух– и трехзарядными катио–нами применяют в углеводородных средах, с однозарядными катионами – в водных средах.
, заменяющие кислоты растительного и животного происхождения. Используют соли жирных кислот с различными катионами: с двух– и трехзарядными катио–нами применяют в углеводородных средах, с однозарядными катионами – в водных средах.
В кислых средах соли карбоновых кислот переходят в слабодиссоциированные и малорастворимые кислоты, а в присутствии некоторых катионов (кальция, магния) образуют нерастворимые соли, что резко снижает эффективность их действия как ПАВ, особенно ухудшает их моющее действие. Большими преимуществами в этом отношении обладают алкилсульфаты и алкилсулъфонаты, которые являются солями сильных кислот и поэтому могут
|

Рис. 12.1
Классификация коллоидных растворов
быть использованы в кислых и солевых растворах. Здесь уместно вспомнить о стиральных порошках, пригодных для стирки в жесткой и морской воде.
Катионные ПАВ – это ПАВ, которые в водном растворе диссоциируют с образованием поверхностно-активного катиона,
К катионным ПАВ относятся:
а) соли первичных, вторичных и третичных алифатических и
ароматических аминов;
б) соли алкилзамещенных аммониевых оснований: [(CH3)2NR 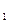 R2]+Cl
R2]+Cl  ;
;
в) пиридиновые соединения.
Катионные ПАВ наиболее токсичны и наименее биологически разлагаемые из всех ПАВ. Их часто используют в качестве бактерицидных, фунгицидных, дезинфицирующих веществ, ингибиторов коррозии.
Амфолитные ПАВ – это ПАВ, содержащие две функциональные группы, одна из которых имеет кислотный характер, а другая основной. В зависимости от среды такое соединение может диссоциировать и как кислота, и как основание. Например, аминокислоты;
+ОН 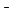 +Н+
+Н+
RNH(CH2)nCOO 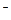
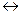 RNH(CH2)nCOOH
RNH(CH2)nCOOH 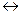 RNH2(CH2+)n.COOH
RNH2(CH2+)n.COOH
Анионоактивпые Катионоактивные
свойства свойства

 Неионогенные ПАВ – ПАВ, которые, в растворах не распадаются на ионы, это соединения, полученные на основе окиси этилена СН2 – СН2 путем
Неионогенные ПАВ – ПАВ, которые, в растворах не распадаются на ионы, это соединения, полученные на основе окиси этилена СН2 – СН2 путем
О
присоединения 

 ее к спиртам, карбоновым кислотам, аминам и др.
ее к спиртам, карбоновым кислотам, аминам и др.
Например, RОH + nСН2 – СН2  RО(ОСН2СН2) n Н
RО(ОСН2СН2) n Н
Полиоксиэтиленоная
цепочка
 В молекулах неионогенных ПАВ углеводородный радикал может содержать от 6 до 18 углеродных атомов, а n может изменяться от нескольких единиц до 100. Неионогенные ПАВ являются смесью гомологов с различной длиной полиоксиэтиленовой цепи. Полиоксиэтиленовая цепь определяет гидрофильные свойства неионогенных ПАВ.
В молекулах неионогенных ПАВ углеводородный радикал может содержать от 6 до 18 углеродных атомов, а n может изменяться от нескольких единиц до 100. Неионогенные ПАВ являются смесью гомологов с различной длиной полиоксиэтиленовой цепи. Полиоксиэтиленовая цепь определяет гидрофильные свойства неионогенных ПАВ.
