Салициловая кислота. натрия салицилат
Салициловая кислота (о-гидроксибензойная кислота) встречается в растительном мире как в свободном, так и в связанном виде во многих эфирных маслах. Салициловая кислота обладает антисептическими свойствами и находит применение как в медицине, так и в пищевой промышленности в качестве консерванта. Более широкое применение в медицине нашли производные салициловой кислоты.
Строение и свойства
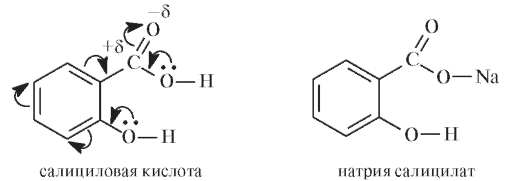
Салициловая кислота о-HOC6H4COOH представляет собой кристаллическое вещество, малорастворимое в воде. По кислотности pKa = 2,98 превосходит бензойную кислоту, нейтрализуется щелочами с образованием моно- и дизамещенных солей. Кислотные свойства обусловливают способность салициловой кислоты, в частности, вступать в реакции с кислотами Льюиса - солями тяжелых металлов (FeCl3, CuSO4, AgNO3).
Получение
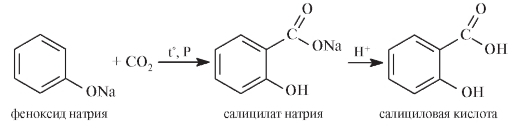
В промышленности салициловую кислоту получают карбоксилированием фенола. При действии диоксида углерода на твердые феноксиды щелочных металлов образуется фенолокислота:
Механизмы действия и биотрансформация
Действие салициловой кислоты аналогично бензойной кислоте (см. выше).
Основными путями биотрансформации салициловой кислоты и ее производных является конъюгация с аминокислотами, например, конъюгат с глицином - салицилуровая кислота:
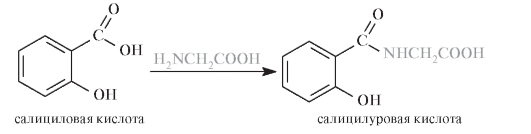
У человека до 75% дозы салициловой кислоты выводится в виде конъюгата с глицином.
Натрия салицилат относится к группе НПВС. Оказывает аналгезирующее, жаропонижающее и противовоспалительное действие, неизбирательно угнетает ЦОГ1 и ЦОГ2, снижает синтез Pg. Обезболивающий эффект обусловлен как центральным, так и периферическим действием. Воздействует на центр терморегуляции, снижает температуру тела при лихорадочных состояниях.
Контроль качества
Определение подлинности.Подлинность салициловой кислоты и натрия салицилата устанавливают ИК-спектрометрией, а также качественными реакциями на салицилат-ион и ион натрия.
Качественной реакцией на салицилат-ион является рН-зависимая реакция с железа (Ш) хлоридом. При рН 2,0-3,0 образуется окрашенный в фиолетовый цвет моносалицилатный комплекс. При рН 3,0-8,0 образуется дисалицилат красного цвета, при рН 8,0-10,0 - трисалицилат желтого цвета.
Субстанцию салициловой кислоты массой 30 мг растворяют в 5 мл 0,05 моль/л растворе NaOH и доводят объем раствора до 20 мл водой. С реактивом FeCl3 образуется фиолетово-красное окрашивание раствора:
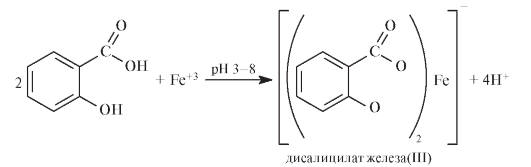
Прибавление к смеси HCl приводит к обесцвечиванию раствора и образованию осадка салициловой кислоты:
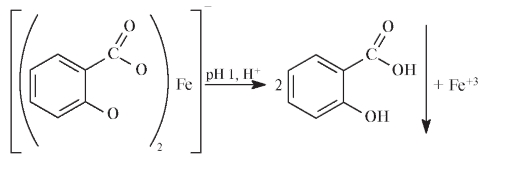
Разрушение комплексного иона объясняется протонированием кислотных групп в средах с рН <1.
Реакция с меди(II) сульфатом сопровождается образованием комплексных ионов, окрашенных в зеленый цвет. Салициловая кислота выступает в роли бидентантного иона, образуя с иономкомплексообразователем Cu+2 комплекс с координационным числом, равным 4:
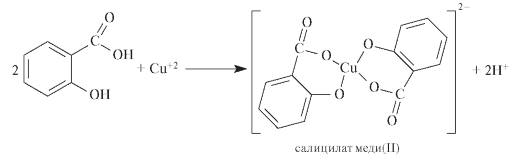
Натрия салицилат идентифицируют аналогично соли бензойной кислоты (см. выше).
Испытания на чистоту.Допустимыми примесями в фармацевтических субстанциях салициловой кислоты и натрия салицилата являются: хлориды (не более 100 мкг/г), сульфаты (в сравнении с эталонным раствором), тяжелые металлы (не более 20 мкг/г), сульфатная зола (не более 0,1%), потеря в массе при высушивании не должна превышать 0,5%.
В субстанциях ЛВ могут обнаруживаться родственные примеси:
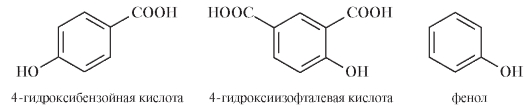
Примеси родственных веществ определяют методом жидкостной хроматографии с УФ-детекцией при 270 нм. Пики на хроматограммах, обнаруживаемые для испытуемого раствора, не должны быть больше пиков стандартных образцов (0,1% для 4-гидроксибензойной кислоты, 0,05% для 4-гидроксиизофталевой кислоты и 0,02% для фенола).
Количественное определение.Количественное определение салициловой кислоты проводят методом алкалиметрии. Для этого 0,120 г ЛВ растворяют в 30 мл спирта, прибавляют 20 мл воды и
титруют 0,1 моль/л раствором NaOH с индикатором феноловым красным. Окраска индикатора изменится в момент нейтрализации карбоксильной группы.
1 мл 0,1 моль/л раствора NaOH соответствует 13,81 мг C7H3O3.
При неправильном подборе кислотно-основного индикатора, например фенолфталеина, окраска индикатора засвидетельствует нейтрализацию не только карбоксильной, но и фенольной группы, объем щелочи израсходуется в два раза больше и результат будет завышенным.
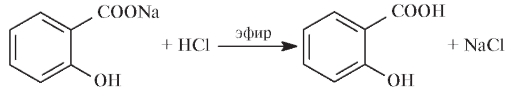
Натрия салицилат количественно определяют ацидиметрическим методом в присутствии эфира, в который экстрагируется выделяющаяся салициловая кислота.
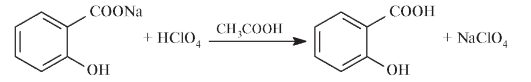
Фармакопейным методом определения натрия салицилата является также кислотно-основное титрование в среде ледяной уксусной кислоты 0,1 моль/л раствором HClO4:
1 мл 0,1 моль/л раствора HClO4 соответствует 16,010 мг
C7H5NaO3.
Ацетилсалициловая кислота
Ацетилсалициловая кислота - первое синтетическое лекарственное вещество и долгожитель в мире лекарственных препаратов, применяется в медицине с 1899 г.
Родоначальницу ацетилсалициловой кислоты - салициловая кислота - использовали как целебное средство со времен Гиппократа. Отвар коры ивы, содержащий салициловую кислоту (лат. salix - ива), применяли как жаропонижающее, обезболивающее и противовоспалительное средство.
Ацетилсалициловая кислота гидролизуется с образованием салициловой кислоты, поэтому их терапевтические свойства схожи. Новое ЛС было открыто и запатентовано немецкой фирмой «Bayer». В 1899 г. фирма «Bayer» запатентовала торговую марку «Аспирин». Название было дано, как полагают, в честь святого Аспиринуса - покровителя страдающих головной болью.
Строение и свойства
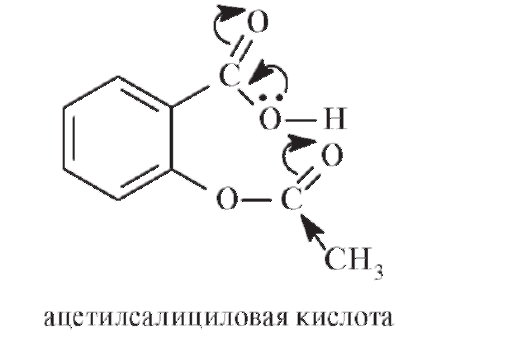
Ацетилсалициловая кислота - ацетилированное производное салициловой кислоты. Для нее характерны реакции кислотноосновного характера, солеобразование, обусловленные свободной карбоксильной группой, а также гидролиз по ацетилированной группе.
Получение
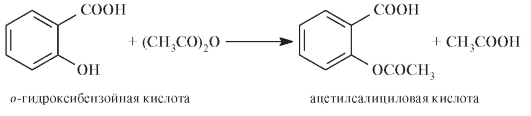
Ацетилсалициловую кислоту получают ацетилированием фенолокислоты уксусным ангидридом: