Карбонові кислоти. оцтова кислота
Карбоновими кислотами називаються органічні речовини, молекули яких містять одну або кілька карбоксильних груп 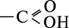 ( або - СООН), сполучених з вуглеводневим радикалом.
( або - СООН), сполучених з вуглеводневим радикалом.
Карбонові кислоти з однією карбоксильною групою називають одноосновними. Насичені одноосновні карбонові кислоти мають загальну формулу СnH2n + 1COOH. За систематичною номенклатурою, назву кислот утворюють із назв відповідних насичених вуглеводнів, додаючи до них суфікс і закінчення -ова і слово кислота.
НСООН метанова (мурашина) кислота
СН3СООН етанова (оцтова) кислота
СН3СН2СООН пропанова (пропіонова) кислота
СН3СН2СН2СООН бутанова (масляна) кислота
Найважливішим представником насичених одноосновних кислот є оцтова кислота.
Структурна формула: 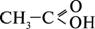
Електронна формула: 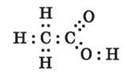
Зв’язок C - H — ковалентний слабко-полярний.
Зв’язки C = O і O - H — ковалентні сильно-полярні.
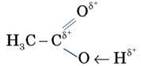
У результаті зсуву електронної густини подвійного зв’язку до Оксигену атом Карбону одержує надлишковий позитивний заряд. через це електронна густина в гідроксильній групі значною мірою зміщена до атома Оксигену. Атом Гідрогену у зв’язку з цим легко відщеплюється у вигляді протона, зумовлюючи кислотні властивості.
Фізичні властивості. Молекула оцтової кислоти полярна, тому між молекулами утворюються водневі зв’язки з утворенням димерів.
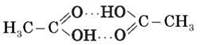
Оцтова кислота — це безбарвна рідина з різким запахом, температури кипіння й плавлення низькі (температура плавлення — 16,6 °С, температура кипіння — 118,1 °С, густина — 1,049 г/см3), добре розчинна у воді (розчин оцтової кислоти у воді називається оцтом).
Хімічні властивості. Оцтова кислота проявляє всі хімічні властивості, притаманні кислотам:
1) електролітична дисоціація. У розчині частина молекул оцтової кислоти дисоціює з утворенням катіону Гідрогену Н+ та аніону кислотного залишку ацетату СН3СОО-
СН3СООН ↔ СН3СОО- + Н+
ацетат -йон
Утворені йони Н+ діють на індикатори, змінюючи їх колір: лакмусу – на червоний, метилоранжу – на рожевий, фенолфталеїн залишається безбарвним. Але необхідно враховувати, що оцтова кислота, як і більшість органічних кислот, належить до слабких кислот і дисоціює тільки невелика кількість її молекул. Тому при складанні рівнянь у йонній формі хімічну формулу оцтової кислоти як слабкого електроліту доцільно зберігати у молекулярному, недисоційованому вигляді.
2) взаємодія з металами. Оцтова кислота взаємодіє з металами, що розташовані у ряду активності металів перед воднем:
2 CH3COOH + Ca → (CH3COO)2Ca + H2 ↑
кальцій ацетат
2 CH3COOH + Ca → 2CH3COO- + Ca 2+ + H2 ↑
3) взаємодія з основними оксидами:
2 CH3COOH + FeO → (CH3COO)2Fe + H2O
ферум (ІІ) ацетат
2 CH3COOH + FeO → 2CH3COO- + Fe 2+ + H2O
4) взаємодія з основами:
CH3COOH + NaOH → CH3COONa + H2O
натрій ацетат
CH3COOH + Na+ + OH- → CH3COO- + Na+ + H2O
CH3COOH + OH- → CH3COO- + H2O
3 CH3COOH + Fe(OH)3 → (CH3COO)3Fe + 3 H2O
ферум (ІІІ) ацетат
3 CH3COOH + Fe(OH)3 → 3 CH3COO- + Fe3+ + 3 H2O
5) взаємодія з солями:
2 CH3COOH + Na2СО3 → 2 CH3COONa + H2O + СО2 ↑
2 CH3COOH + 2Na+ + СО32- → 2 CH3COO- + 2Na+ + H2O + СО2 ↑
2 CH3COOH + СО32- → 2 CH3COO- + H2O + СО2 ↑
6) взаємодія зі спиртами (реакція етерифікації) : при нагріванні суміші карбонової кислоти зі спиртом у присутності концентрованої сульфатної кислоти відбувається утворення естерів (складних ефірів) :
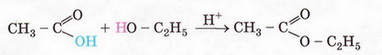 + Н2О
+ Н2О
етилацетат
(етиловий естер оцтової кислоти)
Застосування оцтової кислоти:
1) виробництво барвників;
2) розчинник;
3) харчова промисловість;
4) виробництво ацетатного волокна;
5) виробництво лікарських препаратів (аспірин та ін.).
Вищі карбонові кислоти
Вищими називають кислоти, що містять у молекулі велику кількість атомів Карбону. З вищих одноосновних карбонових кислот найбільше значення мають
С15Н31СООН пальмітинова ( пентадеканова) кислота
С17Н35СООН стеаринова (гептадеканова) кислота
Вони являють собою безбарвні тверді речовини, нерозчинні у воді.
Стеаринову й пальмітинову кислоти можна виділити з рослинних і тваринних жирів. У промисловості ці кислоти одержують шляхом окиснення парафіну, який виділяють із нафти.
Пальмітинова і стеаринова кислоти проявляють властивості, характерні для карбонових кислот, наприклад взаємодіють з лугами :
C17H35COOH + NaOH → C17H35COONa + H2O
натрій стеарат
Солі цих кислот – основні компоненти мила. Стеаринову й пальмітинову кислоти застосовують у виробництві мийних засобів, лаків, фарб, лінолеуму, гуми.
Важливим представником ненасичених карбонових кислот є олеїнова кислота С17Н33СООН.
СН3 – (СН2)7 – СН = СН – (СН2)7 – СООН
Олеїнова кислота – масляниста рідина, що у формі естерів гліцерину входить до складу рослинних жирів. Вона має властивості кислот, зумовлені наявністю карбоксильної групи:
С17Н33СООН + КОН → С17Н33СООК + Н2О
калій олеат
Також олеїнова кислота проявляє властивості ненасичених вуглеводнів, зумовлені наявністю подвійного зв’язку в карбоновому ланцюзі. Так, наприклад, олеїнова кислота знебарвлює бромну воду:
СН3 – (СН2)7 – СН = СН – (СН2)7 – СООН + Br2 →
→ СН3 – (СН2)7 – СН - СН – (СН2)7 – СООН
| |
Br Br
У результаті гідрування ненасичена олеїнова кислота перетворюється на насичену стеаринову кислоту:
С17Н33СООН + Н2 → С17Н35СООН
До вищих ненасичених карбонових кислот належать також лінолева С17Н31СООН та ліноленова С17Н29СООН кислоти.
Жири.
Жири– це естери трьохатомного спирту гліцеролу та вищих карбонових кислот. Загальна назва таких сполук — тригліцериди.
Склад і будову жирів можна зобразити загальною формулою естеру, в якому залишки карбонових кислот позначені радикалами R1, R2, R3:
CH2–O–CO–R1
|
CH–O–CO–R2
|
CH2–O–CO–R3.
Найчастіше до складу молекул жирів входять радикали таких вищих карбонових кислот: пальмітинової C15H31COOH, стеаринової C17H35COOH, олеїнової C17H33COOH.
CH2–O–CO– С17Н35
| тристеарат, естер гліцеролу та стеаринової
CH–O–CO– С17Н35 кислоти
|
CH2–O–CO– С17Н35
За походженням жири бувають:
1) рослинні (олії) ;
2) тваринні ;
3) комбіновані .
За консистенцією:
1) тверді (утворені насиченими вищими карбоновими кислотами) ;
2) рідкі ( утворені ненасиченими вищими карбоновими кислотами).
До складу природних жирів входять як правило вищі карбонові кислоти з парним числом атомів Карбону. Приклади природних жирів:
CH2–O–CO– С17Н33
| Вершкове масло: олео-пальміно-бутират
CH–O–CO– С17Н31
|
CH2–O–CO– С3Н7
CH2–O–CO– С17Н33
| Свиняче сало: олео-пальміно-стеарат
CH–O–CO– С17Н31
|
CH2–O–CO– С17Н35
Лляна олія: 61,5% гліцеридів лінолевої кислоти.
Соняшникова, горіхова олії: 30 – 50% гліцеридів лінолевої кислоти, решта – олеїнової кислоти.
Утворюються жири під час реакцій етерифікації за участі гліцеролу та вищих карбонових кислот:
CH2–OН CH2 – O – CO – C17H35
| |
CH–OН + 3 С17Н35СООН → CH – O – CO – C17H35 + 3 H2O
| |
CH2–OН CH2 – O – CO – C17H35
тристеарат
Хімічні властивості жирів
1) Гідроліз – розкладання жирів під дією води. Протікає в присутності каталізаторів (кислоти, луги, оксиди металів).
а) кислотний гідроліз: у присутності кислот гідроліз жирів призводить до утворення гліцеролу та відповідних карбонових кислот:
CH2 – O – CO – C17H35 CH2 – OH
| |
CH – O – CO – C17H35 + 3 H2O → CH – OH + 3 C17H35COOH
| |
CH2 – O – CO – C17H35 CH2 – OH
б) лужний гідроліз: у присутності лугів гідроліз жирів призводить до утворення гліцеролу та солей вищих карбонових кислот:
CH2 – O – CO – C17H35 CH2 – OH
| |
CH – O – CO – C17H35 + 3 NaOH → CH – OH + 3 C17H35COONa
| |
CH2 – O – CO – C17H35 CH2 – OH
Вищі солі карбонових кислот є основою мила. Натрієві солі (С17Н35СOONa , C15H31COONa) входять до складу твердого мила, а калієві солі ((С17Н35СOOК, C15H31COOК) входять до складу рідкого мила.
2) Гідрування ненасичених жирів. Жири, що утворені ненасиченими карбоновими кислотами ( рідкі жири) можуть прєднувати молекули водню і перетворюватись на насичені ( тверді) жири. Так. Наприклад рідкий жир три олеат при гідруванні перетворюється на твердий жир тристеарат:
CH2 – O – CO – C17H33 СН2 – О – СО – С17Н35
| |
CH – O – CO – C17H33 + 3 Н2 → CH - О – СО – С17Н35
| |
CH2 – O – CO – C17H33 CH2 – O – СО – С17Н35
триолеат тристеарат
Ця реакція має велике промислове значення. За її допомогою соняшникову олію перетворюють на твердий жир маргарин, що є замінником природних твердих жирів тваринного походження.
Біологічна роль жирів. Жири є найважливішими продуктами харчування. В організмі людини основна функція жиру – бути джерелом енергії. Окиснення 1г жиру спричиняє виділенню 39 кДж енергії. Однак буде нерозумним, виходячи з цього, прагнути забезпечити свій організм виключно жирами, оскільки, незважаючи на те, що вони багаті на енергію, жири важко засвоюються. Добовий раціон людини має містити 60 – 70г жиру. Але не можна забувати, що надлишкова кількість жиру, навіть у раціоні здорової людини, дуже шкідлива. Жири не розчиняються ані водою, ані травними соками. В організмі вони розщеплюються й емульгуються за сприяння жовчі. Зайва кількість жиру не встигає проемульгуватися, порушує травні процеси та спричиняє неприємне відчуття печії. Жири є не тільки джерелом енергії в організмі, а й джерелом води. Завдяки цій воді живуть верблюди тривалий час без свіжої води. Для розвитку зародка курчати в інкубаційний період потрібна вода, а надходження її ззовні відсутнє. Зародок забезпечується водою окисленого жиру. Жири необхідні й мешканцям холодного клімату: тюленям, моржам. Підшкірний жир допомагає зберегти внутрішнє тепло. Будь – якій тварині жирові відкладення пом’якшують силу різних поштовхів і ударів. Крім того, жири для тварин – мастильний матеріал. Відомо, водоплавні птахи самі проводять змащення під час чищення пір’я.
Також жири є джерелом вітамінів A, D, E.
Застосування жирів.
1) харчова промисловість;
2) маргарин;
3) у домашніх умовах;
4) мило;
5) гліцерин;
6) медицина;
7) оліфа;
8) косметичні засоби.
Вуглеводи.
Вуглеводи – найважливіші природні сполуки, що характеризуються біологічною активністю, відіграють важливу роль у житті рослин, тварин, людини.
Свою назву одержали через початкові уявлення про склад вуглеводів як сполук Карбону з водою: Cn(H2O)m.
Глюкоза: С6Н12О6 ↔ С6(Н2О)6
Сахароза: С12Н22О11 ↔ С12(Н2О)11
Назва «вуглеводи» збереглася дотепер, хоча й не виражає дійсної, досить складної будови цих речовин.
У рослинах міститься до 80% вуглеводів. В організмі людини й тварин – до 20%. Їжа людини на 70% складається з вуглеводів.
Утворюються вуглеводи у зелених рослинах під час процесу фотосинтезу:
6 СО2 + 6 Н2О → С6Н12О6 + 6 О2
глюкоза
12 СО2 + 11 Н2О → С12Н22О11 + 12 О2
сахароза
6n CO2 + 5n H2O → (C6H10O5)n + 6nO2
крохмаль
Класифікація вуглеводів. В основу класифікації вуглеводів покладено їх відношення до реакцій гідролізу.
Вуглеводи
________________________________|_________________________________
↓ ↓ ↓
Моносахариди Дисахариди Полісахариди
Моносахариди – це вуглеводи, що не вступають у реакцію гідролізу (глюкоза, фруктоза).
С6Н12О6 + Н2О 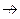
Дисахариди – це вуглеводи, молекула яких під час гідролізу розпадається на дві молекули моносахаридів:
С12Н22О11 + Н2О → С6Н12О6 + С6Н12О6
Полісахариди – це вуглеводи, молекула яких під час гідролізу розпадається на безліч молекул моносахаридів:
(С6Н10О5)n + nH2O → n C6H12O6
Глюкоза
Молекулярна формула - С6Н12О6.
Молекула глюкози містить п’ять гідроксидних груп – ОН та альдегідну групу – СН = О
Тобто за своїми функціями глюкоза є альдегідоспирт. Структурна формула глюкози має вигляд:
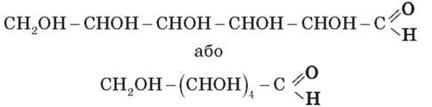
Як показали дослідження, у розчині глюкози є молекули лінійної й циклічної будови.
Фізичні властивості і поширення у природі.Глюкоза - білий кристалічний порошок, добре розчинний у воді. Температура плавлення близько 150ºС. Солодка на смак.
Глюкозудобув 1802 р. французький хімік Ж. Пруст з винограду, тому її дотепер часто називають виноградним цукром. У природі глюкоза трапляється не лише у виноградному соку, а й у соках багатьох інших фруктів і ягід та чи не в усіх органах зелених рослин. Бджолиний мед також містить глюкозу. Особливо багаті на глюкозу виноград, черешні, вишні, малина, суниці, сливи, кавуни. З овочів найбільше глюкози містить гарбуз, білоголовкова капуста та морква. Міститься глюкоза також у крові людини і тварин (близько 0,1%).
Хімічні властивості.
1) Окиснення:
С6Н12О6 + 6 О2 → 6 СО2 + 6 Н2О
У результаті окисненя глюкози в тканинах організму вивільняється енергія, необхідна для нормальної життєдіяльності організмів.
2) Взаємодія з купрум (ІІ) гідроксидом.
Як багатоатомний спирт глюкоза розчиняє свіжоотриманий Cu(OH)2 утворюючи яскраво-синій розчин.
3) Бродіння – розклад цукристих речовин під дією біологічно активних каталізаторів (ферментів).
Спиртове бродіння – відбувається під дією ферменту дріжджів:
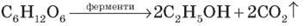
Молочнокисле бродіння – відбувається під дією молочнокислих бактерій:
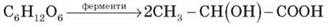
Застосування глюкози.
1) як цінний харчовий продукт;
2) в кондитерському виробництві;
3) у медицині для приготування лікарських препаратів, консервування крові, внутрішньовенного вливання;
4) у виробництві дзеркал та іграшок (сріблення);
5) під час фарбування та обробки тканин і шкір.
Сахароза
Фізичні властивості та поширення у природі.Найважливішою сполукою з дисахаридів є сахароза. Її молекулярна формула C12H22O11.
Сахароза– це безбарвна кристалічна речовина, солодка на смак ( солодша за глюкозу), добре розчиняється у воді. При нагріванні до 190–200 °С її кристали плавляться, утворюючи карамель.
У великих кількостях сахароза міститься у цукрових буряках, стеблах цукрової тростини, а також у березовому та кленовому соках, у багатьох плодах. У промисловості сахарозу виробляють із соку цукрової тростини (вміст 14 -16%), цукрового буряку (16 – 21%) та деяких інших рослин, наприклад, канадського клену, земляної груші.
Хімічні властивості.Найважливішою властивістю сахарози є гідроліз. Як дисахарид сахароза розпадається на дві молекули моносахаридів. Одна з таких молекул – молекула глюкози,інша – фруктози:
С12Н22О11 + Н2О → С6Н12О6 + С6Н12О6
глюкоза фруктоза
Ця хімічна реакція використовується для одержання штучного меду.
