Вопрос Закон Авогадро. Следствия из закона.
Закон Авогадро — В равных объемах различных газов при постоянных температуре и давлении содержится одинаковое число молекул.
Из Закона Авогадро выводится 2 следствия:
Следствие 1: Один моль любого газа при одинаковых условиях занимает одинаковый объем
В частности, при нормальных условиях (T=0 °C (273К) и p=101,3 кПа) объём 1 моля газа, равен 22,4 л. Этот объём называют молярным объёмом газа Vm. Пересчитать эту величину на другие температуру и давление можно с помощью уравнения Менделеева-Клапейрона


Из Уравнения Менделеева-Клапейрона выводятся еще 3 закона
1) Закон Шарля : 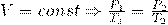
2) Закон Гей-Люссака : 
3) Закон Боля-Мариотта : 
Следствие 2: Отношение масс одинаковых объемов двух газов есть величина постоянная для данных газов
Эта постоянная величина называется относительной плотностью газов и обозначается D. Так как молярные объемы всех газов одинаковы (1-е следствие закона Авогадро), то отношение молярных масс любой пары газов также равна этой постоянной:

В Формуле мы использовали :
 — Относительная плотность газа
— Относительная плотность газа
 — Молярные массы
— Молярные массы
 — Давление
— Давление
 — Молярный объем
— Молярный объем
 — Масса
— Масса
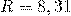 — Универсальная газовая постоянная
— Универсальная газовая постоянная
 — Абсолютная температу
— Абсолютная температу
Следствия закона
Первое следствие из закона Авогадро: один моль любого газа при одинаковых условиях занимаетодинаковый объём.
В частности, при нормальных условиях, т. е. при 0 °C (273К) и 101,3 кПа, объём 1 моля газа, равен 22,4 л. Этот объём называют молярным объёмом газа Vm. Пересчитать эту величину на другие температуру идавление можно с помощью уравнения Менделеева-Клапейрона:
 .
.
Второе следствие из закона Авогадро: молярная масса первого газа равна произведению молярной массывторого газа на относительную плотность первого газа по второму.
Положение это имело громадное значение для развития химии, так как оно дает возможность определятьчастичный вес[2] тел, способных переходить в газообразное или парообразное состояние. Если через m мыобозначим частичный вес тела, и через d — удельный вес[3] его в парообразном состоянии, то отношение m / d должно быть постоянным для всех тел. Опыт показал, что для всех изученных тел, переходящих в пар безразложения, эта постоянная равна 28,9, если при определении частичного веса исходить из удельного весавоздуха, принимаемого за единицу, но эта постоянная будет равняться 2, если принять за единицу удельныйвес водорода. Обозначив эту постоянную, или, что то же, общий всем парам и газам частичный объём черезС, мы из формулы имеем с другой стороны m = dC. Так как удельный вес пара определяется легко, то, подставляя значение d в формулу, выводится и неизвестный частичный вес данного тела.
Элементарный анализ, например, одного из полибутиленов указывает, в нём пайное отношение углерода кводороду, как 1 к 2, а потому частичный вес его может быть выражен формулой СН2 или C2H4, C4H8 и вообще(СН2)n. Частичный вес этого углеводорода тотчас определяется, следуя закону Авогадро, раз мы знаемудельный вес, т. е. плотность его пара; он определен Бутлеровым и оказался 5,85 (по отношению к воздуху); т. е. частичный вес его будет 5,85 · 28,9 = 169,06. Формуле C11H22 отвечает частичный вес 154, формулеC12H24 — 168, а C13H26 — 182. Формула C12H24 близко отвечает наблюденной величине, а потому она идолжна выражать собою величину частицы нашего углеводорода CH2.
