Промышленные методы получения альдегидов
Известно много методов синтеза альдегидов, однако их использование в промышленности зависит во многом от доступности исходного сырья. Основными промышленными методами получения насыщенных алифатических альдегидов являются[20]:
- гидроформилирование алкенов (оксосинтез);
- дегидрирование или окисление первичных спиртов;
- гидратация ацетилена;
- окисление этилена;
- окисление насыщенных углеводородов (С3, С4).
Также большое значение имеют некоторые специфические синтезы альдегидов, широко применяемых в парфюмерной промышленности[20].
Оксосинтез является наиболее важным процессом для получения альдегидов с тремя атомами углерода и выше. В этой реакции алкены реагируют с синтез-газом (CO + H2) с образованием альдегида, содержащего на один атом углерода больше, чем исходный алкен. При использовании несимметричных алкенов образуется смесь продуктов, соотношение которых можно варьировать путём подбора катализатора[20].
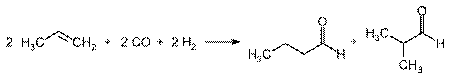
Среди процессов отщепления водорода от первичных спиртов различают дегидрирование, окисление и окислительное дегидрирование. Дегидрирование спиртов проводят при атмосферном давлении и температуре 250—400 °С в присутствии медного или серебряного катализатора. В ходе процесса выделяется водород, который можно использовать без очистки в других процессах. Дегидрирование имеет коммерческое значение в получении уксусного альдегида из этанола: реакцию проводят при 270—300 °С на медном катализатора, активированном церием, при этом за цикл превращается 25—50 % этанола с селективностью 90—95 %. Побочными продуктами являются этилацетат, этилен, кротоновый альдегид и высшие спирты. Окисление спиртов проводится в избытке воздуха или кислорода при 350—450 °С на катализаторе, содержащем оксиды железа и молибдена. Процесс используется в производстве формальдегида. Данные процессы также применяются в синтезе душистых альдегидов[20].
Окисление алкенов является основным промышленным методом получения ацетальдегида и акролеина. В первом случае окислению подвергается этилен в присутствии хлоридов палладия и меди Вакер-процесс [20][8].
C H 2 = C H 2 + P d C l 2 + H 2 O → C H 3 C H O + P d + 2 H C l {\displaystyle {\mathsf {CH_{2}{\text{=}}CH_{2}+PdCl_{2}+H_{2}O\rightarrow CH_{3}CHO+Pd+2HCl}}} 
P d + 2 C u C l 2 → P d C l 2 + 2 C u C l {\displaystyle {\mathsf {Pd+2CuCl_{2}\rightarrow PdCl_{2}+2CuCl}}} 
4 C u C l + 4 H C l + O 2 → 4 C u C l 2 + 2 H 2 O {\displaystyle {\mathsf {4CuCl+4HCl+O_{2}\rightarrow 4CuCl_{2}+2H_{2}O}}}  Процесс получения ацетальдегида, основанный на гидратации ацетилена, в последнее время потерял былое значение. Последние фабрики в Западной Европе, синтезирующие ацетальдегид по данной схеме, были закрыты в 1980 году. Причиной этому послужила бо́льшая доступность этилена в качестве сырья, а также токсичность катализатора — сульфата ртути[20]. Ежегодное мировое производство формальдегида (по данным на 1996 год) составило 8,7·106 т[21], ацетальдегида (на 2003 год) — 1,3·106 т[22]. Основным методом получения бензальдегида является гидролиз бензальхлорида в кислой или щелочной средах. В качестве гидролизующих агентов могут применяться гидроксид кальция, карбонат кальция, гидрокарбонат натрия, карбонат натрия, а также различные кислоты с добавлением солей металлов. Исходное сырьё, в свою очередь, получают при хлорировании толуола в боковую цепь. Менее распространённый процесс основан на частичном окислении толуола[23].
Процесс получения ацетальдегида, основанный на гидратации ацетилена, в последнее время потерял былое значение. Последние фабрики в Западной Европе, синтезирующие ацетальдегид по данной схеме, были закрыты в 1980 году. Причиной этому послужила бо́льшая доступность этилена в качестве сырья, а также токсичность катализатора — сульфата ртути[20]. Ежегодное мировое производство формальдегида (по данным на 1996 год) составило 8,7·106 т[21], ацетальдегида (на 2003 год) — 1,3·106 т[22]. Основным методом получения бензальдегида является гидролиз бензальхлорида в кислой или щелочной средах. В качестве гидролизующих агентов могут применяться гидроксид кальция, карбонат кальция, гидрокарбонат натрия, карбонат натрия, а также различные кислоты с добавлением солей металлов. Исходное сырьё, в свою очередь, получают при хлорировании толуола в боковую цепь. Менее распространённый процесс основан на частичном окислении толуола[23].
